Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Общая характеристика металловСтр 1 из 4Следующая ⇒
Общая характеристика металлов 1. Положение в периодической таблице, строение атомов металлов. 2. Характерные физические свойства металлов. 3. Общие химические свойства. Положение в периодической таблице, строение атомов металлов.
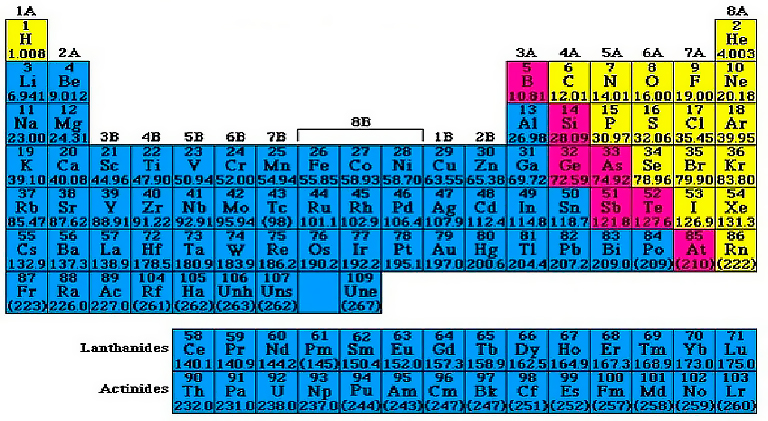
Металлы в периодической системе химических элементов Д.И.Менделеева находятся в левом нижнем углу по диагонали B-At, а далее в побочных подгруппах. Исключение: Н, Ве, В.
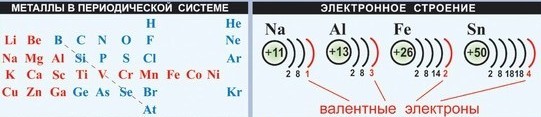
У металлов на последнем электронном слое от 1 до 3 электронов, следовательно, степень окисления от +1 до +3. Могут иметь степень окисления: +4, +5, +6, +7 металлы главных (IV - VI) и побочных подгрупп.
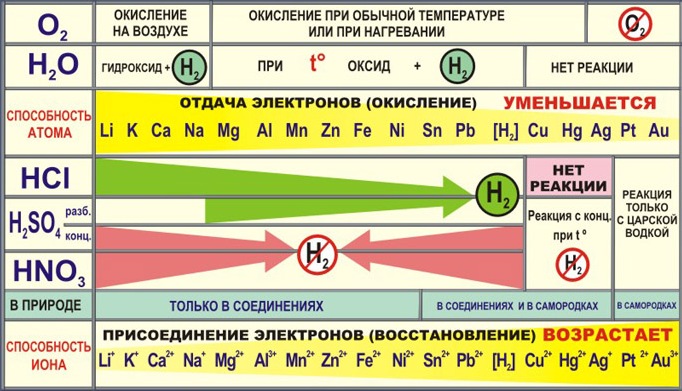
Металлы-восстановители. Восстановительные свойства в периоде ослабевают, радиус атома уменьшается, т.к. количество электронов на внешнем слое увеличивается. Увеличивается заряд ядра. Восстановительные свойства в группе усиливаются. Число электронов на внешнем электронном уровне не изменяется. Радиус атома увеличивается, следовательно металлические свойства усиливаются.
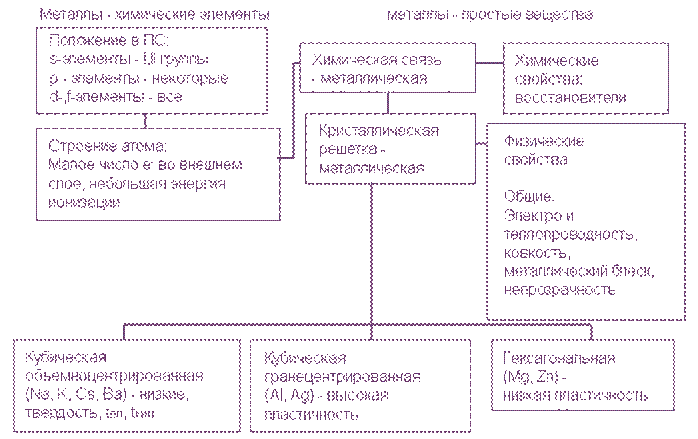
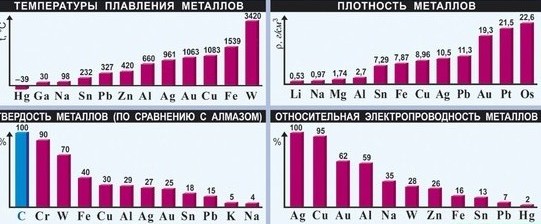
- s - элементы -металлы I и II группы А (кроме Н и Ве). Характерные физические свойства металлов. - Металлический блеск (характерен не только для металлов: его имеют и неметаллы йод и углерод в виде графита); - Хорошая электропроводность; - Возможность лёгкой механической обработки - пластичность; однако, некоторые металлы, например германий и висмут, непластичны; - Высокая плотность (обычно металлы тяжелее неметаллов); - Высокая температура плавления (исключения: ртуть, галлий и щелочные металлы); - Большая теплопроводность; - В реакциях всегда являются восстановителями.
Все металлы (кроме ртути и, условно, франция) при нормальных условиях находятся в твёрдом состоянии, однако они обладают различной твёрдостью. Так, щелочные металлы легко режутся кухонным ножом, а такие металлы, как ванадий, вольфрам и хром легко царапают самую твёрдую сталь и стекло.
Общие химические свойства.
Общие сведения о металлах
Вам известно, что большинство химических элементов от носят к металлам - 92 из 114 известных элементов. Металлы — это химические элементы, атомы ко торых отдают электроны внешнего (а некоторые — и предвнешнего) электронного слоя, превращаясь я положительные ионы. Это свойство атомов металлов, как вы знаете, определяется тем, что они имеют сравнительно большие радиусы и малое число электронов (в основном от 1 до 3) на внешнем слое. Исключение составляют лишь 6 металлов: атомы германия, олова, свинца на внешнем слое имеют 4 электрона, атомы сурьмы, висмута -5, атомы полония — 6. Для атомов металлов характерны небольшие значения электроотрицательности (от 0,7 до 1,9) и исключительно восстановительные свойства, то есть способность отдавать электроны. Вы уже знаете, что в Периодической системе химических алементов Д. И. Менделеева металлы находятся ниже диагонали бор—астат, я также выше нее в побочных подгруппах. В периодах и глинных подгруппах действуют известные вам закономерности в изменении металлических, и значит, восстановительных свойств атомов элементов.
Химические элементы, расположенные вблизи диагонали бор -астат, обладают двойственними свойствами: в одних своих соединениях ведут себя как металлы, в других — проявляют свойства неметалла. В побочных подгруппах восстановительные свойства металлов с увеличением порядкового номера чаще всего уменьшаются. Сравните активность известных вам металлов I группы побочной подгруппы: Сu, Аg, Аu; II группы побочной подгруппы — и вы убедитесь в этом сами. Это можно объяснить тем, что на прочность связи валентных электронов с ядром у атомов этих металлов в большей степени влияет величина заряда ядра, а не радиус атома. Величина заряда ядра значительно увеличивается, притяжение электронов к ядру усиливается. Радиус атома при этом хотя и увеличивается, но не столь значительно, как у металлов главных подгрупп.
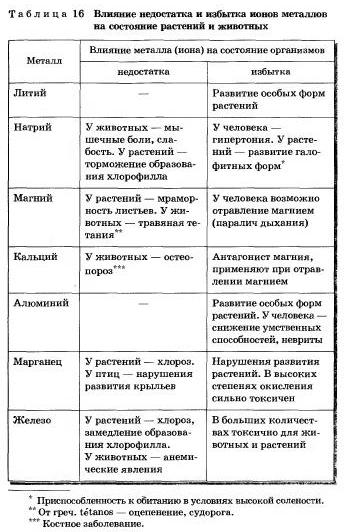
Простые вещества, образованные химическими элементами — металлами, н сложные металлсодержащие вещества играют важнейшую роль в минеральной и органической «жизни» Земли. Достаточно вспомнить, что атомы (ноны) элементов-металлов являются составной частью соединений, определяющих обмен веществ в организме человека, животных, растений. Например, в крови человека найдено 76 элементов и из них только 14 не являются металлами. В организме человека некоторые элементы-металлы (кальций, калий, натрий, магний) присутствуют в большом количестве, то есть являются макроэлементами. А такие металлы, как хром, марганец, железо, кобальт, медь, цинк, молибден, присутствуют в небольших количествах, то есть это микроэлементы. Если вес человека 70 кг, то в его организме содержится (в граммах): кальция — 1700, калия — 250, натрия — 70, магния — 42, железа — 5. цинка — 3. Все металлы чрезвычайно важны, проблемы со здоровьем возникают и при их недостатке, и при избытке. Например, ионы натрия регулируют содержание воды в организме, передачу нервного импульса. Его недостаток приводит к головной боли, слабости, слабой памяти, потери аппетита, а избыток — к повышению артериального давления, гипертонии, заболеваниям сердца. Специалисты по питанию рекомендуют потреблять в день не более 5 г (1 чайная ложка) поваренной соли (NaСl) на взрослого человека. О влиянии металлов на состояние животных и растений можно узнать из таблицы 16.
Простые вещества — металлы С развитием производства металлов (простых веществ) и сплавов связало возникновение цивилизации («бронзовый век», железный век). Начавшаяся примерно 100 лет назад научно-техническая революция, затронувшая и промышленность, и социальную сферу, также тесно связана с производством металлов. На основе вольфрама, молибдена, титана и других металлов начали создавать коррозионностойкие, сверхтвердые, тугоплавкие сплавы, применение которых сильно расширило возможности машиностроения. В ядерной и космической технике из сплавов вольфрама и рения делают детали, работающие при температурах до 3000 ºС. в медицине используют хирургические инструменты из сплавов тантала и платины, уникальной керамики на основе оксидов титана и циркония.
И конечно же мы не должны забывать, что в большинстве сплавов используют давно известный металл железо (рис. 37), а основу многих легких сплавов составляют сравнительно «молодые» металлы: алюминий и магний. Сверхновыми стали композиционные материалы, представляющие, например, полимер или керамику, которые внутри (как бетон железными прутьями) упрочнены металлическими волокнами, которые могут быть из вольфрама, молибдена, стали и других металлов и сплавов — все зависит от поставленной цели, необходимых для ее достижения свойств материала. Вы уже имеете представление о природе химической связи в кристаллах металлов. Напомним на примере одного из них — натрия, как она образуется.
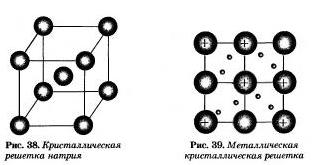
Единственный валентный электрон атома натрия Зs1 может занимать любую из девяти свободных орбиталей, ведь они не очень отличаются по уровню энергии. При сближении атомов, когда образуется кристаллическая решетка, валентные орбитали соседних атомов перекрываются, благодаря чему электроны свободно нере-мещаются с одной орбитали на другую, осуществляя связь между всеми атомами кристалла металла. Такой тип химической связи называют металлической. Металлическую связь образуют элементы, атомы которых на внешнем слое имеют мало валентных электронов по сравнению с большим числом внешних энергетически близких орбиталей. Их валентные электроны слабо удерживаются в атоме. Электроны, осуществляющие связь, обобществлены и перемещаются по всей кристаллической решетке в целом нейтрального металла.
Веществам с металлической связью присущи металлические кристаллические решетки, которые обычно изображают схематически тик, как показано на рисунке узлах находятся катионы и атомы металлов. Обобществленные электроны электростатически притягивают катионы металлов, расположенные в у ал их кристаллической решетки, обеспечивая ее стабильность и прочность (обобществленные электроны изображены в виде черных маленьких шариков). Металлическая связь — это связь в металлах и сплавах между атом-ионами металле, расположенными в уллах кристаллической решетки, которая осуществляется обобществленными валентными электронами. Некоторые металлы кристаллизуются в двух или более кристаллических формах. Это свойство веществ — существовать а нескольких кристаллических модификациях — называют полиморфизмом. Полиморфизм для простых веществ вам известен под названием аллотропия. Олово имеет две кристаллические модификации: Белое олово - очень мягкий металл. При охлаждении ниже 13,2 ºС он рассыпается в серый порошок, так как при переходе |1» п значительно увеличивается его удельный объем. Это явление получило название оловянной чумы. Конечно, особый вид химической связи и тип кристаллической решетки металлов должны определять и объяснять их физические свойства. Каковы же они? Это металлический блеск, пластичность, высокая электрическая проводимость и теплопроводность, рост злектрн чес кого сопротивления при повышении температуры, а также такие практически значимые свойства, как плотность, температуры плавления и кипения, твердость, магнитные свойства.
Давайте попробуем объяснить причины, определяющие основные физические свойства металлов. Почему металлы пластичны? Механическое воздействие на кристалл с металлической кристаллической решеткой вызывает смещение слоев ион-атомов относительно друг друга, в так как электроны перемещаются но всему кристаллу, разрыв связей не происходит, поэтому дли металлов характерна большая пластичность. Аналогичное воздействие на твердое вещество с коннлент-кыми связями (атомной кристаллической решеткой) приводит к разрыву ковалентных связей. Разрыв связей в ионной решетке приводит к взаимному отталкиванию одноименно заряженных ионов (рис. 40). Поэтому вещества с атомными и ионными кристаллическими решетками хрупкие. Наиболее пластичные металлы — это Аu, Af, Cu, Sn, РЪ, Zn. Они легко вытягиваются в проволоку, поддаются ковке, прессованию, прокатыванию в листы- Например, из золота можно изготовить золотую фольгу толщиной 0,008нм, в из 0,5 г этого металла можно вытянуть нить длинной 1 км. Даже ртуть, к ото рея, как вы знаете, при комнатной температуре жидкая, при низких температурах я твердом состоянии становится ковкой, как свинец. Не обладают пластичностью лишь Bi и Мn, они хрупкие. Способы получения металлов Значительная химическая активность металлов (взаимодействие с кислородом воздуха, другими неметаллами, водой, растворами солей, кислотами) приводит к тому, что в земной коре они встречаются главным образом в виде соединений: оксидов, сульфидов, сульфатов, хлоридов, карбонатов и т. д. В свободном виде встречаются металлы, расположенные в ряду напряжений правее водорода, хотя гораздо чаще медь и ртуть в природе можно встретить в виде соединений. Минералы и горные породы, содержащие металлы и их соединения, из которых выделение чистых металлов технически возможно и экономически целесообразно, называют рудами. Получение металлов из руд — задача металлургии. Чтобы реализовать этот процесс, надо учесть активность металла, подобрать восстановитель, рассмотреть технологическую целесообразность, экономические и экологические факторы. В соответствии с этим существуют следующие способы получения металлов: пирометаллургический. гидрометаллургический, электрометаллургический. Пирометаллургия - восстановление металлов из руд ори высоких температурах с помощью углерода, оксида углерода(П). водорода, металлов •- алюминия, магния. Например, олово восстанавливают из касситерита, а медь — из куприта прокаливанием с углем (коксом). Сульфидные руды предварительно подвергают обжигу при доступе воздуха, а затем полученный оксид восстанавливают углем. Из карбонатных руд металлы выделяют также путем накачивания а углем, так как карбонаты при нагревании разлагаются, превращаясь в оксиды, а последние восстанавливаются углем.
Гидрометаллургия — это восстановление металлов им их солей в растворе. Процесс проходит в 2 этапа: 1) природное соединение растворяют в подходящем реагенте для получении раствори соли этого металле; Затем медь извлекают из растворе соли либо:электролизом, либо вытесняют из сульфата железом. Таким способом получают серебро, цинк, молибден, золото, уран. Электрометаллургия — восстановление металлов в про цессе электролиза растворов или расплавов их соединений. Электролиз Если в раствор или расплав электролита опустить электроды и пропустить постоянный электрический ток, то ионы будут двигаться направленно: катионы — к катоду (отрицательно заряженному электроду), анионы - к аноду (положительно заряженному электроду). Па катоде катионы принимают электроны и восстанавливаются на аноде анионы отдают электроны и окисляются. Этот процесс называют электролизом. Простейший пример таких процессов электролиз расплавленных солей. Рассмотрим процесс электролиза расплава хлорида натрия. В расплаве идет процесс термической диссоциации. Под дейстиием алектрического тока катионы движутся к катоду и принимают от него электроны. Главное, что вы должны помнить: в процессе электролиза за счет электрической энергии осуществляется химическая реакция, которая самопроизвольно идти не может. Сложнее дело обстоит в случае электролиза растворов электролитов. В растворе соли, кроме ионов металла и кислотного остатка, присутствуют молекулы воды. Поэтому при рассмотрении процессов на электродах необходимо учитывать их участие в электролизе. Для определения продуктов электролиза водных растворов электролитов существуют следующие правила. 1. Процесс на катоде зависит не от материала катода, на которого он сделан, а от положения металла (катиона электролита) в электрохимическом ряду напряжений, при этом если: 1.1. Катион электролита расположен в ряду напряжений а начале ряда (по Аl включительно), то на катоде идет процесс восстановления воды (выделяется водород). Катионы металла не восстанавливаются, они остаются в растворе. Эти правила отражены на схеме 10. 2. Процесс на аноде зависит от материала анода и от природы аннона (схема 11). 2.1. Коли анод растворяется (железо, цинк. медь, серебро и все металлы, которые окисляются в процессе электролиза), то окисляется металл анода, несмотря на природу аниона. 2.2. Если анод не растворяется (его называют инертным — графит, золото, платина), то:
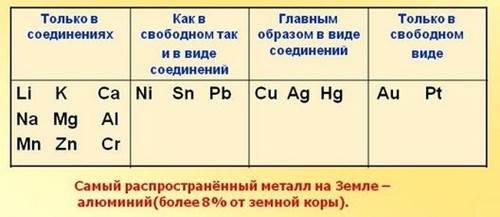
Электролиз расплавов н растворов веществ широко используют в промышленности: 1. Для получения металлов (алюминии, магний, натрий, кадмий получают только электролизом). Металлы в природе Если вы внимательно изучали химию в предыдущих классах, то вам известно, что таблица Менделеева насчитывает более девяноста видов металлов и приблизительно шестьдесят из них можно встретить в природной среде. Встречающиеся в природе металлы можно условно разделить на такие группы: • металлы, которые можно встретить в природе в свободном виде;
В отличие от других химических элементов, металлы довольно часто встречаются в природе в виде простых веществ. Они, как правило, имеют самородное состояние. К таким металлам, которые представлены в виде простых веществ, можно отнести золото, серебро, медь, платину, ртуть и другие. Но не все металлы, встречающиеся в природной среде, представлены в самородном состоянии. Некоторые металлы можно встретить в виде соединений и их называют минералами. Кроме того, такие химические элементы, как серебро ртуть и медь, можно встретить, как в самородном состоянии, так и в состоянии имеющих вид соединений. Все те минералы, из которых в дальнейшем можно получить металлы, называются рудами. В природе существуют руда, в состав которой входит железо. Такое соединение получило название железной руды. А если же в составе находится медь, но соответственно, такое соединение называется медной рудой. Конечно же, наиболее распространенными в природе являются металлы, которые активно взаимодействуют с кислородом и серой. Их принято называть оксидами и сульфидами металлов. Таким распространенным элементом, который образует металл, является алюминий. Алюминий содержится в глине, а также входит в состав таких драгоценных камней, как сапфир и рубин.
Вторым по популярности и распространению, является такой металл, как железо. Он, как правило, встречается в природе в виде соединений, а в самородном виде его можно встретить только в составе метеоритных камней. Следующими по распространению в природной среде, вернее в земной коре, являются такие металлы, как магний, кальций, натрий, калий. Интересные факты о металлах Держа в руке монеты, вы, наверное, замечали, что от них исходит характерный запах. Но, оказывается это не запах металла, а запах, который исходит от соединений, который образуется при соприкосновении металла с человеческим потом. А знали ли вы, что в Швейцарии налажен выпуск золотых слитков в форме шоколадной плитки, которую можно разломать на дольки и использовать в качестве подарка или платежного средства? Такие шоколадные плитки компания производит из золота, серебра, платины и палладия. Если такую плитку разломать на дольки, то каждая из них весит всего один грамм.
А еще, довольно таки интересным свойством обладает такой металлический сплав, как нитинол. Он уникален тем, что обладает эффектом памяти и при нагреве деформированное изделие из этого сплава способно возвращаться к своей первозданной форме. Такие своеобразные материалы с так называемой памятью применяют для изготовления втулок. Они обладают свойством при низких температурах сжиматься, а при комнатной температуре эти втулки распрямляются и это соединение является даже надежнее, чем сварка. А происходит такое явление благодаря тому, что эти сплавы имеют структуру термоупругости. А задумывались ли вы над тем, почему в золотые ювелирные изделия принято добавлять сплав серебра или меди? Оказывается, это происходит потому, что золото в чистом виде очень мягкое и его легко поцарапать даже с помощью ногтя. Источник — «http://edufuture.biz/index.php?title=%D0%9C%D0%B5%D1%82%D0%B0%D0%BB%D0%BB%D1%8B_(%D0%A5%D0%B8%D0%BC%D0%B8%D1%8F_11_%D0%BA%D0%BB%D0%B0%D1%81%D1%81)» |
Общая характеристика металлов
1. Положение в периодической таблице, строение атомов металлов.
2. Характерные физические свойства металлов.
3. Общие химические свойства.