
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Решение задач и упражнений по теме:Стр 1 из 4Следующая ⇒
Практическое занятие № 2. Решение задач и упражнений по теме: «Непредельные углеводороды». Цель: отработка практических умений и навыков на решении заданий по номенклатуре, изомерии непредельных углеводородов. 1) Задание: написать по одному изомеру на каждый вид изомерии для вещества: пентин –1, 3 – метилбутин – 1, пентадиен – 1,3. 2) Дано вещество: CH3 – CH = CH – CH3 | CH3 Напишите структурные формулы двух изомеров и двух гомологов, назовите их. 3) Решить задачи на вывод молекулярной формулы и расчеты по уравнению реакций. А) Найдите молекулярную формулу углеводорода ряда этилена, если массовая доля углерода в нем составляет 85,7%, а относительная плотность углеводорода по водороду равна 21. Б) Определите молекулярную формулу вещества, при сжигании 2,1 г которого получили 6,6 оксида углерода (IV) и 2.7 воды, плотность паров его по воздуху равна 2,9. 4) Осуществление превращения: C→ CH4→ CH3Cl→ C2H6→ C2H4 →C2H5OH Запишите уравнения реакций. Форма контроля: проверка тетрадей. Практическое занятие № 3. Решение задач и упражнений по теме: «Ароматические углеводороды». Цель: отработка практических умений и навыков на решении заданий по номенклатуре, изомерии ароматических углеводородов. Задания:
CH3 H3C – CH – CH3 | |
CH2 – CH3
CH3
а) 2 – метил – 3 – этилбензол б) 1 – метил – 4 – изобутилбензол в) 1, 3, 5 - триметилбензол
Форма контроля: проверка тетрадей. Практическое занятие № 4. Практическое занятие № 6 Изомерия, номенклатура, Химические свойства карбоновых кислот. Цель: отработка практических умений и навыков. Задания:
а) O2; б) H2O; в) CH3OH; г) CH; д) KOH. Составьте уравнения реакций.
Форма отчета: защита в парах сменного состава. Решить задачи. 1. В состав органического вещества входят 40% углерода, 6,66% водорода и 53, 34% кислорода. Найдите молекулярную формулу вещества и назовите его, если известно, что плотность паров по воздуху равна 2,07. 2. Сколько граммов уксусной кислоты можно получить из 112 л ацетилена. 3. Составить уравнения реакций, с помощью которых можно осуществить следующие превращения: А) СН4 --› СН3 С1 ---› СН3 ОН ---› НСНО ---› НСООН ---› НСООС 3Н7 Б) СН3 СН2 СОО Nа --› СН3 СН2 СООН --› СН3 СН С1 СООН --› СН3 СНС1СООС2 Н5--› С2 Н5 ОН Укажите тип и условия каждой реакции. 4. При сгорании сложного эфира (образованного одноосновными предельными спиртами и кислотами) массой 10,2 г образовалось 11,2 л оксида углерода (4) и 9 г воды. Определить молекулярную формулу этого вещества, составить структурные формулы не менее двух изомеров на разные виды изомерии и дать им названия по международной номенклатуре.
Форма отчета: совместная работа на уроке. Практическое занятие №7 «Углеводы». Заполните таблицу. Для этого расставьте «+», если согласны с утверждениями, данными ниже таблицы.
Форма контроля: проверка тетрадей. Практическое занятие № 8. Решение задач и упражнений. Цель: отработка практических умений и навыков. Задания:
C2H2 → C6H6 → C6H5NO2 → C6H5NH2 → C6H2Br3NH2
а) нитропропана; б) 1-нитробутана; в) 2-нитро – 2 – метилпропана.
а) HNO2; б) HCl; в) C2H5Br. 4. При взаимодействии смеси анилина, бензола и фенола массой 5 г с бромом образовался осадок. При обработке этой смеси гидроксидом натрия получилось вещество массой 2, 32 г, а при восстановлении всей смеси водородом образовался циклический углеводород массой 1,94 г. Определите массову4ю долю (%) веществ в смеси. Ответ: 26,4% C6H5NH2; 36% C6H6; 37,6% C6H5OH. Форма отчета: проверка тетрадей. Самостоятельная работа №4 Тема: Волокна. Тема: Значение и применение азотсодержащих. Вопросы для самостоятельного изучения: 1. Волокна и их свойства и классификация. Форма отчета: конспект в виде схемы. Вопросы для самостоятельного изучения: 1. Применение аминов. - красители - сульфамидные лекарственные препараты 2. Типы РНК и их биологические функции. Генная инженерия и биотехнология. Трансгенные формы растений и животных. Форма отчета: конспект. Самостоятельная работа №5 Вариант№1
1) sp 2 – гибридизации. 3) sp 3 - гибридизации 2) sp – гибридизации 4) sp 3 d 2 – гибридизации
СН3 СН3 I I СН3 – С = С – С – СН3
I I CН3 СН3 1) 1,1,2,3,3,3 – гексаметилпропен -1. 2) 2,3,4,4 – тетраметилпентен – 2 3) 2,3,4,4 – тетраметилпентен – 3. 4) 2,3,4,4,4 – пентаметилбутен – 2.
3. Общее число изомеров с формулой С4Н8 (учитывая структурную, геометрическую, межклассовую изомерию) равно … 1) 6; 2) 7; 3) 4; 4) 5.
4. Бромная вода обесцвечивается при пропускании через нее … 1) этена; 2) пропана; 3) этана; 4) метана.
5. При взаимодействии с пропена с хлороводородом образуется … 1) 1,2 – дихлорпропан; 2) прпанол -2; 3) 1 – хлорпропан; 4) 2 – хлорпропан.
6. Реакция присоединения водорода к непредельным УВ – это реакция … 1) гидрогалогенирования; 2) гидрирования; 3) галогенирования; 4) гидратация.
7. Реакция получения хлорэтана из этена – это реакция.. 1) отщепления; 2) замещения; 3) присоединения; 4) перегруппипровки.
8. Общая формула алкадиенов … 1) СnH2n-2 2) СnH2n+2 3) СnH2n 4) СnH2n-6 9. При действии воды на СаС2 образуется … 1) этан; 2) этен; 3) этин); 4) метан.
10. При гидрировании ацетилена избытком водорода образуется … 1) бензол; 2) этан; 3) этен; 4) бутан.
11. Вулканизация это – процесс нагревания каучука с … 1) сажей; 2) фосфором; 3) бромом; 4) серой.
12. Реакция Лебедева это реакция … 1) гидрирования и гидратации 2) гидрирования и дегидратации 3) дегидрирования и гидратации 4) дегидрирования и дегидратации.
13. Пропуская над нагретым до 4000 активированным углем … можно получить бензол. 1) метан, 2) этен, 3) ацетилен, 4) этан.
14. Для бензола возможны следующие типы реакций 1) только присоединения, 2) только замещения, 3) и замещения, и присоединения, 4) ни замещения, ни присоединения.
15. Толуол – это … 1) метилбензол, 2) 1,2 – диметилбензол, 3) 1,3 – диметилбензол, 4) 1,4 – диметилбензол Вариант№2
1) 0,154 нм; 2) 0, 140нм; 3) 0,134; 4) 0,120. 2. Назовите соединение СН3 I СН3 – С - С = СН – СН3 I I CН3 СН3 1) 3,4,4,4 – тетраметилбутен -2. 2) 2,2,3 – триметилпентен – 3 3)1,1,1,2 – триметилбутен – 2 4) 3,4,4 – триметилпентен – 2.
3. Общее число изомеров с формулой С4Н8 (учитывая структурную, геометрическую, межклассовую изомерию) равно … 1) 6; 2) 7; 3) 4; 4) 5.
4. Фиолетовый раствор перманганата калия обесцвечиваются при пропускании через него … 1) бутана; 2) пропана; 3) этана; 4) пропена.
5. При взаимодействии бутена – 1 с бромоводородом образуется … 1) 1, 2 – дибромбутан; 2) 1 – бромбутан; 3) 2 – бромбутан; 4) бутанол -2.
6. Реакция полимеризации – это реакция … 1) присоединения; 2) замещения; 3) отщепления; 4) перегруппипровки.
7. Реакция отщепления воды – это реакция … 1) дегидрирования; 2) дегидратации; 3) дегидрогалогенирования; 4) перегруппипровки.
8. Общая формула алкинов … 1) СnH2n-2 2) СnH2n+2 3) СnH2n 4) СnH2n-6
9. Степень окисление и валентность атома углерода в ацетилене равны соответственно… 1) -1 и 4; 2) -4 и 4; 3) -1 и 2; 4) 1 и 4.
10. При гидрировании бутадиена – 1, 3 избытком водорода образуется … 1) бензол; 2) этан; 3) этен; 4) бутан.
11. Резина по сравнению с каучуком … 1) менее эластична и более износостойкая 2) более эластична и более износостойкая 3) более эластична и менее износостойкая 4) менее эластична и менее износостойкая
12. В натуральном каучуке элементарные звенья находятся … 1) только в транс – конфигурации 2) и в цис - и в транс – конфигурации 3) только в цис – конфигурации 4) или только в цис -, или только в транс – конфигурации
13. Общая формула гомологов бензола… 1) СnH2n-2 2) СnH2n+2 3) СnH2n 4) СnH2n-6
14. В молекуле бензола атом углерода находится в состоянии 2) sp 2 – гибридизации. 3) sp 3 - гибридизации 3) sp – гибридизации 4) sp 3 d 2 – гибридизации 15. Для бензола возможны следующие типы реакций 1) только присоединения, 2) только замещения, 3) и замещения, и присоединения, 4) ни замещения, ни присоединения.
Ким №7 по теме «Углеводы»
Практическое занятие № 2. Решение задач и упражнений по теме: «Непредельные углеводороды». Цель: отработка практических умений и навыков на решении заданий по номенклатуре, изомерии непредельных углеводородов. 1) Задание: написать по одному изомеру на каждый вид изомерии для вещества: пентин –1, 3 – метилбутин – 1, пентадиен – 1,3. 2) Дано вещество: CH3 – CH = CH – CH3 | CH3 Напишите структурные формулы двух изомеров и двух гомологов, назовите их. 3) Решить задачи на вывод молекулярной формулы и расчеты по уравнению реакций. А) Найдите молекулярную формулу углеводорода ряда этилена, если массовая доля углерода в нем составляет 85,7%, а относительная плотность углеводорода по водороду равна 21. Б) Определите молекулярную формулу вещества, при сжигании 2,1 г которого получили 6,6 оксида углерода (IV) и 2.7 воды, плотность паров его по воздуху равна 2,9. 4) Осуществление превращения: C→ CH4→ CH3Cl→ C2H6→ C2H4 →C2H5OH Запишите уравнения реакций. Форма контроля: проверка тетрадей. Практическое занятие № 3.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-04-12; просмотров: 169; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.186.6 (0.08 с.) |








 а) б)
а) б) 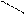



 СH3
СH3
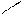
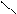 CH
CH 


