
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Гальванические преобразователиСодержание книги
Поиск на нашем сайте Принцип действия гальванических преобразователей основан на зависимости ЭДС гальванической цепи от концентрации ионов в электролите и окислительно-восстановительных процессов, происходящих на электродах. Они используются для определения концентрации ионов в различных растворах. Наиболее широкое применение гальванические преобразователи получили в качестве преобразователей pH-метров – приборов для измерения активности (концентрации) водородных ионов [3]. При этом концентрация водородных ионов определяется по разности потенциалов, которая возникает на электродах, опущенных в исследуемый раствор. Известно, что дистиллированная вода имеет слабую, но вполне определенную электрическую проводимость, что объясняется ионизацией воды, которая происходит по схеме
При равновесии процессов диссоциации (образования ионов) и образования из ионов молекул воды произведение концентраций положительных [ Таким образом, растворы, в которых число ионов водорода [ При растворении в воде кислоты увеличивается концентрация положительных ионов [ При растворении в воде щелочи увеличивается концентрация [ Концентрацию водородных ионов характеризуют так называемым водородным показателем pH = – lg[ Для измерения концентрации водородных ионов, т. е. для определения pH, применяется метод, основанный на измерении электродного (пограничного) потенциала между водородом и раствором, содержащим ионы [ Так как измерить абсолютное значение потенциала невозможно, его измеряют относительно другого потенциала. Поэтому гальванический преобразователь всегда состоит из двух полуэлементов, электрически соединенных друг с другом: рабочего (измерительного), представляющего собой исследуемый раствор с электродом, и сравнительного (образцового) с неизменным пограничным потенциалом, состоящего из электрода и раствора с постоянной концентрацией [3], [4]. В качестве сравнительного полуэлемента можно использовать водородный электрод с нормальной постоянной концентрацией водородных ионов. При промышленных измерениях применяется более удобный сравнительный каломельный электрод. Широко используются также стеклянные электроды. Приборы, предназначенные для анализа жидких растворов по водородному показателю (pH-метры), широко применяются для контроля различных химических процессов. Они состоят соответственно из гальванического преобразователя и измерительного устройства. Основной влияющей величиной при измерении pH является температура. С изменением температуры анализируемой жидкости меняются потенциалы измерительного и сравнительного электродов. Выходной сигнал гальванической ячейки с ростом температуры увеличивается в первом приближении по линейному закону [4]. Известны схемы pH-метров, у которых предусмотрена коррекция показаний в зависимости от температуры анализируемой жидкости [17]. ЭДС гальванических преобразователей измеряется при помощи автоматических компенсаторов с большим входным сопротивлением (не менее 1010Ом).
|
||
|
Последнее изменение этой страницы: 2021-04-05; просмотров: 203; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.15 (0.006 с.) |

 .
. ] и отрицательных [
] и отрицательных [ 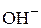 ] ионов в воде практически постоянно (при постоянной температуре) и равно
] ионов в воде практически постоянно (при постоянной температуре) и равно  (моль/л)2, причем в чистой воде концентрации положительных и отрицательных ионов одинаковы и равны
(моль/л)2, причем в чистой воде концентрации положительных и отрицательных ионов одинаковы и равны 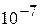 моль/л.
моль/л.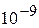 , то pH = 9. Обозначение pH было введено в 1907 г. датским химиком Серенсеном по начальным буквам латинских слов «pondus Hydrogenic», что означает в переводе «вес водорода». Растворы с pH < 7 являются кислыми, а растворы с pH > 7 – щелочными.
, то pH = 9. Обозначение pH было введено в 1907 г. датским химиком Серенсеном по начальным буквам латинских слов «pondus Hydrogenic», что означает в переводе «вес водорода». Растворы с pH < 7 являются кислыми, а растворы с pH > 7 – щелочными.


