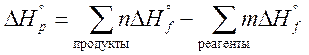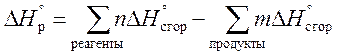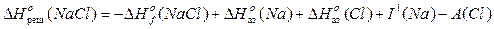Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Основные положения и понятияСодержание книги
Поиск на нашем сайте Ø Большинство химических реакций сопровождаются тепловым эффектом (изменением энтальпии). Энтальпия (H) – функция состояния, описывающая теплосодержание химической системы при постоянном давлении (теплосодержание расширяющейся системы): H ≡ U – pV, H ≡ Qp. Единицы измерения джоули (Дж) или калории (кал). Изменение энтальпии реакции (D H р) – тепловой эффект химической реакции при постоянном давлении (изобарный процесс). Ø По знаку величины изменения энтальпии (теплового эффекта) реакции различают экзотермические и эндотермические химические реакции. Экзотермические реакции – в процессе реакции тепло выделяется во внешнюю среду (D H <0) Эндотермические реакции – в процессе реакции тепло поглощается из внешней среды (D H >0) Ø Химические реакции приводят не только к изменению природы реагирующих веществ, но и к изменению их внутренней энергии Внутренняя энергия вещества (U) – все виды энергии, кроме потенциальной и кинетической энергии системы в целом. Ø Стандартная энтальпия образования вещества (D H ° f) – изменение энтальпии при образовании 1 моля сложного вещества из простых веществ, взятых при стандартных условиях в их наиболее устойчивых модификациях; измеряется в кДж/моль. Стандартные условия – температура 25°С (298 К), давление 1 атм. (101 325 Па). Ø Энтальпии образования простых веществ в стандартных условиях в их наиболее устойчивых модификациях приняты равными нулю. Ø Стандартная энтальпия сгорания (D H °сг.) – изменение энтальпии при реакции сгорания 1 моля вещества в атмосфере кислорода при давлении 1 атм. Ø Стандартная энтальпия атомизации (D H ° ат) [2] – изменение энтальпии при образовании 1 моля газообразных атомов из простого вещества. Законы и следствия 1. Закон Лавуазье-Лапласа 2.
Тепловой эффект химической реакции зависит только от состояния исходных веществ и продуктов реакции и не зависит от числа промежуточных стадий, т.е. от пути протекания процесса C(графит) + 1/2 O2 (г) = CO (г) D H ° 1 + CO(г) + 1/2 O2 (г) = CO2 (г) D H ° 2 3. Следствия из закона Гесса 2. Изменение стандартной энтальпии химической реакции равно разности сумм стандартных энтальпий образования продуктов и стандартных энтальпий образования исходных веществ (с учетом количеств реагирующих веществ, т.е. стехиометрических коэффициентов).
3. Тепловой эффект реакции равен сумме теплот сгорания исходных веществ за вычетом суммы теплот сгорания продуктов, с учетом их стехиометрических коэффициентов.
Энтальпийные диаграммы. Циклы Борна-Габера Расчет энергии кристаллической решетки. Энергия кристаллической решетки – теплота, выделяющаяся при образовании решетки из газообразных ионов. Энтальпия образования кристаллической решетки – отрицательна (экзотермична), т.к. идет процесс образования химических связей. Кристаллическая решетка – это решетка, состоящая из упорядоченно расположенных ионов (атомов).
I 1 – первый потенциал ионизации натрия Потенциал ионизации – энергия, необходимая для отрыва одного электрона от нейтрального газообразного атома и удаления его на бесконечно большое расстояние А – энергия сродства к электрону хлора Сродство к электрону – энергия, выделяющаяся при присоединении одного электрона, находящегося на бесконечно большом расстоянии от атома, к нейтральному газообразному атому.
|
|||||||||||
|
Последнее изменение этой страницы: 2021-04-05; просмотров: 138; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.16 (0.006 с.) |