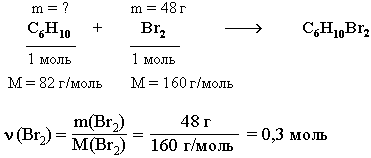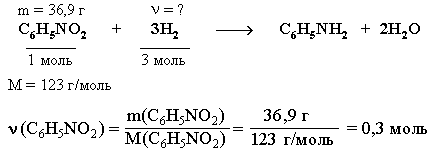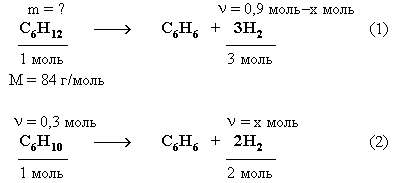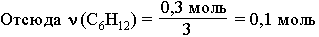Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Расчет массы, объема и количества исходных веществ или продуктов реакции с учетом примесей ⇐ ПредыдущаяСтр 3 из 3
Задача. Определить массу образца технического углерода, содержащего 3% примесей, необходимого для получения 67,2 л (н.у.) метана.
Расчет массы, объема и количества исходных веществ или продуктов реакции с учетом концентрации их в растворе (смеси) Задача. Сколько грамм бромной воды с массовой долей брома 3,2% потребуется для реакции с 10 л смеси этана и этилена, в которой объемная доля этилена равна 28%?
Расчет массы, объема и количества веществ с учетом выхода продукта реакции Задача. Бензол количеством вещества 0,5 моль прореагировал с избытком брома (в присутствии катализатора). При этом получили бромбензол массой 70 г. Определите массовую долю выхода бромбензола.
Задачи повышенной трудности
На олимпиадах предлагаются более сложные задачи, чем рассмотренные ранее. Обычно в них сочетаются различные типы расчетов – как по формулам веществ, так и по уравнениям реакций. Решение таких задач требует не только глубоких знаний химии, но и развитого логического мышления, владения алгебраическим аппаратом (системы уравнений с несколькими неизвестными, неравенства, степенные и логарифмические функции и т.п.). Рассмотрим решение одной из олимпиадных задач. Задача. При дегидрировании смеси циклогексана и циклогексена в бензол выделился водород массой, достаточной для полного восстановления 36,9 г нитробензола в анилин. Найти %-ный (по массе) состав исходной смеси, если известно, что такая же масса этой смеси может обесцветить 480 г 10%-ного раствора брома в CCl4.
1. Определим m(Br2) в растворе СCl4:
m(Br2) = m(раствора) *ω(Br2) = 480 г * 0,1 = 48 г
2. Из углеводородов исходной смеси с Br2 реагирует только циклогексен С6Н10, являющийся ненасыщенным соединением. По уравнению этой реакции рассчитаем массу С6Н10.
ν (С6Н10) = ν (Br2) = 0,3 моль m(C6Н10) = ν (С6 Н10) * M(С6 Н10) = 0,3 моль * 82 г/ моль = 24,6 г
ν (Н2) = 3*ν (С6Н5NO2) = 0,9 моль
Из уравнения (2) следует, что x = ν (H2) = 0,6 моль. Тогда количество водорода, выделившегося в реакции (1) равно:
ν (Н2) = 0,9 моль – 0,6 моль = 0,3 моль.
m(C6H12) = ν (C6H12) * M(C6H12) = 0,1 моль * 84 г/моль = 8,4 г
5. Определим массу исходной смеси углеводоров:
m(смеси) = m(C6H12) + m(C6H10) = 8,4 г + 24,6 г = 33,0 г
Ответ: ω (С6Н10) = 0,745 (74,5%) ω (С6Н12) = 0,255 (25,5%)
Примечание: знаком * отмечены задачи повышенной трудности
1. Какое количество вещества составляет 92 г этанола С2Н5ОН? 2. Определите массу глюкозы, содержащей 0,6 моль атомного углерода. 3. Определите массовую долю кислорода (в %) в метиловом спирте, состав которого выражен формулой СН3ОН. 4. Какой объем водорода (н.у.) может присоединить смесь газов массой 15,4 г, которая содержит этилен (ω = 54,5%), пропилен (ω = 27,3%) и бутилен (ω = 18,2%). 5. Природный газ одного из месторождений содержит метан (ω = 92%), этан (ω = 3%), пропан (ω = 1,6%), бутан (ω = 0,4%), азот (ω = 2%), другие газы (ω = 1%). Определите массу органических веществ, входящих в состав 20 л (н.у.) природного газа. 6. При сгорании алкана массой 3,6 г образуется оксид углерода (IV) объемом 5,6 л (н.у). Плотность алкана по водороду равна 36. Установите молекулярную формулу алкана. 7. Вывести молекулярную формулу вещества, если оно содержит С (ω = 39,97%), Н (ω = 6,73%) и О (ω = 53,3%) и 300 мл паров этого вещества (н.у.) имеют массу, равную 2,41 г. 8. Сколько г хлора потребуется для превращения 19 г бензола С6Н6 в гексахлоран С6Н6Сl6? 9. При нагревании иодметана СH3I массой 2,84 г с металлическим натрием массой 0,69 г получили этан С2Н6 объемом 179,2 мл при н.у. Определите объемную долю выхода продукта реакции. 10. Сколько граммов 80% - го технического карбида кальция CaC2 потребуется для получения 2,8 л ацетилена при н.у.? 11. Сколько граммов толуола С7Н8 потребуется для получения 113,5 г тринитротолуола С7Н5(NO2)3, если массовая доля выхода продукта составляет 80% от теоретически возможного? 12. Какую массу бромной воды с массовой доле брома 1,6% может обесцветить пропилен объемом 1,12 л (н.у.)? 13. Какой объем воздуха потребуется для сжигания 30 л ацетилена С2Н2 (н.у.), содержащего 5% негорючих примесей? Содержание кислорода в воздухе считать равным 20% по объему.
14. Сколько л водорода (н.у.) выделится при каталитическом дегидрировании 49 г метилциклогексана в толуол, если объемная доля выхода продукта равна 75% от теоретически возможного? 15*. При сгорании 13,44 л (н.у.) смеси монооксида углерода, метана и ацетилена образовалось 17,99 л СО2 (н.у.) и 9 г Н2О. Сколько литров каждого газа содержится в смеси? 16*. При взаимодействии 11,2 г алкена с бромоводородом получено 27,4 г вещества. Напишите формулы всех возможных изомеров алкена. 17*. Анализ смеси метана и ацетилена показал, что общее содержание углерода в смеси по массе равно 88, 46%. Определите состав смеси в % по массе. 18*. При сгорании 14,6 г хлорсодержащего органического вещества было получено 13,44 л СО2 и 3,6 г Н2О. Весь хлор, содержавшийся в навеске, вдвое меньшей, чем исходная, переведен в AgCl массой 14,3 г. Плотность по водороду исследуемого хлорорганического вещества равна 74. Определите молекулярную формулу этого вещества. 19*. Какой объем хлороводорода может прореагировать с 15 г смеси, состоящей из равных массовых долей триметиламина, пропиламина и метилэтиламина? 20*. При окислении одноатомного спирта массой 11,2 г кислородом воздуха в присутствии катализатора при 500°С образовалась кислота, на нейтрализацию которой потребовалось 59,4 мл 20% раствора КОН (d=1,18 г/мл). Какова формула исходного спирта?
|
||||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 269; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.225.255.134 (0.01 с.) |