
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
II .7. Диссоциация комплексных соединений.
Комплексные соединения диссоциируют на ионы внутренней и внешней сферы, например: Cu3[ Cr (CN)6]2 = 3Cu2+ + 2 [ Cr (CN)6]3- [Zn(H2O)4 ] I2 = [Zn(H2O)4 ]2+ +2I-
r Упражнение для самостоятельного решения: Напишите уравнения диссоциации для комплексных соединений: H2[PtBr6], [Fe(H2O)6]2 (SO)4, Ca[Sn(OH)6],Mg3[ Al (CN)6]2.
p Комплексные ионы могут ионизировать далее, но поскольку связь между комплексообразователем и лигандами - ковалентная неполярная, то ионизации идет слабо, ступенчато. Например:
________________________________________________________________
Суммарное уравнение:
Об устойчивости комплексных ионов (комплексов) судят по константе устойчивости или константе нестойкости комплексного иона: для 2-ой ступени константа нестойкости будет иметь вид: [ [Cr (CN)2] + ] * · [ CN- ] *
[[ Cr (CN)3] 0] * · здесь величины в квадратных скобках - равновесные молярные концентрации ионов (моль/л). Чем больше величина константы нестойкости, тем менее прочный комплексный ион. Величина обратная константе нестойкости называется константой устойчивости. Чем больше ее значение, тем устойчивее ион: [ [ Cr (CN)3] ] 0
[[Cr (CN)2] +] · [CN-]
II.8. Получение некоторых комплексных соединений: 1. AgBr + 2 Na2S2O3 à Na3[Ag(S2O3)2] + NaBr натрия дитиосульфатоаргенат (I) К осадку бромида серебра прилить раствор тиосульфата натрия. Наблюдается растворение соли. Получается комплексное соединение.
2. К свежеприготовленному осадку хлорида серебра прилить раствор 10 %-го раствора гидроксида аммония. Осадок растворяется. Реакция протекает по уравнению:
AgCl + 2 NH4OH à [Ag(NH3)4]Cl + 2 H2O хлорид тетраамминсеребра (1) Данное комплексное соединение можно разрушить, например, при помощи азотной кислоты: [Ag(NH3)4]Cl + 2 HNO3 à 2 NH4NO3 + AgClI [Ag(NH3)4]+ + Cl- + 2 H+ à 2 NH4+ + AgClI p Катион аммония, который может быть представлен как комплекс, является более устойчивым, чем комплекс тетраамминсеребра (I). Его константа нестойкости меньше, а константа устойчивости больше последнего.
3. При растворении бурого осадка оксида серебра (I) в растворе аммиака происходит образование бесцветногораствора комплексного соединения гидроксида тетраамминсеребра (I) гидроксида: Ag2О + 4 NH4OH à 2 [Ag(NH3)4]ОН + 3 H 2O 4. Получение комплексных соединений меди (+2) – аммиакатов из нерастворимых гидроксида меди (+2) и гидроксосульфата меди (+2). Цвет полученных растворов - темно-синий, очень насыщенный. В реакцию берут свежеприготовленные осадки: A) CuSO4 + 2 NaOH à Cu(OH)2↓ + Na2SO4 Cu(OH)2 + NH4OH à [Cu(NH3)4](OH)2 тетраамминмеди(+2) гидроксид Б) 2 CuSO4 + 2 NH4OH à (CuOH)2SO4 ↓ + (NH4)2SO4 гидроксосульфат меди (+2) (CuOH)2SO4 + 6 NH4OH + (NH4)2SO4 à 2 [Cu(NH3)4] SO4 + 8 H2O
Суммарно: CuSO4 + + 4 NH4OH à [Cu(NH3)4] SO4 + 4 H2O тетраамминмеди(+2) сульфат
II.9. Значение и применение комплексных соединений. 1.Знание строения и свойств комплексных соединений необходимо в методе анализа - комплексонометрии при определении ионов: Zn2+, Mg2+, Ca2+, Ba2+, Cd2+. p Комплексонометрический метод основан на реакции комплексообразования катионов металлов с комплексонами. Комплексонами являются, например,
А) этилендиаминтетрауксусная кислота (ЭДТУК) – четырехосновная кислота: HOOCCH2 CH2COOH
\ / N-CH2-CH2 – N / \ HOOCCH2 CH2COOH (H4Y –сокращенное название) Б) трилон Б – двузамещенная натриевая соль этилендиаминтетрауксусной кислоты- Na2H2Y. Распространенное название этого комплексона – ЭДТА (этилендиаминтетраацетат). Максимальная дентатность его равна шести и при образовании комплексных соединений – комплексонатов возникает несколько хелатных циклов, поэтому комплексы обладают высокой устойчивостью. Ион металла М2+ (например, Са2+ и Мg2+) замещает в ЭДТА два атома водорода карбоксильных групп и связывается еще с атомами азота донорно-акцепторной связью: O=C-O O-C=O | \ / |
H2C CH2 \ /
/ \ HOOCH2C CH2COOH
Металл 3+ замыкает еще одно кольцо с СООН- группой. 2. Некоторые органические вещества могут использоваться как лиганды для связывания вредных ионов и выведения их из организма. 3. Комплексные соединения получаются во многих химических реакциях.
II.10. Кристаллогидраты солей можно рассматривать, как комплексные соединения. В водных растворах все ионы окружены молекулвми воды, то есть, гидратированы. Реализуя определенное координационное число, эти ионы существуют в виде комплексов, хотя часть молекул воды может быть во внешней сфере: CuSO4∙5H2O - медный купорос - пятиводный кристаллогидрат сульфата меди (II). Координационное число иона меди (Cu2+) = 4 Формула медного купороса в виде комплексного соединения: [Cu(H2O)4]SO4∙H2O монокристаллогидрат пентааквамеди (II) cульфата II.11. Двойные соли. KAl(SO4)2 - сульфат калия, алюминия. Имеют ионную связь (между атомами металлов и кислорода) и ковалентную связь (между атомами неметаллов). В твердом состоянии эти соли можно отнести к комплексным соединениям в твердом состоянии. В растворах же такие соли полностью диссоциируют на ионы. K-O O \ // S / \\ O O
Al –O O à K+ + Al3+ + 2 SO42-
S / \\ O O
ПРИЛОЖЕНИЕ Названия некоторых лигандов
Таблица растворимости неорганических соединений
Ряд напряжений металлов
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 362; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.224.33.107 (0.024 с.) |
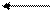
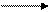 [ Cr (CN)4]- [Cr (CN)3] 0 + CN- (1 ступень)
[ Cr (CN)4]- [Cr (CN)3] 0 + CN- (1 ступень)
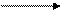 [ Cr (CN)3] 0 [Cr (CN)2] + + CN- (2 ступень)
[ Cr (CN)3] 0 [Cr (CN)2] + + CN- (2 ступень)
 [ Cr (CN)2] + [Cr (CN)] 2+ + CN- (3 ступень)
[ Cr (CN)2] + [Cr (CN)] 2+ + CN- (3 ступень)
 [ Cr (CN)] 2+ Cr 3+ + CN- (4 ступень)
[ Cr (CN)] 2+ Cr 3+ + CN- (4 ступень)
 [ Cr (CN)4]- Cr 3+ + 4CN-
[ Cr (CN)4]- Cr 3+ + 4CN-  К нест. =
К нест. = 
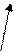 | M |
| M |
 N N
N N H2 C CH2
H2 C CH2
 \ //
\ //


