Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Нитро- и аминосоединения ароматического ряда ⇐ ПредыдущаяСтр 2 из 2
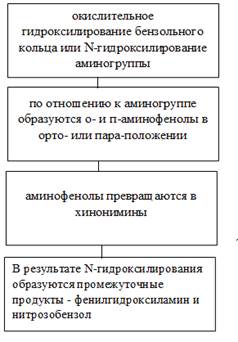
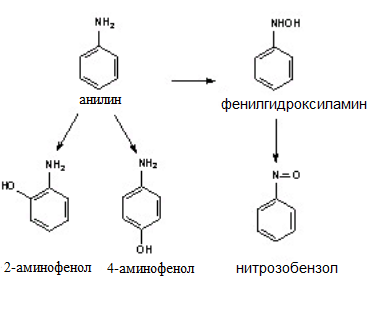
Характерными представителями группы нитро- и аминосоединений ароматического ряда являются нитробензол и анилин, которые схожи по механизму токсического действия, физико-механическим свойствам и развивающимися симптомам при острой интоксикации. Анилин-это ядовитое химическое вещество с характерным аммиачным запахом. Внешне выглядит, как бесцветная маслянистая жидкость. Взрывоопасен,при температуре от 75 °C образует взрывоопасные соединения. Широко используется в производстве различных красителей-ручки,карандаши. У людей наблюдается разная чувствительность к анилину. ПДК анилина в воздухе составляет от 0,1 мг/м ^3 до 0,6 мг/м^ 3.При более высоких концентрациях возникает острая интоксикация. Данное химическое вещество в виде паров всасывается через кожные покровы или через дыхательные пути и поступает в кровь, где происходит равномерное распределение в органах и тканях. Анилин способен к биотрансформации,протекает в 2 этапа.1 этап представлен на рисунке 2.1
Рис.2.1 1 этап процесса биотрансформации.
На следующем этапе фенилгидроксиамин и нитрозобензол вступают в реакции конъюгации с глюкуроновой, серной кислотами и глутатионом, а также в реакцию N-ацетилирования. Конъюгаты - высоко полярные, нетоксичные соединения выводятся из организма через почки. Процесс биотрансформации протекает в печени. Механизм действия нитро- и аминосоединений неразрывно связан с их метаболизмом. Метгемоглобин образуется в следствии активации свободнорадикальных процессов в эритроцитах.На рисунке 2.2 представлен механизм токсического действия.
Рис.2.2. Механизм токсического действия
Нитриты Нитриты - это производные азотистой кислоты. Различные представители данной группы веществ во многом схожи по механизму токсического действия и клинической картине острого отравления. Метгемоглобинобразующей активностью обладают неорганические производные, расслабляющим действием на стенки кровеносных сосудов-органические представители. Нитрит натрия(NaNO₂)-ядовитое химическое вещество, которое при попадании в организм человека вызывает отравления. Внешне представляет из себя порошок желтоватого цвета. Температура плавления составляет 271 ℃. При нагревании может разлагаться с образованием токсичных газов. Растворим в воде,по вкусу напоминает поваренную соль.
ПДК нитрита натрия в воздухе рабочей зоны составляет 0,1 мг/м^3. В организм попадает через рот, путем проглатывания зараженной пищи и воды, часть вещества окисляется до нитратов, часть восстанавливается до оксида азота, часть превращается в нитрозоамины, значительная часть выводится в неизменённом виде через почки. Механизм токсического действия нитритов связан с тем,что в организме быстро выделяются оксид азота и нитритная группа. Окись азота, который и в норме постоянно образуется в организме и выполняет функцию регулятора сосудистого тонуса, действует на соответствующие рецепторы. Возбуждение окиси азота-рецепторов вызывает расслабление сосудистой стенки и в тяжелых случаях приводит к остро развивающейся сосудистой недостаточности. Нитрит-ион вызывает метгемоглобинообразование. Механизм действия сложен и вероятно связан с формированием окислительно-восстановительной пары “нитрит-нитрат”, активирующей свободно-радикальный процесс в эритроцитах, а также с угнетением активности метгемоглобинредуктаз, супероксиддисмутазы и каталазы [7]. Заключение Итак, можно сделать вывод, что отравления различными химическими веществами может быть вызвано целым рядом причин. Одной из главных является несоблюдение техники безопасности, в результате которой человек подвергает себя опасности. Так же отравления могут возникать по причине халатного отношения взрослого к ребенку. Из-за невнимательности взрослого, дети, в силу своей любопытности, могут проглотить опасное химическое вещество. При первых симптомах отравления необходимо сразу же обращаться в медицинские учреждения за оказанием необходимой помощи. Помните, что самолечение может приводить к трагическим ситуациям.
Список литературы 1.Отравление окисью углерода [Электронный ресурс]. https://www.ismu.baikal.ru/ismu/news.php/ URL:https://www.ismu.baikal.ru/src/downloads/9e233aa2_zobnin_yu.v._so-metod.rekomendatsii.pdf 2.Отравления метгемоглобинообразователями,лечение,причины,симптомы,профилактика. [Электронный ресурс]. https://www.pitermed.com/ URL: https://www.pitermed.com/simptomy-bolezni/?cat=18&word=63832
3. Углерод и его соединения // Вредные вещества в промышленности: Справочник для химиков, инженеров и врачей. Т. III. Неорганические и элементоорганические соединения /Под ред. Н. В. Лазарева и И. Д. Гадаскиной. – Л.: Химия, 1977. – С. 235-275. 4. Шафран Л. М., Леонова Д. И., Пресняк И. С. и др. Токсикология горения в проблеме химической безопасности производства и окружающей среды // 3-й Съезд токсикологов России: Тезисы докладов (Москва, 2-5 декабря 2008).- М., 2008. - С.340-342 5.Межрегиональная благотворительная общественная организация «Ассоциация клинических токсикологов». [Электронный ресурс]. https://mzdrav.rk.gov.ru/ru/index URL:https://mzdrav.rk.gov.ru/file/Toksicheskoe_dejstvie_okisi_ugleroda_18042014_Klinicheskie_rekomendacii.pdf 6. Отравление монооксидом углерода (угарным газом) / Под ред. Ю. В. Зобнина / Зобнин Ю. В., Савватеева-Любимова Т. Н., Коваленко А. Н., Петров А. Ю., Васильев С. А., Батоцыренов Б. В., Романцов М. Г. – СПб.: Издательство «Тактик-Студио», 2011. – 80 с. 7.Метглобинообразователи. [Электронный ресурс]. https://studfile.net/ URL: https://studfile.net/preview/3591581/page:3/
|
||||||
|
Последнее изменение этой страницы: 2021-02-07; просмотров: 250; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.15.1 (0.005 с.) |