
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Исследования с целенаправленным изучением уровня концентрации препарата в плазме крови
До настоящего времени наиболее валидными экспериментами по выявлению взаимосвязи уровня концентрации препарата и клинической реакцией считались исследования, использующие назначение фиксированных дозировок препарата и последующую ретроспективную оценку полученных соотношений. В ходе многих из этих исследований не было выявлено достаточного числа больных, не проявляющих клинической реакции при высоких уровнях концентрации препарата. Кроме того, клинические и лабораторные данные анализировались после завершения эксперимента и, следовательно, мы не знаем, могла ли возникнуть клиническая реакция у больных при последующем снижении уровня концентрации препарата в крови. Более целесообразно планировать исследования таким образом, чтобы уровень концентрации препарата являлся непосредственным первичным материалом эксперимента. Существует также ряд проблем со статистическим анализом. В этом смысле валидность оценки повышается соответственно размерам выборки (суммарно в нескольких исследованиях), что позволяет статистически более объективно определить граничные значения терапевтического окна и обеспечить в последующем целенаправленное исследование уровня концентрации препарата. В процессе исследования Volavka и др. 111 больных шизофренией и шизоаффективным расстройством были рандомизировано распределены на три группы, в которых терапия осуществлялась в течение шести недель при уровнях концентрации галоперидола 2-13,13,1-24 и 24,1-35 нг/мл [35]. Больным, у которых клиническая реакция не возникала, лечение назначалось еще на 6 недель с другим уровнем концентрации препарата. Тем не менее интерпретация полученных результатов затруднена в связи с продолжительностью периода, необходимого для постепенного повышения концентрации до среднего или высокого уровня. В последующей работе Volavka и др. проводили лечение больных с острой психотической симптоматикой на низком (в среднем 2,2 нг/мл) или среднем (10,5 нг/мл) уровне концентрации галоперидола. За 3 недели лечения у 25 больных с уровнем концентрации препарата в плазме крови ниже 3 нг/мл возникала минимальная клиническая реакция. У больных со средней концентрацией последующее снижение ее уровня привело к улучшению вторичной, связанной с лекарствами негативной симптоматики [36].
Взаимоотношение между уровнем концентрации галоперидола и реакцией на терапию изучалось еще во время нескольких исследований. В связи с методологическими проблемами результаты этих исследований значительно отличались. Кроме того, в работах с фиксированной дозировкой у больных без терапевтической реакции и с уровнем концентрации препарата, ниже или выше границ предполагаемого терапевтического диапазона не проводились изменения дозировки. Такое изменение с приведением уровня концентрации в соответствие с серединой предполагаемого терапевтического диапазона позволило бы на практике проверить предположение о том, что в результате должна улучшаться клиническая реакция.
Рис. 5.13. Клиническая реакция, полученная на основе предписанного уровня концентрации препарата в фазе Б исследования. (Воспроизведена с разрешения Janicak et al. Acta Psychiatr Scand 1997) Размер анализируемой в фазе Б выборки, состоящей из больных, не имевших терапевтической реакции в фазе А, был незначителен. Но у тех больных, у которых уровень концентрации препарата после его изменения оказался в среднем диапазоне, степень клинического улучшения была намного выше, чем у больных, у которых уровень концентрации препарата оставался в низком или высоком диапазоне. Одной из задач нашего исследования была разработка формулы предсказания дозы для более быстрого достижения желаемого уровня устойчивой концентрации галоперидола. "Тестовые дозы" в 15 мг галоперидола перед началом исследования с достижением целевых уровней концентрации позволили разработать и проверить эту формулу, в основе которой лежит линейная регрессионная модель [38, 39].
Наши данные, полученные в фазе А, соответствуют данным McEvoy и коллег о пороговой дозировке нейролептиков [40]. Они определили нейролептический порог (НП) при наблюдении 106 больных шизофренией и ши-зоаффективным расстройством, равным 3,7± ±2,3 мг/сут). Наши результаты, полученные в фазе А, совпали с этими данными (терапевтическая реакция не вызывалась при уровне концентрации ниже 2 нг/мл, что соответствует суточной дозировке галоперидола приблизительно 3,3 мг). После двух недель первичного лечения McEvoy рандомизировано назначал еще на 2 недели галоперидол или в прежней дозировке (НП), или переходил на более высокие дозировки (в среднем 11,6±4,7 мг/сут). В аналогичной фазе Б наши результаты показали большую степень улучшения, чем у McEvoy и др. (соответственно 8,1 и 2,9 единиц по шкале BPRS). Результаты наших исследований также дополняют ряд исследований с применением позитрон-эмиссионной томографии (Nordstrom и др., Nyberg и др.) по определению оптимальной степени связывания D2 рецепторов в системе стриа-тум [41,42]. Так, связывание менее 60% D2 рецепторов является недостаточным, а более 80% может вести к повышению риска экстрапирамидной симптоматики. Wolkin и др. обнаружили, что уровень концентрации галоперидола в 5-15 нг/мл ведет к ускоренной блокаде D2 рецепторов вплоть до 80% [43]. Позднее Kapur и др. сообщили, что назначение галоперидола в дозировке 2 мг/сут на 2 недели у 7 больных с острым психотическим состоянием вызывало связывание D2 рецепторов на 66% (±7%) [44]. У этих первичных больных уровень концентрации составил 0,6-1,5 нг/мл. При этом уровне у пяти больных улучшение по шкале CGI составило 45% для продуктивных и 55% для негативных симптомов. Ни в одном исследовании не было показано, что более высокие уровни концентрации препарата отличаются большей эффективностью (в некоторых работах обнаруживают скорее падение эффективности, в других отмечают формирование плато при повышении концентрации). Кроме того, излишнее повышение уровня концентрации ведет к увеличению риска осложнений. Имеются, например, публикации, доказывающие, что быстрое наращивание дозировки предрасполагает к развитию ней-ролептического злокачественного синдрома [45,46]. Мы хотели бы акцентировать внимание на вытекающем из этих работ общем выводе о том, что высокие дозировки нейролептиков или высокий уровень концентрации препарата не имеет никаких преимуществ перед стандартными назначениями. После сорокалетнего использования типичных нейролептиков мы только сейчас начинаем определять точные взаимоотношения между клинической реакцией и дозировкой или уровнем концентрации препарата. В отношении новых препаратов мы должны обладать подобной информацией заранее, чтобы избежать использования чрезмерных дозировок. Эта информация может иметь важное значение также для планирования клинических испытаний новых препаратов, позволяя определять адекватные клинические дозировки при использовании в качестве контроля традиционных нейролептиков (так назывемые параллельные исследования дозы-реакции).
Клинический пример: Женщина, 29 лет, с диагнозом "шизоаффективное расстройство" в состоянии обострения была принята в нашу исследовательскую клинику. После предоставления информированного согласия больная была включена в исследование по целенаправленному изучению уровня концентрации галопери-дола в крови. По принципу случайной выборки она была распределена в группу больных с высоким уровнем концентрации препарата в крови и в течение трех недель получала 60 мг/сут галоперидола. Перед началом исследования ее состояние по шкале BPRS составило 40 единиц. После первичного лечения уровень концентрации препарата в крови у нее достиг 38,4 нг/мл, а оценка по BPRS составляла 39 единиц. Затем она была переведена в группу со средним уровнем концентрации и получала 16 мг/сут галоперидола. Спустя 24 дня при уровне концентрации галоперидола в плазме крови 14,2 нг/мл ее состояние оценивалось в 22 единицы по BPRS. Таким образом, лечение в первой фазе не вызвало улучшения состояния, а во второй привело к 45%-му улучшению по шкале BPRS. При этом, если учитывать, что наименьшая оценка по BPRS составляет 18 единиц, улучшение составило 82% от подлежащих измерению показателей. Клинический пример: Больной шизофренией 29-летнего возраста был госпитализирован в нашу исследовательскую клинику в связи с усилением параноидной и галлюцинаторной симптоматики. После предоставления информированного согласия и 12-дневного периода вымывания состояние больного было оценено по шкале BPRS в 48 единиц. Он был распределен в группу больных с запланированным низким уровнем концентрации препарата. После трех недель назначения галоперидола по 2 мг/сут уровень концентрации препарата в крови больного составил 1,29 нг/мл, а клиническое состояние оценивалось в 37 единиц по BPRS (23% изменения). Затем он был переведен в группу со средним уровнем концентрации препарата и дозировка галоперидола была увеличена до 18 мг/сут. После 27 дней дополнительного лечения уровень концентрации препарата составил 12,0 нг/мл, а оценка по шкале BPRS — 21 (55% улучшения по сравнению с начальной оценкой). Если опять считать 18 единиц наименьшей возможной оценки, то улучшение составило 84% от возможного изменения показателей.
Психотическая симптоматика клинически и статистически значительно уменьшилась после того, как у обоих больных уровень концентрации галоперидола был приведен к диапазо-^'10-1^иуШ. С^естйует вероятность того, что их состояние улучшилось просто в связи с длительностью лечения, однако резкое улучшение стандартизованной оценки их клинического состояния совпало именно с переходом на вторую фазу эксперимента. Оценка побочных эффектов по шкале Simp-son-Angus выразилась в средних величинах и не изменялась в течение всего эксперимента. Таким образом, это не подтверждает представлений о том, что снижение токсического влияния препарата ведет к клиническому улучшению. Клозапин Последние сообщения указывают, что для максимально эффективного лечения клозапином больных с явлениями терапевтической резис-тентности необходим уровень концентрации препарата в плазме крови от 350 до 450 нг/мл [14,47-49]. ЗАКЛЮЧЕНИЕ В заключение необходимо отметить, что роль мониторинга уровня концентрации препарата в плазме крови все еще остается очень неопределенной. Тем не менее лекарственный мониторинг может быть полезен в следующих ситуациях: • Для определения правильности выполнения больным терапевтического режима. • Для установления адекватности назначений у больных с устойчивостью к терапии. • Для предотвращения токсического действия излишне высокого уровня концентрации препарата в плазме крови. • Для наблюдения за состоянием больных с сопутствующими соматическими заболеваниями или с дополнительными психотроп-ными или другими лекарственными назначениями. • Для получения максимальной клинической реакции в тех случаях, когда связь между уровнем концентрации препарата и клинической реакцией четко установлена. • Для получения данных, которые могут быть использованы с целью установить взаимоотношения между дозировкой препарата и клинической реакцией на него. • Для подстраховки врача в потенциально сложных медико-правовых ситуациях. литература 1. Wode-Helgodt В, Borg S, Fyro В, Sedvall G. Clinical effects and drug concentrations in plasma and cerebrospinal fluid in psychotic patients treated with fixed doses of chlorpromazine. Acta Psychiatr Scand 1978; 58:149-173- 2. Chang SS, Javaid JI, Dysken MW, Casper RC, Jani-cak PG, Davis JM. Plasma levels of fluphenazine during fluphenazine decanoate treatment in schizophrenia. Psychopharmacology 1985; 87: 55-58. 3. Dysken MW, Javaid JI, Chang SS, Schaffer C, Sha-hid A, Davis JM. Fluphenazine pharmacokine-tics and therapeutic response. Psychopharmacology 1981; 73: 205-210. 4. Janicak PC. Javaid JI, Sharma RP, ComatyJE, Pe-terson J, Davis JM. Trifluoperazine plasma levels and clinical response. J Clin Psychopharmacol 1989; 9 (5): 340-346. 5. Mavroidis ML, Kanter DR, Hirschowitz J, Carver DL Clinical relevance of thiothixene plasma levels. J Clin Psychopharmacol 1984; 4 (3): 155-157. 6. Smith RC, Baumgartner R, Misra CH, et al. Halo-peridol. Plasma levels and prolactin response as predictors of clinical improvement in schizophrenia. Chemical versus radioreceptor plasma level assays. Arch Gen Psychiatry 1984; 41:1044-1049, 7. Garver DL, Hirschowitz J, Glicksteen GA, Kanter DR, Mavroidis ML. Haloperidol plasma and red blood cell levels and clinical antipsychotic response. J Clin Psychopharmacol 1984; 4: 133-137. 8. Mavroidis ML, Garver L Plasma haloperidol levels and clinical response: confounding variables. Psychopharmacol Bull 1985; 21: 62-65. 9. Potkin SG, Shen Y, Zhou D, Pardes H, Shu L, Phelps B, Poland R. Does a therapeutic window for plasma haloperidol exist? Preliminary Chinese data. Psychopharmacol Bull 1985; 21 (1): 59-61.
10. Van Putten T, Marder SR, May PRA, Poland RE, O'Brien RP. Plasma levels of haloperidol and clinical response. Psychopharmacol Bull 1985; 21: 69-72. 11. Van Putten T, Marder SR, Mintz J, Poland RE. Haloperidol plasma levels and clinical response: a therapeutic window relationship. Psychopharmacol Bull 1988; 24: 172-175. 12. Davis JM, Ericksen SE, Hurt S, Chang SS, Javaid JI, Dekirmenjian H, Casper R. Haloperidol plasma levels and clinical response: basic concepts and clinical data. Psychopharmacol Bull 1985; 21: 48-51. 13. Santos JL, Cabranes JA, Vasquez FF, Almoguera I, Ramos JA. Clinical response and plasma haloperidol levels in chronic and subchronic schizophrenia. Biol Psychiatry 1989; 26: 381-388. 14. Perry PJ, Miller DD, Arndt SV, Cadoret RJ. Cloza-pine and norclozapine plasma concentrations and clinical response of treatment refractory schizophrenia. Am J Psychiatry 1991; 148:231-235. 15. Marder S, Davis JM, Janicak PG, eds. Clinical use of neuroleptic plasma levels. Washington, DC: American Psychiatric Press, Inc, 1993; 137-142. 16. Curry SH. Determination of nanogram quantities of chlorpromazine or its metabolites in plasma using gas liquid chromatography with an electron capture detector. Anal Chem 1968; 40: 1251-1255. 17. Curry SH, Marshall JHL, Davis JM, Janowsky DS. Chlorpromazine plasma levels and effects. Arch Gen Psychiatry 1970; 22: 289-296. 18. May PRA, Van Putten T, Jenden DJ, Yale C, Dixon WJ. Chlor-promazine levels and the outcome of treatment in schizophrenic patients. Arch Gen Psychiatry 1981; 38: 202-207. 19. Van Putten T, Aravagiri M, Marder SR, Wirshing WC, Mintz J, Chabert N. Plasma fluphenazine levels and clinical response in newly admitted schizophrenic patients. Psychopharmacol Bull 1991; 27 (2): 91-96. 20. Marder SR, Van Putten T, Aravagiri M, et al. Fluphenazine plasma levels and clinical response. Psychopharmacol Bull 1990; 26: 256-259. 21. Yesavage JA, Holman CA, Cohn R, Lombrozo L Correlation of initial serum levels and clinical response. Arch Gen Psychiatry 1983; 40:301-304. 22. Janicak PG, Javaid JI, Davis JM. Neuroleptic plasma levels: methodological issues, study design, and clinical applicability. In: Marder SR, Davis JM, Janicak PG, eds. Clinical use of neuroleptic plasma levels. Washington, DC: APPI Press, 1993:17-44. 23. Smith RC. Plasma haloperidol levels and clinical response. Arch Gen Psychiatry 1987; 44: 1110-1112. 24. Palao DJ, Arauxo A, Brunei M, et al. Haloperidol: therapeutic window in schizophrenia. J Clin Psy-chopharmacology 1994; 14: 303-310. 25. Magliozzi JR, Hollister LE, Arnold KV, Earle GM. Relationship of serum haloperidol levels to clinical response in schizophrenic patients. Am J Psychiatry 1981; 138 (3): 365-367. 26. Bleeker JAC, Dingemans PM, Frohne-de Winter ML, van der Slooten EPJ. Plasma level and effect of low dose haloperidol in acute psychosis. Psychopharmacol Bull 1984; 20 (2): 317-319- 27. Shostak M, Perel JM, Steller RL, et al. Plasma haloperidol and clinical response: a role for reduced haloperidol in antipsychotic activity. J Clin Psychopharmacol 1987; 7: 394-400. 28. Doddi S, Rifkin A, Karajgi B, Cooper T, Borenstein M. Blood levels of haloperidol and clinical outcome in schizophrenia. J Clin Psychopharmacol 1994; 14 (3): 187-195. 29. Kirch GG, Bigelow LB, Korpi ER, Wagner RL, Zalc-man S, Wyatt RJ. Serum haloperidol concentration and clinical response in schizophrenia. Schizophrenia Bull 1988; 14 (2): 283-289. 30. Bigelow L, Kirch DG, Braun T, et al. Absence of relationship of serum haloperidol concentration and clinical response in chronic schizophrenics: a fixed-dose study. Psychopharmacol Bull 1985; 21 (1): 66-68. 31. Rimon R, Averbuch I, Rozick P, et al. Serum and CSF levels of haloperidol by radioirnmunoassay and radioreceptor assay during high-dose therapy of resistant schizophrenic patients. Psycho-pharmacology 1981; 73:197-199. 32. Coryell W, Kelly M, Perry P, Miller DD. Haloperidol plasma levels and acute clinical change in schizophrenia. J Clin Psychoparmacol 1990; 10 (6): 397-402. 33. Volavka J, Cooper ТВ. Review of haloperidol level and clinical response: looking through the window. J Clin Psychopharmacol 1987; 7:25-30. 34. Perry PJ, Pfohl BM, Kelly MW. The relationship of haloperidol concentrations to therapeutic response. J Clin Psychopharmacol 1988; 8: 38-43. 35. Volavka J, Cooper T, Czobor P, et al. Haloperidol blood levels and clinical effects. Arch Gen Psychiatry 1992; 49: 354-361. 36. Volavka J, Cooper ТВ, Czobor P, Meisner M. Plasma haloperidol levels and clinical effects in schi-zoprenia and schizoaffective disorder. Arch Gen Psychiatry 1995; 52: 837-845. 37. Janicak PG, Javaid JI, Sharma RP, et al. A two-phase, double-blind randomized study of three haloperidol blood levels for acute psychosis with reassignment of initial non-responders. Acta Psy-chiatrica Scand 1997; 95: 343-350. 38. Javaid JI, Janicak PG, Hedeker D, Sharma RP, Da-vis JM. Steady-state plasma level prediction for haloperidol from a single test dose. Psychopharmacol Bull 1991; 27 (1): 83-88. 39. Javaid JI, Janicak PG, Sharma RP, Leach A, Davis JM, Wang Z. Prediction of haloperidol steady-state levels in plasma after a single test dose. J Clin Psychopharmacology 1996; 16:45-50. 40. McEvoy JP, Hogarty GE, Steingard S. Optimal dose of neuroleptic in acute schizophrenia. A controlled study of the neuroleptic threshold and higher haloperidol dose. Arch Gen Psychiatry 1991; 48: 739-745. 41. Nordstrom Α-L, Farde L, Halldin С. High 5-HT2 receptor occupancy in clozapine treated patients demonstrated by PET. Psychopharmacology 1993; 110:365-367. 42. Nyberg S, Farde L, Eriksson L, Halldin C, Eriksson B. 5-HT2 and D2 dopamine receptor occupancy in the living human brain. A PET study with risperi-done. Psychopharmacology 1993; 110:265-272. 43. Wolkin A, Brodie JD, Barouche F, et al. Dopamine receptor occupancy and haloperidol plasma levels [Letter]. Arch Gen Psychiary 1989; 46:482-483. 44. Kapur S, Remington G, Jones C, et al. What is the lowest effective dose of haloperidol? Evidence from PET Studies. Biol Psychiatry 1996; 39: 513. 45. Ericksen SE, Hunt SW, Davis JM. Dosage of an-tipsychotic drugs [Letter]. New Engl J Med 1979; 294:1296-1297. 46. Keck PE, Harrison GP, Cohen BM, McElroy SL, Nierenberg AA. Risk factors for neuroleptic malignant syndrome. A case study. Arch Gen Psychiatry 1989; 46:914-918. 47. Potkin SG, Bera R, Gulasekaram B, et al. Plasma clozapine concentrations predict clinical response in treatment resistant schizophrenia. J Clin Psychiatry 1994; 55 [9, suppl B]: 117-121. 48. Miller DD, Fleming F, Holman TL, Perry PJ. Plasma clozapine concentrations as a predictor of clinical response: a follow-up study. J Clin Psychiatry 1994; 55 [9, suppl B]: 117-121. 49. Kronig MH, Munne RA, Szymanski S, et al. Plasma clozapine levels and clinical response for treatment refractory schizophrenic patients. Am J Psychiatry 1995; 152: 179-182.
|
|||||||||
|
Последнее изменение этой страницы: 2021-01-08; просмотров: 71; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.149.29.112 (0.054 с.) |
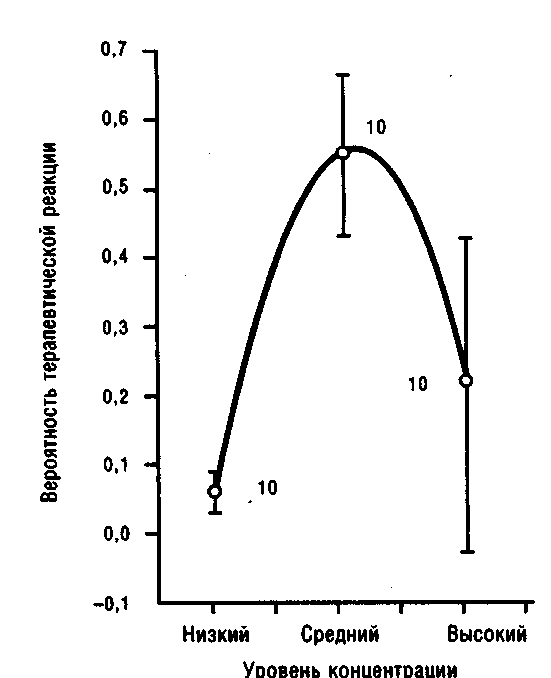 Мы попытались провести подобную проверку, изменяя назначения галоперидола у больных без начальной терапевтической реакции таким образом, чтобы его концентрация совпала с предполагаемым терапевтическим диапазоном (рис. 5.12) [37]. 25-30% наблюдаемых больных с уровнем концентрации галоперидола в низком, среднем и высоком диапазоне проявили терапевтическую реакцию в течение фазы А эксперимента. Далее, во второй фазе Б этого эксперимента мы попытались добиться положительной клинической реакции у больных с начальной частичной терапевтической реакцией или с ее отсутствием путем изменения дозировки в среднем на 25 мг/сут, тем самым приближаясь к уровню концентрации в 12 нг/мл (рис. 5.13).
Мы попытались провести подобную проверку, изменяя назначения галоперидола у больных без начальной терапевтической реакции таким образом, чтобы его концентрация совпала с предполагаемым терапевтическим диапазоном (рис. 5.12) [37]. 25-30% наблюдаемых больных с уровнем концентрации галоперидола в низком, среднем и высоком диапазоне проявили терапевтическую реакцию в течение фазы А эксперимента. Далее, во второй фазе Б этого эксперимента мы попытались добиться положительной клинической реакции у больных с начальной частичной терапевтической реакцией или с ее отсутствием путем изменения дозировки в среднем на 25 мг/сут, тем самым приближаясь к уровню концентрации в 12 нг/мл (рис. 5.13).


