Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
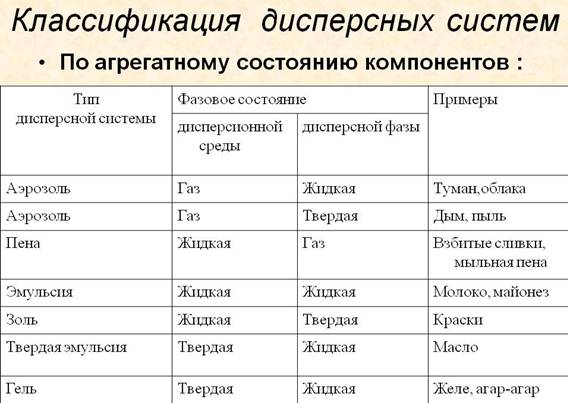
Предмет коллоидной химии. Признаки коллоидного состояния. Дисперсность и удельная поверхность. Классификации дисперсных систем.Стр 1 из 3Следующая ⇒
КОЛЛОК 1 КОЛЛДА Предмет коллоидной химии. Признаки коллоидного состояния. Дисперсность и удельная поверхность. Классификации дисперсных систем. Коллоидна химия - раздел физической химии, изучающий поверхностные явления и дисперсные физико-химические системы
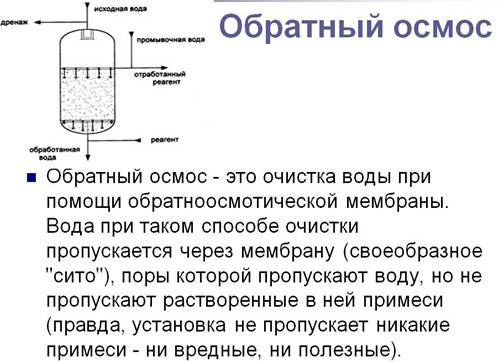
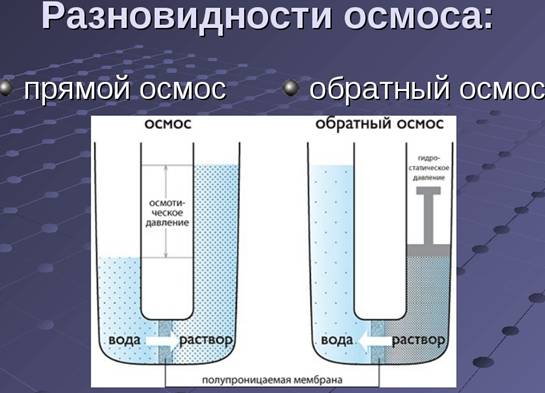
Методы получения дисперсных систем. Пептизация. Формула мицеллы гидрофобного золя. Мембранные процессы (осмос, обратный осмос, диализ, ультрафильтрация). Методы очистки коллоидных систем. Осмос – это односторонняя диффузия молекул растворителя через полупроницаемую мембрану при условии разности концентраций раствора по обе стороны мембраны. Механизм: При разделении двух растворов различной концентрации или раствора и чистого растворителя полупроницаемой перегородкой (мембраной) возникает поток растворителя от меньшей концентрации вещества к большей, что приводит к выравниванию концентраций. Возникновение потока обусловлено тем, что число ударов молекул растворителя о мембрану со стороны более разбавленного раствора (или чистого растворителя) будет больше, чем со стороны более концентрированного раствора. Это избыточное число ударов и является причиной перемещения растворителя через поры мембраны туда, где молекул меньше. Подобное объяснение является кинетической трактовкой причины осмоса.
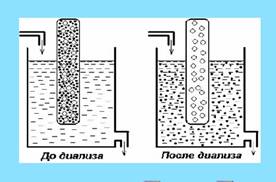
Диализ – процесс очистки коллоидных растворов от ионов и молекул низкомолекулярных примесей в результате их диффузии в чистый растворитель сквозь полупроницаемую мембрану.
Ультрафильтрация – диализ под давлением!
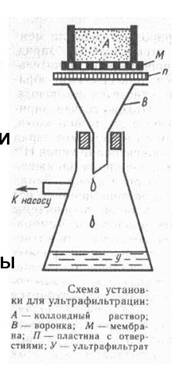
Ультрафильтрация – фильтрование коллоидного раствора через полупроницаемую мембрану, пропускающую дисперсную среду с низкомолекулярными примесями и задерживающую частицы дисперсной фазы или макромолекулы. Для ускорения этого процесса, его проводят при перепаде давления по обе стороны от мембраны: под разряжением снизу от мембраны (вакуум) и повышением давления сверху от мембраны.
Седиментация и центрифугирование. Дисперсионный анализ суспензий.
Метод седиментации применим только для агрегативно устойчивых суспензий, т.е. в условиях, исключающих агрегацию (коагуляцию) частиц. С этой целью используют достаточно разбавленные дисперсные системы (с концентрацией дисперсной фазы 0,5--1%), которые при необходимости могут быть стабилизированы с помощью поверхостноактивных веществ (ПАВ).
Оптические свойства коллоидных систем. Явление светорассеяния (закон Релея). Мутность. Нефелометрия. Турбидиметрия.
Правило Шульце-Гарди · Коагулирующим действием обладает один из ионов и это тот ион, заряд которого противоположен по знаку заряду коллоидной частицы · Коагулирующая способность электролита возрастает с увеличением знака заряда коагуляционного иона
ДЛФО описывает поведение лиофобных систем, механизм скрегативной устойчивости взаимодействия между частицами для устойчивости (С) и неустойчивости (r).
КОЛЛОК 1 КОЛЛДА Предмет коллоидной химии. Признаки коллоидного состояния. Дисперсность и удельная поверхность. Классификации дисперсных систем. Коллоидна химия - раздел физической химии, изучающий поверхностные явления и дисперсные физико-химические системы
|
|||||
|
Последнее изменение этой страницы: 2021-01-08; просмотров: 353; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.200.197 (0.005 с.) |