Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Предпочтительные приемы синтеза ⇐ ПредыдущаяСтр 3 из 3
• Высокая воспроизводимость свойств реагентов • Короткий путь от реагентов к конечному продукту (получение Al2O3 – Y3Al5O12 при приложении импульсов тока в 2000 А продолжительностью несколько миллисекунд) • Предотвращение кристаллизации промежуточных фаз (закалка расплава, замораживание раствора солей) • Контроль эволюции системы путем введения темплата в виде кристаллов-затравок или подложки для эпитаксиального роста пленок • Подавление хаоса с использованием петли обратной связи. А так же: Диссипативные структуры как материалы
-Клеточные структуры вибропрессованных порошков -Псевдомонокристаллы, выращенные из движущихся суспензий
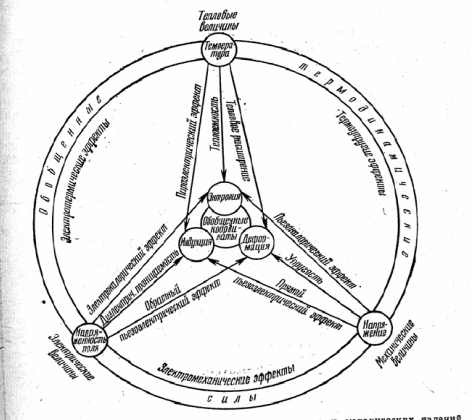
Схема взаимодействия тепловых, электрическихт и механических явлений в кристаллах
Из книги Ю.И.Сиротин, М.П.Шаскольская «Основы кристаллофизики». М.:Наука, 1979 Основные определения: • Эволюция – трансформация систем, связанная с их развитием во времени и пространстве • КСО (консервативная самоорганизация) – результат эволюции системы в направлении изменения энергии Гиббса, • ДСО (диссипативная самоорганизация) - результат эволюции системы в направлении изменения энтропии. • Равновесные структуры образуются при незначительном отклонении от равновесия, а диссипативные структуры образуются и сохраняются в сильно неравновесных условиях благодаря интенсивному обмену веществом и энергией с окружающей средой. • Геоэволюция и биоэволюция (переход от неживого к живому) – сложные процессы, включающие как КСО, так и ДСО (М.Лен), причем во времени доля КСО падает, а доля ДСО растет. Чем сложнее система, тем сильнее процессы обмена веществом и энергией, то есть скорость гео- и биоэволюции. •... Геомимикрия (гидротермальный синтез минералов (Александров) •... Биомимикрия (биокерамика) Современные биоматериалы Основная черта нового тысячелетия – возрастающий интерес к увеличению качества и продолжительности человеческой жизни. Достижение подобной цели предполагает, в частности, создание материалов для искусственных органов и тканей. За последние 30 лет использовано более 40 различных материалов (керамика, металлы, полимеры) для лечения, восстановления и замены более 40 различных частей человеческого тела, включая кожные покровы, мышечную ткань, кровеносные сосуды, нервные волокона, костную ткань. Разработка заменителей костной ткани знаменует, по словам проф. Л. Хенча, революционный этап в развитии человечества: “Тысячелетия тому назад открытие того, что огонь может превратить бесформенную глину в керамическую утварь, привело к возникновению земледельческой цивилизации и радикально улучшило качество и продолжительность жизни. Другая революция произошла уже в наши дни в
области использования керамики в медицинских целях. Это инновационное применение специально спроектированных керамических материалов для замены и лечения больных или поврежденных частей тела” [1]. Эту область современного материаловедения именуют (не вполне, впрочем, справедливо) биокерамикой, она охватывает материалы для эндопротезов в травматологии и ортопедии, пломбировочные материалы в стоматологии, имплантаты в челюстно-лицевой хирургии, медико-косметические средства. В настоящее время рынок биокерамики имеет емкость ∼2.3 млрд.$, прогнозируемый годовой прирост составляет 7-12 %, объемы требуемых материалов оцениваются на уровне десятков тонн [1,2]. Число больных, нуждающихся в операциях по восстановлению целостности кости, довольно велико: для США эта цифра составляет 1 млн. человек и более ежегодно (из них свыше 300 тыс. – протезирование тазобедренного и коленного суставов, такой же порядок имеют зубные имплантаты). Динамика продвижения идеи на рынок биоматериалов имеет ряд особенностей, связанных с прохождением длительных тестов и сертификаций, в силу этого обстоятельства лишь немногие из рассматриваемых ниже материалов могут считаться рекомендованными к применению. Текущее состояние рынка имплантатов может рассматриваться как ожидание массированного вторжения новых идей и материалов. Биокерамика должно обладать определенными химическими свойствами (отсутствие нежелательных химических реакций с тканями и межтканевыми жидкостями, отсутствие коррозии), механическими характеристиками (прочность, трещиностойкость, сопротивление замедленному разрушению,
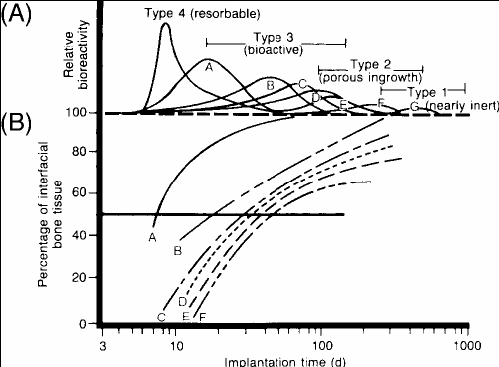
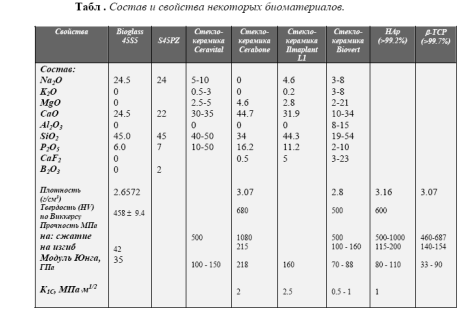
износостойкость), биологическими свойствами (отсутствие реакций со стороны имунной системы, срастание с костной тканью, стимулирование остеосинтеза). По характеру отклика организма на имплантат биоматериалы классифицируют следующим образом: 1) токсичные (если окружающие ткани отмирают при контакте) – большинство металлов; 2) биоинертные (нетоксичные, но биологически неактивные) - керамика на основе Al2O3, ZrO2; 3) биоактивные (нетоксичные, биологически активные, срастающиеся с костной тканью) - композиционные материалы типа биополимер/фосфат кальция, керамика на основе фосфатов кальция, биостекла. Основной недостаток биоинертной керамики – низкая долговечность вследствие экранирования механических нагрузок, приводящее к резорбции костной ткани, прилегающей к имплантату, и утрату последнего. Тем не менее, подобные материалы, по-видимому, не имеют пока альтернативы, как заменители тазобедренного сустава. К наиболее ярким представителям биоактивных материалов относятся биостекла (наиболее используется состав "45S5": 24.5 % Na2O, 24.5 % CaO, 45.0% SiO2, 6% P2O5; варьируя состав, можно изменять биоактивность стекол и их резорбируемость) и материалы на основе гидроксиапатита (ГАП) – Ca10(PO4)6(OH)2 (плотная и пористая керамика; ГАП-покрытия на металлических имплантатах; композиты ГАП–полимер, моделирующие, как, например, композит ГАП–коллаген, состав и структуру кости). К сожалению, невысокие механические характеристики подобных материалов не позволяют создавать крупные нагружаемые имплантаты. Перспективы в области разработки биоматериалов связаны с развитием всего спектра имеющейся на сегодня биокерамики. Особый интерес представляют исследования, исповедающие “регенерационный” подход [1], в котором акцент делается не на замещение дефекта имплантатом с подходящими механическими характеристиками, а на быструю биодеградацию материала и замену его костной тканью (т.е. на первое место у таких материалов выходят биологические свойства). Т.о. биоматериалы необходимы для лечения, восстановления и замены: • кожных покровов, мышечной ткани • кровеносных сосудов • нервных волокон • костной ткани – эндопротезы в травматологии и ортопедии – стоматология (пломбировочные материалы),челюстно-лицевая хирургия – медико-косметические средства (кремы, пасты) За последние 30 лет использовано более 40 различных материалов (керамика, металлы, полимеры) для замены более 40 различных частей человеческого тела. Требования, предъявляемые к биоматериалам:
• химические свойства – отсутствие нежелательных химических реакций с тканями и межтканевыми жидкостями – отсутствие коррозии, или растворение с контролируемой скоростью • механические свойства – прочность – трещиностойкость – сопротивление замедленному разрушению(усталости) – износостойкость • биологические свойства – отсутствие реакций со стороны иммунной системы (биосовместимость) – срастание с костной тканью – стимулирование остеосинтеза Отклик организма на имплантат Если материал токсичный – окружающие ткани отмирают биоинертный – образуется соединительная волокнистая ткань биоактивный – образуется костная ткань
биорезорбируемый – происходит замена материала костной тканью
Перспективны для применения в медицинских целях и углеродные материалы. Так, например, использование материалов на основе композитов туглеродных трубок с полимерами позволяет создавать биосовместимые имплантаты. Упругие модули углеродных материалов близки к костным, а в ходе in vitro тестов не наблюдается ухудшения прочностных свойств [2]. Другой перспективный "кандидат" на роль полного заменителя сустава - углеродный композит, армированный углеродными волокнами. Его механические свойства близки к характеристикам кости. В зависимости от микроструктуры материала, которая легко контролируется в широких пределах, получаю следующие значения энергии разрушения, упругих модулей, прочности на изгиб: 400-2900 Дж/м2, 10-72 ГПа, 100-450 МПа соответственно. Эти механические параметры соответствуют материалам с размерами дефектов в несколько сот мкм (например, пор диаметром до 120 мкм). Углеродные материалы биосовместимы, более того, можно легко контролировать их резорбируемость. На сегодняшний день углеродные композиты – наиболее вероятные материалы, которые прейдут на замену Тi протезам. Очень интересным и перспективным является так называемый "регенерационный подход". При этом используются различные материалы (биодеградируемые полимеры, биоактивные стекла, композиты HAp/CaSO4, Покрытие из НАр (b), на полимерных волокнах (a) в растворе-аналоге межтканевой жидкости костные клетки и протеины на носителях из HAp, CaSO4 и др.) для стимуляциии ускорения костной регенерации. Правда, данный подход применим лишь кзалечиванию малых дефектов.
|
|||||||
|
Последнее изменение этой страницы: 2020-11-28; просмотров: 168; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.109.102 (0.014 с.) |