Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема: « особенности биохимии и патологических процессов печени »Стр 1 из 12Следующая ⇒
Министерства здравоохранения российской федерации КАФЕДРА БИОЛОГИЧЕСКОЙ ХИМИИ
ОСОБЕННОСТИ БИОХИМИЧЕСКИХ И ПАТОЛОГИЧЕСКИХ ПРОЦЕССОВ ПЕЧЕНИ Учебное пособие
Владикавказ, 2017 ОСОБЕННОСТИ БИОХИМИЧЕСКИХ И ПАТОЛОГИЧЕСКИХ ПРОЦЕССОВ ПЕЧЕНИ: Учебное пособие /А.Е. Гурина, Л.Х. Дзоциева. – Владикавказ, 2017. – 95 с.
Авторы: А.Е.Гурина - к.м.н., доцент, зав. кафедрой биологической химии ФГБОУ ВО СОГМА Минздрава России; Л.Х.Дзоциева - к.м.н., ассистент кафедры биологической химии ФГБОУ ВО СОГМА Минздрава России. Рецензенты: А.Б.Иванов - д.б.н., профессор, зав. кафедрой нормальной и патологической физиологии медицинского факультета ФГБОУ ВО «Кабардино-Балкарский государственный университете им. Х.М.Бербекова» А.А.Байгильдина - д.м.н., профессор кафедры биологической химии ФГБОУ ВО «Башкирский государственный медицинский университет» Минздрава России.
В учебном пособии с современных позиций освещены основные разделы биохимии и патобиохимии печени: анатомо-функциональные особенности, методы биохимической диагностики, патобиохимические механизмы нарушения функции печени. Детально описаны синдромы печени и дифференциальная диагностика желтух. Для самостоятельной работы студентов и контроля знаний в пособии приводятся тестовые задания и ситуационные задачи, что облегчает усвоение программы дисциплины, обеспечивает систематизацию знаний и дает возможность оценить уровень самоподготовки. Пособие иллюстрировано оригинальными таблицами и схемами. Предназначено студентам, обучающимся в образовательных организациях высшего образования по специальностям «Лечебное дело», «Педиатрия», по дисциплине «Клиническая биохимия». СОДЕРЖАНИЕ
УСЛОВНЫЕ ОБОЗНАЧЕНИЯ
. ПРЕДИСЛОВИЕ В данном учебном пособии представлены современные данные об анатомо-биохимических особенностях печени, функциях и методах их оценки, патогенетические механизмы развития патологических процессов в печени, представлены алгоритмы биохимической диагностики основных синдромов. Пособие позволяет получить дополнительные знания по обмену билирубина и дифференциальной диагностики желтух, использовать их в клинической практике. В пособии излагаются основные алгоритмы биохимической диагностики различных расстройств с указанием нормативных показателей, которые могут быть учтены студентами при решении ситуационных задач. Для самоконтроля представлен комплект тестовых заданий и ситуационных задач.
Ситуационные задачи являются необходимым инструментом закрепления и систематизации знаний, развивают аналитическое и ассоциативное мышление. Некоторые из них базируются на конкретных клинических примерах, что приближает образовательный процесс к практической медицине. Пособие содержит наглядные материалы - таблицы, рисунки. Содержащаяся в таблицах и рисунках информация формирует целостное представление об этиологии и механизмах формирования и развития патологических реакций, процессов, компенсаторных явлениях, факторах декомпенсации и причинно-следственных связях в патологии. Данное пособие поможет обучающимся приобрести знания в понимании биохимических механизмов развития патологических процессов в печени и использовать их в клинической практике. Предназначено студентам медицинских вузов, обучающихся по специальности «Лечебное дело» и «Педиатрия» по дисциплине «Клиническая биохимия».
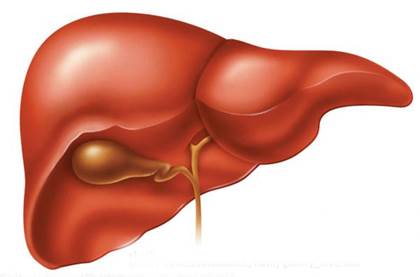
Строение печени. Печень - один из наиболее крупных и уникальных органов человечес-кого организма, выполняющий разнообразные функции, играющий важную роль в процессах пищеварения, обмена веществ, детоксикации. Масса печени взрослого человека составляет 1300-1800 г. Расположена печень в правом верхнем квадранте живота и прикрыта рёбрами. Анатомически в печени выделяют две доли - правую и левую. Правая доля почти в 6 раз крупнее левой; в ней выделяют два небольших сегмента: хвостатую долю на задней поверхности и квадратную долю на нижней поверхности. Правая и левая доли разделяются: спереди - складкой брюшины, так называемой серповидной связкой; сзади - бороздой, в которой проходит венозная связка, и снизу - бороздой, в которой находится круглая связка. Кровоснабжение печени осуществляется из двух источников: воротная вена несёт венозную кровь из кишечника и селезёнки, а печёночная артерия, отходящая от чревного ствола, обеспечивает поступление артериальной крови. Сосуды входят в печень через углубление, называемое воротами печени, которое располагается на нижней поверхности правой доли ближе к её заднему краю. Воротная вена и печёночная артерия в воротах печени дают ветви к правой и левой долям, а правый и левый желчные протоки соединяются и образуют общий желчный проток. Иннервация печени осуществляется волокнами седьмого - десятого грудных симпатических ганглиев, которые прерываются в синапсах чревного сплетения, а также волокнами правого и левого блуждающих и правого диафрагмального нервов.
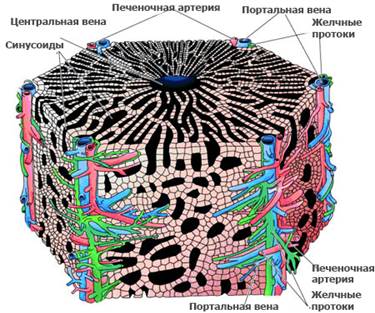
Структура печени. Структурной единицей печени является ацинус или печеночная долька. Она имеет пирамидальную форму, состоящую из центрально расположенной печёночной вены и периферически расположенных портальных трактов, содержащих жёлчный проток, ветви воротной вены и печёночной артерии. Между этими двумя системами располагаются балки гепатоцитов и содержащие кровь синусоиды. Ткань печени представлена двумя системами каналов - портальными трактами и печёночными центральными каналами, которые расположены таким образом, что не касаются друг друга; расстояние между ними составляет 0,5 мм. Эти системы каналов расположены перпендикулярно друг другу. Кровь из терминальных ветвей воротной вены попадает в синусоиды; при этом направление кровотока определяется более высоким давлением в воротной вене по сравнению с центральной.
Рис.1 Строение печеночной дольки (источник life4well.ru)
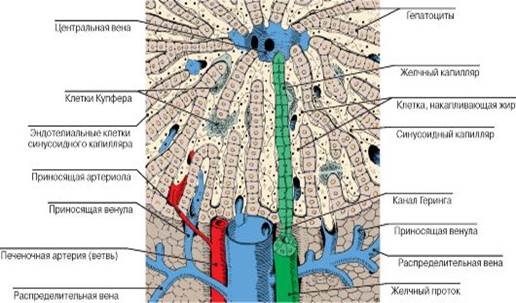
Центральные печёночные каналы окружены пограничной пластинкой печёночных клеток. Портальные тракты содержат терминальные ветви воротной вены, печёночную артериолу и жёлчный проток с небольшим количеством круглых клеток и соединительной ткани. Они окружены пограничной пластинкой печёночных клеток. Различают ряд функциональных зон ацинусов, в центре каждого из которых лежит портальная триада с терминальными ветвями портальной вены, печёночной артерии и жёлчного протока - зона 1. Ацинусы расположены в основном перпендикулярно по отношению к терминальным печёночным венам соседних ацинусов. Периферические, хуже кровоснабжаемые отделы ацинусов, прилежащие к терминальным печёночным венам (зона 3), наиболее страдают от повреждения (вирусного, токсического или аноксического). Зоны, расположенные ближе к оси, образованные приносящими сосудами и жёлчными протоками более жизнеспособны, и позднее в них может начаться регенерация печёночных клеток Гепатоциты - клетки печени, составляют около 60% массы печени. Они имеют полигональную форму и диаметр, равный приблизительно 30 мкм. Гепатоцит граничит с синусоидом и пространством Диссе, с жёлчным канальцем и соседними гепатоцитами. Базальной мембраны у гепатоцитов нет. Синусоиды выстланы эндотелиальными клетками. К синусоидам относятся фагоцитирующие клетки ретикулоэндотелиальной системы (клетки Купфера), звёздчатые клетки, также называемые жирозапасающими, клетками Ито или липоцитами. Тканевое пространство между гепатоцитами и синусоидальными эндотелиальными клеткаминазываетсяпространством Диссе. В перисинусоидальной соединительной ткани проходят лимфатические сосуды, которые на всём протяжении выстланы эндотелием. Тканевая жидкость просачивается через эндотелий в лимфатические сосуды. Ветви печёночной артериолы образуют сплетение вокруг жёлчных протоков и впадают в синусоидальную сеть на различных её уровнях. Они снабжают кровью структуры, расположенные в портальных трактах. Прямых анастомозов между печёночной артерией и воротной веной нет. С жёлчных канальцев начинается экскреторная система печени. Плазматическая мембрана пронизана микрофиламентами, образующими поддерживающий цитоскелет. Поверхность канальцев отделена от остальной межклеточной поверхности соединительными комплексами, состоящими из плотных контактов, щелевых контактов и десмосом. Внутридольковая сеть канальцев дренируется в тонкостенные терминальные жёлчные протоки или дуктулы (холангиолы, канальцы Геринга), они заканчиваются в более крупных (междольковых) жёлчных протоках, расположенных в портальных трактах. Последние разделяются на мелкие (диаметром менее 100 мкм), средние (±100 мкм) и крупные (более 100 мкм).
Рис. 2 Строение желчных протоков (источник myslide.ru)
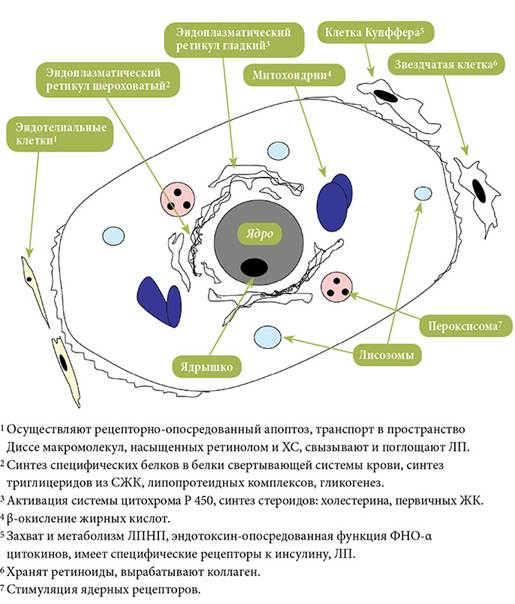
Рис.3 Структура гепатоцита (источник umedp.ru)
Купферовские клетки печени - это очень подвижные макрофаги, связанные с эндотелием, которые окрашиваются пероксидазой и имеют ядерную оболочку. Они фагоцитируют крупные частицы и содержат вакуоли и лизосомы. Эти клетки образуются из моноцитов крови и имеют лишь ограниченную способность к делению. Они фагоцитируют по механизму эндоцитоза (пиноцитоза или фагоцитоза), который может опосредоваться рецепторами (абсорбционный) или происходить без участия рецепторов (жидкофазный). Функциональные особенности клеток Купфера: 1. поглощают состарившиеся клетки, инородные частицы, опухолевые клетки, бактерии, дрожжи, вирусы и паразитов; 2. захватывают и перерабатывают окисленные липопротеины низкой плотности (которые считаются атерогенными) и удаляют денатурированные белки и фибрин при диссеминированном внутрисосудистом свёртывании крови; 3. содержат специфические мембранные рецепторы для лигандов, включая фрагмент Fc иммуноглобулина и компонент С3 комплемента, которые играют важную роль в представлении антигена; 4. активируются при генерализованных инфекциях или травмах. Они специфически поглощают эндотоксин и в ответ вырабатывают ряд факторов, например фактор некроза опухоли, интерлейкины, коллагеназу и лизосомальные гидролазы. Токсическое действие эндотоксина, таким образом, обусловлено продуктами секреции клеток Купфера, поскольку сам по себе он нетоксичен; 5. секретируют также метаболиты арахидоновой кислоты, в том числе простагландины; 6. имеют специфические мембранные рецепторы к инсулину, глюкагону и липопротеинам. Углеводный рецептор N-ацетилгликозамина, маннозы и галактозы может служить посредником в пиноцитозе некоторых гликопротеинов, особенно лизосомальных гидролаз. Кроме того, он опосредует поглощение иммунных комплексов, содержащих IgM; 7. выполняют эритробластоидную функцию в печени плода. Распознавание и скорость эндоцитоза клетками Купфера зависят от опсонинов, фибронектина плазмы, иммуноглобулинов. Эндотелиальные клетки - клетки образуют стенку синусоидов. Фенестрированные участки эндотелиальных клеток (фенестры) имеют диаметр 0,1 мкм и образуют ситовидные пластинки, которые служат биологическим фильтром между синусоидальной кровью и плазмой, заполняющей пространство Диссе. Эндотелиальные клетки имеют подвижный цитоскелет, который поддерживает и регулирует их размеры. Эти «печёночные сита» фильтруют макромолекулы различного размера. Через них не проходят крупные, насыщенные триглицеридами хиломикроны, а более мелкие, бедные триглицеридами, но насыщенные холестерином и ретинолом остатки могут проникать в пространство Диссе. Синусоидальные эндотелиальные клетки активно удаляют из кровообращения макромолекулы и мелкие частицы с помощью рецепторно-опосредованного эндоцитоза. Они несут поверхностные рецепторы к гиалуроновой кислоте (главный полисахаридный компонент соединительной ткани), хондроитинсульфату и гликопротеину, содержащему на конце маннозу, а также рецепторы типа II и III к фрагментам Fc IgG и рецептор к белку, связывающему липополисахариды. Эндотелиальные клетки выполняют очистительную функцию, удаляя ферменты, повреждающие ткани, и патогенные факторы (в том числе микроорганизмы). Кроме того, они очищают кровь от разрушенного коллагена и связывают и поглощают липопротеины.
Клетки Ито расположены в субэндотелиальном пространстве Диссе. Они содержат длинные выросты цитоплазмы, некоторые из которых тесно контактируют с паренхиматозными клетками, а другие достигают нескольких синусоидов, где могут участвовать в регуляции кровотока и влияющие на портальную гипертензию. В нормальной печени эти клетки являются местом хранения ретиноидов. Они содержат актин и миозин и сокращаются при воздействии эндотелина-1. При повреждении гепатоцитов звёздчатые клетки утрачивают жировые капли, пролиферируют, мигрируют в зону 3, приобретают фенотип, напоминающий фенотип миофибробластов, и вырабатывают коллаген типа I, III и IV, а также ламинин. Кроме того, они выделяют протеиназы клеточного матрикса и их ингибиторы, например тканевый ингибитор металлопротеина. Коллагенизация пространства Диссе приводит к снижению поступления в гепатоцит субстратов, связанных с белком. Естественные киллеры или ямочные клетки - это лимфоциты, прикреплённые к обращённой в просвет синусоида поверхности эндотелия. Их псевдоподии проникают сквозь эндотелиальную выстилку, соединяясь с микроворсинками паренхиматозных клеток в пространстве Диссе. Эти клетки живут недолго и обновляются за счёт лимфоцитов циркулирующей крови, дифференцирующихся в синусоидах. Ямочные клетки обладают спонтанной цитотоксичностью по отношению к опухолевым и инфицированным вирусом гепатоцитам.
Ферменты печени Наиболее часто в качестве объекта для исследования используют сыворотку крови, ферментный состав которой относительно постоянен. Нормальная активность ферментов в сыворотке крови отражает соотношение между биосинтезом и высвобождением ферментов (при обычном обновлении клеток), а также их клиренсом из кровотока. Повышение скорости обновления ферментов, повреждения клеток обычно приводят к повышению активности ферментов в сыворотке крови. По активности сывороточных ферментов печени можно установить вариант поражения печени (паренхиматозный или холестатический). Локализация ферментных систем в печени следующее: Цитоплазма клетки содержит следующий ряд ферментов: 1. аланинаминотрансферазу (АлАТ), 2. часть аспартатаминотрансферазы (АсАТ), 3. лактатдегидрогеназу (ЛДГ), 4. часть гамма-глутамилтранспептидазы (ГГТП) 5. другие ферменты. Митохондриальная фракция, в ней сосредоточены: 1. большая часть АсАТ (около 70%), 2. глутаматдегидрогеназа (ГлДГ), 3. алкогольдегидрогеназа и много других. Шероховатый эндоплазматическая ретикулум содержит холинэстеразу (ХЭ) и др.
В гладком эндоплазматическом ретикулуме находятся: 1. глюкозо-6-фосфатаза, 2. УДФ-глюкуронилтрансфераза, 3. гемсодержащий мембраносвязанный цитохром Р-450 и др.
Лизосомы содержат кислые гидролазы (кислая фосфатаза, рибонуклеаза и др.), которые активируются при снижении рН клетки. Билиарный полюс содержит мембранозависимые ферменты, такие как щелочная фосфатаза (ЩФ), 5-нуклеотидаза, часть ГГТП, лейцинаминопептидаза (ЛАП). Распределение ферментов внутри клетки объясняет неодинаковое повышение активности ферментов при различных патологических процессах. Например, при поражении центральных отделов долек (острый алкогольный гепатит, острый венозный застой и др.), повышается активность митохондриальной глутаматдегидрогеназы, как следствие недостатка кислорода и повреждение митохондрий, а при поражении портальных трактов (острый вирусный гепатит, хронический активный гепатит - ХАГ), повышается активность цитоплазматических трансаминаз. Функции клеток, расположенных в периферической зоне кровообращения ацинуса, примыкающей к терминальным печёночным венам (зона 3), отличаются от функции клеток, примыкающих к терминальным печёночным артериям и портальным венам (зона 1). Очевидно, что эти зоны различаются по снабжению кислородом: клетки зоны 3 получают кислород в последнюю очередь и особенно склонны к аноксическому повреждению. Ферменты цитохрома Р 450, участвующие в метаболизме лекарств, в основном сосредоточены в зоне 3. Наиболее высокие концентрации токсичных продуктов метаболизма лекарств обнаруживаются в гепатоцитах зоны 3. Кроме того, в них снижена концентрация глутатиона, поэтому гепатоциты зоны 3 оказываются особенно восприимчивыми к лекарственным повреждениям печени. Таблица 1. Метаболизм гепатоцитов в зависимости от их расположения в зоне 3 (центральной) или в зоне 1 (перипортальной) (по Шерлок Ш., Дули Дж).
Гепатоциты зоны 1 получают кровь с более высокой концентрацией желчных кислот и поэтому играют особенно важную роль в образовании желчи, зависящем от желчных кислот. Гепатоциты зоны 3 участвуют в образовании желчи, не зависящем от желчных кислот. Причины метаболических различий между зонами различны. Одни функции (глюконеогенез, гликолиз, кетогенез) зависят от направления движения крови по синусоидам, другие (осуществляемые цитохромом Р 450) - от скорости транскрипции генов, которая неодинакова в перивенулярных и перипортальных гепатоцитах. Например, при алкогольном поражении, может нарушаться микроциркуляция печени из-за коллагенизации пространства Диссе, образования базальной мембраны под эндотелием и изменения его фенестрированности. Все эти процессы наиболее выражены в зоне 3. Они приводят к потере питательных веществ, предназначенных для гепатоцитов, и к развитию портальной гипертензии. При патологических процессах в печени обнаруживается лимфоцитарная инфильтрация. Рецепторы на поверхности лимфоцитов, антиген, ассоциированный с функцией лейкоцитов (LFA-1), и молекулы межклеточной адгезии (ICAM-1 и ICAM-2) взаимодействуют между собой. В норме ICAM-1 экспрессируется в основном на клетках, выстилающих синусоиды, и в незначительной степени на портальном и печёночном эндотелии. Синусоидальная мембрана гепатоцита представляет собой домен, который содержит большое количество рецепторов и обладает высокой метаболической активностью. Он отделён от жёлчного канальца латеральным доменом, который участвует в межклеточном взаимодействии. Рецепторно-опосредованный эндоцитоз обеспечивает перенос крупных молекул, таких, как гликопротеины, факторы роста и белки-переносчики (трансферрин). Эти лиганды связываются с рецепторами синусоидальной мембраны, которые образуют окаймлённые клатрином ямки, обеспечивающие начало эндоцитоза. Судьба лиганда внутри клетки различна. Многие лиганды переносятся в лизосомы, где разрушаются, а рецепторы возвращаются на синусоидальную мембрану для повторного использования. Некоторые лиганды переносятся в составе пузырьков через клетку и выделяются в просвет жёлчных канальцев.
Основные функции печени Печень является важнейшим органом, принимающим участие в обмене веществ, как образующихся в организме, так и поступающих в него. По многообразию метаболических реакций она превосходит все другие органы. Некоторые обменные процессы (например, синтез мочевины) протекают только в печени, поскольку лишь печень располагает для них необходимыми ферментными системами. Обмен веществ в печени необходим не только для поддержания структуры и функции данного органа, но и для выработки определенных субстанций, поступающих затем в кровь и участвующих в осуществлении важных функций других органов. Гомеостаз ряда веществ, являющихся субстратами метаболизма (например, глюкозы), обеспечивается также печенью. 1. Синтетическая. Печень осуществляет синтез белков, ферментов, факторов свертывания крови, холестерина, фосфолипидов и др. В печени происходит основное образование кетоновых тел. 2. Детоксицирующая для эндогенных и экзогенных веществ. Детоксикация лекарственных препаратов включает 2 фазы: 1 - модификация лекарств в окислительно-восстановительных реакциях с помощью цитохрома Р450, 2 фаза - конъюгация лекарств водорастворимыми веществами путем присоединения глюкуроновой, серной кислот, глутатиона и др. При заболеваниях печени реакции первой фазы снижены или отсутствуют. 3. Секреторная. Желчесекретирующий аппарат включает желчные канальцы, микроворсинки, прилегающие к ним лизосомы и комплекс Гольджи. Механизм секреции желчи включает выделение холестерина, желчных кислот, пигментов, фосфолипидов в виде специфического макромолекулярного комплекса - желчной мицеллы. Образовавшиеся в печени первичные желчные кислоты поступают в кишечник, где под действием кишечной флоры превращаются во вторичные желчные кислоты. Последние всасываются в кишечнике и вновь поступают в печень (кишечно-печеночная циркуляция). Печень их конъюгирует с глицином и таурином, превращая в амфифильные соединения, обладающие высокой способностью к эмульгированию гидрофобных веществ. Любые процессы, вызывающие нарушение соотношения компонентов в желчи (гормональные, воспалительные и др.), приводят к нарушению желчеотделения - холестазу. 4. Экскреторная - выделение с желчью различных, в том числе твердых, веществ. Белоксинтетическая функция. 1. альбумины 100%, 2. a1-глобулины 90%, 3. a2-глобулины 75%, 4. b-глобулины 50%, 5. g-глобулины - небольшое количество, 6. фибриноген, 7. факторы свертывания крови (в т.ч. витамин К-зависимые) 8. псевдохолинэстераза (ХЭ) Альбумин относится к самым легким белкам крови, ОММ 65-70 кДа, и синтезируется исключительно печенью. Альбумины поддерживают онкотическое давление, снижение содержания приводит к отекам. Если снижение концентрации альбумина не связано с неполноценным питанием, нарушением всасывания в кишечнике или большой потерей белка, оно обусловлено выраженным снижением функции печени. Альбумины играют важную роль в транспортировке веществ, плохо растворимых в воде (гидрофобных). К таким веществам относятся билирубин, холестерин, жирные кислоты, ряд гормонов и лекарств. Нарушение транспортной функции альбумина приводит ко многим патологическим изменениям. Печень поддерживает уровень аминокислот, в т.ч. циклических (тирозин, триптофан, фенилаланин), нейтрализует аммиак, превращая его в мочевину. Синтез мочевины - одна из самых стабильных функций печени. 2. Обмен липидов. Синтез холестерина на 90% осуществляется печенью и кишечником. Значительная часть холестерина в печени превращается в желчные кислоты, стероидные гормоны, витамин D. Печень преобразует токсичные для мозга жирные кислоты с короткой цепью (4-8 атомов углерода - капроновая, изовалериановая и др.) в жирные кислоты с длинной цепью (16-18 атомов углерода). 3. Углеводный обмен. Печень является центральным органом гомеостаза глюкозы, путем гликогенеза, гликогенолиза, глюконеогенеза. Печень вырабатывает инсулиназы - ферменты, расщепляющие инсулин, поддерживает уровень молочной и пировиноградной кислот. 4. Пигментный обмен включает превращение в гепатоците путем конъюгации с глюкуроновой кислотой токсичного жирорастворимого непрямого билирубина, в нетоксичный водорастворимый прямой. Выделение билирубинглюкуронида может происходить либо путем прямой секреции в желчный капилляр, либо включением в желчную мицеллу. 5. Обмен порфиринов включает синтез гема, состоящего из комплекса протопорфирина с железом. Гем необходим для синтеза гемсодержащих ферментов печени (цитохромы и др.). Врожденное нарушение синтеза гема в печени приводит к заболеваниям - печеночным порфириям. 6. Обмен гормонов. При заболеваниях печени наблюдается повышение уровня гормонов, связанное с нарушением их секреции с желчью или искажением нормального обмена гормона (недостаточного разрушения). Повышается уровень адреналина и норадреналина (медиаторов симпатической нервной системы), минералокортикоида альдостерона, половых гормонов, особенно эстрогенов, тканевых гормонов серотонина и гистамина. 7. Обмен микроэлементов. Печень синтезирует белки для транспорта и депонирования железа, она также является основным депо железа. Печень играет важную роль в обмене меди: она синтезирует церулоплазмин - гликопротеид, связывающий до 90% меди крови, а также поглощает из плазмы крови медь, непрочно связанную с альбумином, и экскретирует избыток меди при помощи лизосом с желчью в кишечник. Биохимические исследования. Биохимические исследования играют важную роль в диагностике и определении тяжести, прогноза и течения заболеваний печени. В большинстве случаев эта оценка становится возможной не по результатам отдельного теста, а на основании интерпретации данных, полученных при применении нескольких тестов. Для более удобной оценки целесообразно сгруппировать применяемые тесты в зависимости от исследуемой функции печени. С помощью биохимических тестов можно охарактеризовать: ● целостность гепатоцитов; ● экскрецию желчи; ● синтетическую функцию печени; ● другие специальные функции. Оценка целостности гепатоцитов, нарушения которой в легких случаях проявляются повышенной проницаемостью клеточной мембраны, а в тяжелых случаях - некрозом клеток, проводится на основании обнаружения ферментов печеночных клеток в плазме крови. Чаще всего с этой целью ис- пользуют определение активности трансаминаз - аспартатаминотрансферазы (АсАТ) и аланинаминотрансферазы (АлАТ). Чувствительность трансаминаз является высокой. Глутаматдегидрогеназа (ГЛДГ) содержится исключительно в митохондриях и характеризуется наибольшей активностью в перивенозных гепатоцитах ацинуса. Это объясняет, почему наибольший подъем активности данного фермента отмечается при венозном застое в печени и при шоке. Для оценки экскреции желчи применяется прежде всего определение активности щелочной фосфатазы (ЩФ) и гамма - глутамилтранспептидазы (ГГТП). Увеличение активности этих ферментов в плазме крови при холестазе объясняется их усиленным освобождением из каналикулярных мембран гепатоцитов и их повышенным синтезом. Повышение активности ГГТП не считается специфичным для холестаза, поскольку может встречаться также при нарушении целостности гепатоцитов. Этот фермент является в настоящее время наиболее чувствительным клинико-биохимическим маркером заболеваний гепатобилиарной системы; его повышение наступает сравнительно рано и бывает очень выраженным при алкогольном поражении печени. Гипербилирубинемии как симптом холестаза характеризуются достаточно низкой чувствительностью и специфичностью. Однако определение фракций билирубина имеет важное дифференциально - диагностическое значение, поскольку позволяет разграничить конъюгированную и неконъюгированную гипербилирубинемию. Исследование уровня билирубина помогает также в оценке прогноза при некоторых хронических заболеваниях печени. Для оценки синтетической функции печени применяется в первую очередь исследование уровня факторов свертывания крови, которые вырабатываются только в печени и имеют короткий период полураспада в плазме (например, фактор VII). Чаще всего определяется протромбиновое время по Квику, которое зависит от факторов свертывания I, II, V, VII и X, синтезируемых в печени. Поскольку для некоторых из этих факторов (II, VII и Х) необходимо еще и присутствие витамина К, увеличение протромбинового времени может обусловливаться не только снижением синтетической функции печени, но и уменьшением всасывания витамина К вследствие холестаза. Активность холинэстеразы в сыворотке также отражает состояние синтетической функции печени. Этот фермент вырабатывается в печени, время его полураспада в крови составляет около 10 дней. Напротив, определение уровня альбумина в плазме как показателя, отражающего сниженную синтетическую функцию печени, характеризуется достаточно низкими чувствительностью и специфичностью. Хотя альбумин вырабатывается исключительно в печени, ее резервные способности в этом плане настолько высоки, что уровень альбумина в плазме начинает снижаться только при выраженном поражении паренхимы печени. Кроме того, снижение синтеза альбумина может компенсироваться уменьшением его распада. Другими причинами, приводящими к гипоальбуминемии, могут служить заболевания, сопровождающиеся синдромом мальабсорбции. Клинико-биохимические методы оценки специальных функций печени применяются с целью диагностики определенных заболеваний. Так, поликлональная гипергаммаглобулинемия индуцируется при хронических заболеваниях печени антигенами желудочно-кишечного тракта, которые в результате сниженной функции печени или вследствие формирования портокавальных анастомозов недостаточно удаляются из крови. Эти антигены стимулируют образование антител плазматическими клетками, происходящими из В-лимфоцитов. Наличие фиброза можно установить, определив уровень в сыворотке пептида проколлагена типа III. Таблица 2. Уробилиноген Под влиянием бактерий билирубин в кишечнике превращается в бесцветные тетрапиррольные соединения, которые называют общим термином «уробилиноген». Приблизительно 20% от его общего количества абсорбируется в кишечнике и затем вновь экскретируется печенью с жёлчью. Небольшая часть уробилиногена выделяется с мочой. Содержание уробилиногена в моче используют в дифференциальном диагнозе заболеваний печени и жёлчных путей. При полной обструкции жёлчного протока, когда билирубин не поступает в кишечник, уробилиноген в моче может отсутствовать. Прямой билирубин в сыворотке Содержание прямого билирубина в сыворотке в норме составляет 0,00- 5,1 мкмоль/л. Исследование обычно проводят в целях дифференциальной диагностики желтух. При паренхиматозной желтухе наступает деструкция печеночных клеток, нарушается экскреция прямого билирубина в желчные капилляры, и он попадает непосредственно в кровь, где содержание его значительно увеличивается. Кроме того, снижается способность печеночных клеток синтезировать билирубинглюкурониды; вследствие этого количество непрямого билирубина в крови также увеличивается. При механической желтухе нарушено желчевыделение, что приводит к резкому увеличению содержания прямого билирубина в крови. Несколько повышается в крови и концентрация непрямого билирубина. При гемолитической желтухе содержание прямого билирубина в крови не изменяется. Непрямой билирубин в сыворотке Содержание непрямого билирубина в сыворотке в норме составляет 3,4-13,7 мкмоль/л. Исследование непрямого билирубина играет важнейшую роль в диагностике гемолитических анемий. В норме в крови 75 % общего билирубина приходится на долю непрямого (свободного) билирубина к 25 % на долю прямого (связанного) билирубина. Непрямой билирубин повышается при гемолитических анемиях, пернициозной анемии, при желтухе новорожденных, синдроме Жильбера, синдроме Криглера-Найяра. Повышение непрямого билирубина при гемолитической анемии обусловлено интенсивным образованием его вследствие гемолиза эритроцитов, и печень оказывается неспособной к образованию столь большого количества билирубин-глюкуронидов. При перечисленных синдромах нарушена конъюгация непрямого билирубина с глюкуроновой кислотой. Щелочная фосфатаза Активность ЩФ повышается при холестазе и в меньшей степени при поражении гепатоцитов. Увеличение синтеза ЩФ гепатоцитами связано с повышенным образованием белка и РНК. Выделение фермента в сыворотку может быть обусловлено его проникновением из канальцев в синусоиды через разрыхлённые плотные контакты. Повышение активности ЩФ связано также с повышенным выделением ЩФ в синусоиды из плазматических мембран гепат
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2020-11-11; просмотров: 122; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.222.111.24 (0.101 с.) |