
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Термодинамические процессы газов
Пример 17. В баллоне вместимостью 15 л содержится воздух под давлением 0,4 МПа и при температуре 30 ° С. Какова температура воздуха в результате подвода к нему 16 кДж теплоты? Удельная изохорная теплоемкость равна 736 Дж/(кг × К). Решение. Предварительно вычислим массу воздуха по уравнению состояния:
Из формулы для количества теплоты:
Ответ: 345 ° С.
Пример 18. Найти, какая часть теплоты, подведенной в изобарном процессе к двухатомному идеальному газу, расходуется на увеличение его внутренней энергии. Решение. Удельное количество теплоты, подведенной в изобарном процессе, определяется из уравнения: q 12 = Изменение удельной внутренней энергии определяется по формуле: u 2 - u 1 = Следовательно, доля теплоты, затрачиваемой на изменение внутренней энергии: (u 2 - u 1)/ q 12 = Ответ: 71,4%.
Пример 19. Азот массой 0,5 кг расширяется по изобаре при давлении 0,3 МПа так, что температура его повышается от 100 до 300 ° С. Найти конечный объем азота, совершенную им работу и подведенную теплоту. Решение. Предварительно нужно найти удельную газовую постоянную азота R 0 = 8,31/0,028 = 296,8 Дж/(кг × К). Теперь найдем начальный объем азота: V 1 = m × R 0 × T 1 / p 1 = 0,5 × 296,8 × (100+273)/0,3 × 106 = 0,184 м3. Конечный объем найдем из уравнения изобары: V 2 = V 1 × T 2 / T 1 = 0,184 × (300+273)/(100+273) = 0,283 м3. Определим работу изменения объема:
Работа изменения давления изобарного процесса W 12 = 0. Для определения теплоты, подведенной к газу, найдем по табл. 2 приложения среднюю удельную изобарную теплоемкость при средней температуре 200 ° С: Тогда, Q 12 = Ответ: 1,052 × МДж
Пример 20. В компрессоре сжимается воздух массой 2 кг при постоянной температуре 200 ° С от p 1 = 0,1 МПа до p 2 = 2,5 МПа. Найти массу воды m возд, необходимую для охлаждения сжимаемого воздуха, если начальная температура воды 15 ° С, а конечная 50 ° С, удельная теплоемкость воды 4,19 кДж/(кг × К). Решение. Найдем работу сжатия
L12 = 2 × 287,1 × (200+273) × ln (0,1 × 106/2,5 × 106) =-874 кДж. Так как в изотермическом процессе Q 12 = L 12, то Q 12 = - 874 кДж. Это значит, что в результате работы сжатия внутренняя энергия сжимаемого воздуха должна была увеличиться на 874 кДж и для сохранения температуры постоянной столько же теплоты нужно отвести от воздуха путем охлаждения его водой. Искомое количество воды найдем, пользуясь уравнением
Q 12 = Из этого уравнения
Ответ: 5,96 кг.
Пример 21. Воздух массой 2 кг при давлении 1 МПа и температуре 300 ° С расширяется по адиабате так, что объем газа увеличивается в 5 раз. Найти конечные объем, давление, температуру, работу изменения объема и изменение внутренней энергии. Решение. Находим начальный объем газа из уравнения состояния: V 1 = m × R 0 × T 1 / p 1 = 2 × 287,1 × (300+273)/1000000 = 0,329 м3. По условию конечный объем: V 2 =5 × V 1 = 5 × 0,329 = 1,645 м3. Находим конечное давление из уравнения адиабаты: p 2 = p 1 × (V 1 / V 2) k = 1000000 × (1/5)1,41 = 103383 Па. Конечную температуру найдем из уравнения состояния: T 2 = V 2 × p 2 /(m × R 0) =1,645 × 1000000 /(2 × 287,1) = 286,5 К. Работа изменения объема в адиабатном процессе: L 12 = m × R 0 × (T 2 - T 1)/(1- k) = 2 × 287,1 × (286,5-573)/(1-1,41) = 401 кДж. Изменение внутренней энергии в адиабатном процессе равно работе изменения объема, следовательно, U 2 - U 1 = L 12 = 401 кДж. Ответ: 401 кДж.
Пример 22. Воздух с начальным объемом 8 м3 и начальной температурой 20 ° С сжимается по политропе с показателем n =1,2 от давления 0,09 МПа до давления 0,81 МПа. Найти конечные температуру, объем воздуха и работу изменения давления. Решение. Находим конечную температуру:
Определим конечный объем из уравнения Менделеева-Клапейрона:
Работа изменения давления
W 12 = -1,2 × (0,81 × 1,28-0,09 × 8)/(1-1,2) = 1,9 МДж. Ответ: 1,9 МДж.
Решение. Для двухатомного газа показатель адиабаты равен » 1,4. Так как 1<n<k, то линия процесса проходит выше адиабаты и ниже изотермы (рис. 1). Это значит, что теплота подводится, внутренняя энергия уменьшается и за счет этого совершается положительная работа изменения объема.
Решение. Так как n<1, то линия процесса проходит выше изотермы (рис. 2). Это значит, что теплота подводится, внутренняя энергия увеличивается. Положительная работа изменения объема совершается за счет части подведенной теплоты.
Решение. Так как 1<n<k, то линия процесса проходит ниже адиабаты и выше изотермы (рис. 3). Это значит, что теплота отводится, внутренняя энергия увеличивается и за счет этого совершается положительная работа изменения давления. Второе начало термодинамики
|
||||||
|
Последнее изменение этой страницы: 2020-10-24; просмотров: 133; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.139.104.214 (0.008 с.) |
 = 0,4 × 106 × 0,015/(287,1 × 303) = 0,069 кг.
= 0,4 × 106 × 0,015/(287,1 × 303) = 0,069 кг. = 30+16000/(0,069 × 736) = 345 ° С.
= 30+16000/(0,069 × 736) = 345 ° С. .
. .
. /(
/(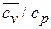 =1/ k = 1/1,4 = 0,714 или 71,4%.
=1/ k = 1/1,4 = 0,714 или 71,4%.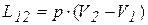 = 0,3 × 106 × (0,283-0,184) = 29,7 кДж.
= 0,3 × 106 × (0,283-0,184) = 29,7 кДж. = 1052 Дж/(кг × К).
= 1052 Дж/(кг × К). = 0,5 × 1052 × (300-100) = 1,052 × 106 Дж.
= 0,5 × 1052 × (300-100) = 1,052 × 106 Дж. ;
;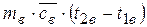 .
.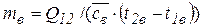 = 874235/(4190 × 35) = 5,96 кг.
= 874235/(4190 × 35) = 5,96 кг. = 293 × (0,81/0,09)0,2/1,2 = 423 К.
= 293 × (0,81/0,09)0,2/1,2 = 423 К. = 423 × 0,09 × 8/(293 × 0,81) = 1,28 м3.
= 423 × 0,09 × 8/(293 × 0,81) = 1,28 м3.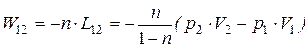 .
.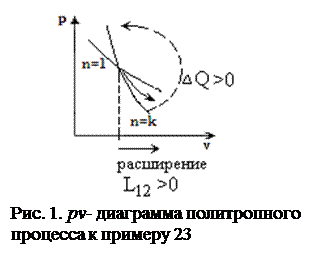 Пример 23. Определить условия протекания политропного процесса расширения двухатомного газа с показателем 1,32.
Пример 23. Определить условия протекания политропного процесса расширения двухатомного газа с показателем 1,32. Пример 24. Процесс расширения газа происходит по политропе с показателем 0,8. Определить условия протекания процесса.
Пример 24. Процесс расширения газа происходит по политропе с показателем 0,8. Определить условия протекания процесса.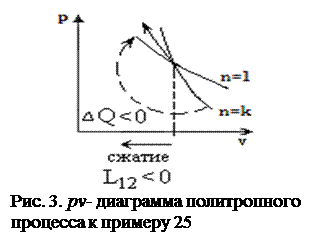 Пример 25. Процесс сжатия воздуха в компрессоре проходит по политропе с показателем 1,15. Определить условия протекания процесса.
Пример 25. Процесс сжатия воздуха в компрессоре проходит по политропе с показателем 1,15. Определить условия протекания процесса.


