
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Анализ основных характеристик химического источника тока
На штатной технике основным источником энергии для стартерного запуска двигателя шасси является аккумуляторная батарея - химический источник тока. Аккумуляторная батарея на автомобиле служит для питания электрическим током стартера при пуске двигателя, для обеспечения током всех других приборов электрооборудования, когда генератор не работает или не может отдавать энергию в цепь. На автомобиле ГАЗ-66 устанавливается свинцовая батарея типа 6СТ-68ЭМ. Номинальное напряжение данной аккумуляторной батареи составляет 12В, емкость при 10-часовом режиме разрядки - 68А×ч. Аккумуляторная батарея состоит из шести аккумуляторных элементов. Каждый аккумулятор представляет собой совокупность положительного и отрицательного электродов и электролита, действие которого основано на использовании обратимых электрохимических систем (рисунок 2.1). Аккумулятор обладает способностью накапливать электрическую энергию от постороннего источника тока в процессе заряда, сохранять ее в течение некоторого времени и отдавать ее в процессе разряда. Электролит, которым заполняются аккумуляторы, состоит из серной кислоты H2SO4 и дистиллированной воды Н2О. Стартерные аккумуляторы отличаются незначительным внутренним сопротивлением, что обеспечивает небольшое падение напряжения на выходных зажимах аккумулятора при его разряде большим током, вследствие чего свинцовые батареи получили наиболее широкое применение в качестве стартерных.
Рисунок 2.1 Схема электрохимических процессов при разряде (а) и заряде (б) свинцового аккумулятора
На рисунке 2.1 используются следующие обозначения:- отрицательный электрод из губчатого свинца;2 - положительной электрод из двуокиси свинца; Н2SO4 - электролит;н - нагрузка, приложенная к аккумулятору;- ток аккумулятора. Общие характеристики аккумуляторов определяют работоспособность и техническое состояние. С течением времени в зависимости от состояния и режимов использования аккумуляторов эти характеристики не изменяются. . Электродвижущая сила аккумулятора (Е), являющаяся разностью потенциалов на выводах при разомкнутой внешней цепи. Величина этой силы зависит от химических свойств и структуры активных веществ пластин, концентрации и свойств электролита и не зависит от размеров электрода:
Е = 0,84 + r, (2.1)
где Е - электродвижущая сила, В; r - плотность электролита, г/см3. Из формулы (2.1) следует, что значение электродвижущей силы зависит от плотности активного вещества аккумуляторной батареи. . Напряжение аккумуляторной (U), которое является разностью потенциалов на выводах батареи при замкнутой внешней цепи, то есть при прохождении через аккумулятор электрического тока. В процессе заряда и разряда напряжение изменяется, но всегда отличается от электродвижущей силы на величину падения напряжения U0 на его внутреннем сопротивлении (Rа). Величина напряжения аккумулятора при разряде равна: р = Е - U0×Е - Iр×Rа, (2.2)
где Uр - напряжение разряда, В; Е - электродвижущая сила, В;0 - падение напряжения, В;а - внутреннее сопротивление аккумулятора, Ом;р - разрядный ток, А. . Внутреннее сопротивление аккумулятора (Rа) представляет собой сумму сопротивлений электродов, электролита, сепараторов, межэлементных соединений и полюсных выводов (Rэ), а также сопротивления поляризации (Rп) обусловленное изменением электродных потенциалов при прохождении тока: a = Rэ + Rп, (2.3)
где Ra - полное сопротивление аккумулятора, Ом;э - сумма сопротивлений электродов, Ом;п - сопротивление поляризации, Ом. Внутреннее сопротивление оказывает существенное влияние как на величину отдаваемого тока, так и на напряжение аккумулятора. Величина разрядного тока определяется по закону Ома для полной цепи:
Iр =
где Iр - разрядный ток, А; Е - электродвижущая сила, В;- сопротивление внешней цепи, Ом;а - внутреннее сопротивление, Ом. У свинцовых аккумуляторов во время разряда изменяется внутреннее сопротивление и уменьшается напряжение. . Емкость аккумулятора (Q) - это количество электричества, отдаваемое им при разряде до определенного конечного напряжения. Емкость измеряется в ампер-часах и определяется по формуле: =
где Q - емкость аккумулятора, А×ч;p - разрядный ток, А;p - время разряда, с. При постоянстве разрядного тока выражение имеет вид: = Ip × Ip. (2.6)
Номинальная емкость по ГОСТ 959-71 определяется для автомобильных аккумуляторов при 20-часовом режиме разряда до конечного напряжения. Разряд аккумулятора до нулевого значения не допускается. Емкость зависит от многих факторов, основными из которых являются: количество активных веществ электродов, участвующих в реакции; плотность и температура электролита; величина разрядного тока; характер нагрузки и величина саморазряда.
На автомобиле ГАЗ-66 при разряде в течение 20 часов ток разряда определяется формулой: р = 0,05×Q20, (2.7)
где Iр - разрядный ток, А;20 - емкость, отдаваемая аккумулятором при 20-часовом разрядном режиме. Таблица 2 Технико-эксплуатационные характеристики аккумуляторной батареи 6СТ-68ЭМ
Конечное напряжение при этом режиме не должно упасть ниже 1,8В. При 10-часовом режиме разряда напряжение должно быть не менее 1,7В. При стартерном разряде величина тока определяется выражением: p = 3Qн, (2.8)
где Ip - ток стартерного разряда, А;н - номинальная емкость аккумулятора, А×ч. В стартерном режиме конечное напряжение на аккумуляторе должно быть не менее 1,5В. Для исправной и работоспособной аккумуляторной батареи значение стартерного тока составляет 204 А. В таблице 2 приводятся основные технико-эксплуатационные характеристики аккумуляторной батареи 6СТ-68ЭМ.
2.2
При стартерном запуске от аккумуляторной батареи потребляется большой ток, который может достигать для стартеров малой мощности (автомобильных) 200-600А. В этом случае резко возрастает внутреннее сопротивление аккумулятора вследствие понижения плотности электролита в порах активной массы, и напряжение на выводах батареи падает. После прекращения разряда большими токами (выключения стартера) плотность электролита в порах активной массы постепенно повышается за счет ее выравнивания, а электродвижущая сила и напряжение постепенно увеличиваются. Длительно разряжать батарею токами стартерного режима нельзя, так как это приведет к интенсивному износу пластин, быстрому разряду батареи, уменьшению отдачи по емкости, сульфации электродов и сокращению срока службы. Поэтому стартер при пуске двигателя шасси включается не более чем на 5-10 секунд с последующим включением не раннее чем через 50-60 секунд. Такой режим пуска благоприятен не только для аккумуляторной батареи, но и для стартера, который не рассчитан на длительную непрерывную работу. Длительный перерыв между включениями стартера позволяет выравниться плотности электролита в порах пластин и не перегреваться стартеру. Если двигатель не запускается после двух-трех повторных включений стартера, то необходимо найти причину, устранить ее и только после этого вновь проводить пуск двигателя.
Принцип действия свинцового кислотного аккумулятора описывается наиболее распространенной теорией двойной сульфации: (-) Pb ½H2SO4½ PbO2 (+) (2.9)
В заряженном состоянии активной массой отрицательного электрода является губчатый свинец Pb, электролитом - водный раствор серной кислоты (H2SO4 + Н2О), активной массой положительного электрода является двуокись свинца PbO2. В исходном состоянии под действием воды происходит электролитическая диссоциация - распад молекул кислоты:
H2SO4
В результате взаимодействия электролита с активными массами на отличительном электроде нейтральный свинец отдает два электрода и становится двухзарядным положительным ионом свинца Pb++. При этом ионы свинца переходят в электролит, а на отрицательной пластине остаются два электрона. На положительной пластине в результате взаимодействия PbO2 с электролитом образуются четырехзарядные положительные ионы свинца Pb++++. Таким образом, в аккумуляторе существует поляризация электродов и между ними имеется разность потенциалов. Под поляризацией понимается изменение потенциала электрода под влиянием прохождения тока от исходного бестокового значения потенциала до нового значения при прохождении тока. При стартерном разряде на отрицательной пластине протекает процесс окисления, а на положительной - восстановления, поддерживающие на отрицательном электроде избыток, а на положительном - недостаток электронов. При подключении нагрузки начинается перетекание электронов с отрицательного на положительный электрод. В то же время на отрицательном электроде атомы свинца, окисляясь, отдают два электрона (на рисунке 2.1), образуя новые двухзарядные положительные ионы свинца Pb++. Здесь этот ион соединяется с кислотным остатком SO4 - -, образуя молекулу сульфата свинца. Вследствие небольшой растворимости в электролите сульфат выпадает из раствора и слагается в виде мелких кристаллов на отрицательной пластине. Электрохимическая реакция у отрицательного электрода описывается уравнением: ++ + SO4- - - 2
На положительном электроде четырехзарядные ионы свинца Pb++++, принимая два электрона, пришедшие с отрицательного электрода, превращаются в двух зарядный ион Pb++. Этот ион поступает в электролит, где соединяется с кислотным остатком SO4 - -, образуя молекулу сульфата свинца, отлагаемую на положительную пластину. Одновременно у положительной пластины кислород соединяется с ионами водорода, образуя воду. Реакция у положительного электрода имеет вид:
О2 + 4Н+ + SO4- - + 2
Разряд аккумулятора можно выразить уравнением:
Таким образом, при стартерном разряде из одной молекулу двуокиси свинца, одного атома свинца и двух молекул серной кислоты образуется на каждой пластине по одной молекуле сульфата свинца, а у положительной пластины - две молекулы воды. Поступление воды в электролит при разряде снижает концентрацию серной кислоты и плотность электролита падает. Вещества, образующиеся во время разряда, имеют более прочную электронную структуру, чем вещества, вступившие в реакцию, и поэтому обладают меньшим запасом энергии, вследствие чего выделяется энергия. Таким образом, при стартерном разряде аккумулятора химическая энергия преобразуется в электрическую, а та, в свою очередь, в механическую энергию. Общий ресурс глубоких разрядов большинства аккумуляторных батарей составляет 100-300 циклов. Автомобильный аккумулятор имеет срок службы 3-4 года, что соответствует пробегу в 40-70 тысяч километров.
|
||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2020-03-14; просмотров: 131; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.227.114.125 (0.017 с.) |

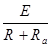 , (2.4)
, (2.4)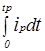 , (2.5)
, (2.5) 2H+ + SO4 - (2.10)
2H+ + SO4 - (2.10) ® PbSO4 (2.11)
® PbSO4 (2.11)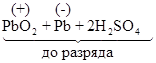 ®
®  (2.13)
(2.13)


