
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Роль почек в реакциях компенсации нарушений кислотно-щелочного равновесияСодержание книги
Поиск на нашем сайте
Почки осуществляют регуляцию содержания кислот и оснований в организме с помощью трех основных процессов: 1. Ацидогенез (секреция Hˉ-ионов эпителием канальцев нефрона и выведения их с мочой путем преобразования основных фосфатов в кислые, а также экскреция слабых органических кислот). Секреция Hˉ-ионов обеспечивается сложной работой эпителия канальце нефрона, где постоянно с участием угольной карбоангидразы из C 2. Аммониогенез. Усиление аммониогенеза наблюдается при значительном снижении pH мочи. Этот процесс заключается в образовании аммиака из глутамина и других аминокислот в эпителии канальцев нефрона и последующем связывании им Hˉ-ионов. Образовавшийся ион аммония реагирует с анионом синильной кислоты (обычно с хлором). Аммиачная соль 3. Реабсорбция гидрокарбоната. Фильтрующийся в нефроне гидрокарбонат обычно не появляется во вторичной моче. Проходя через канальцы, он отдает катион натрия взамен на секретируемые ионы водорода и превращается в угольную кислоту, расщепляющуюся до
|
||
|
Последнее изменение этой страницы: 2020-03-14; просмотров: 217; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.217.89 (0.01 с.) |

 и воды происходит образование угольной кислоты, которая затем диссоциирует на ионы водорода, активно секретируемые в просвет канальцев, а ионы HC
и воды происходит образование угольной кислоты, которая затем диссоциирует на ионы водорода, активно секретируемые в просвет канальцев, а ионы HC 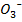 . Интенсивность секреции Hˉ-ионов зависит от количества C
. Интенсивность секреции Hˉ-ионов зависит от количества C  в клетках, а следовательно, от pC
в клетках, а следовательно, от pC  (основного компонента фосфатного буфера), то превращение его в
(основного компонента фосфатного буфера), то превращение его в  вызывает некоторое подкисление мочи, но в меньшей степени, чем свободные ионы водорода. Освобожденные при этом ионы натрия реабсорбируются и уходят в кровь в составе
вызывает некоторое подкисление мочи, но в меньшей степени, чем свободные ионы водорода. Освобожденные при этом ионы натрия реабсорбируются и уходят в кровь в составе 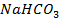 . Количество кислого фосфата и слабых органических кислот (кетановые тела, молочная, лимонная и другие кислоты) определяет титрационную кислотность мочи.
. Количество кислого фосфата и слабых органических кислот (кетановые тела, молочная, лимонная и другие кислоты) определяет титрационную кислотность мочи. выводится с мочой, не снижая значения ее pH. Аммонийный катион способен замещать значительное количество катионов натрия в моче, которые реабсорбирубтся в кровь взамен на секретируемые ионы водорода, и это является одним из путей сохранения гидрокарбоната в организме.
выводится с мочой, не снижая значения ее pH. Аммонийный катион способен замещать значительное количество катионов натрия в моче, которые реабсорбирубтся в кровь взамен на секретируемые ионы водорода, и это является одним из путей сохранения гидрокарбоната в организме. иводы. Моча при этом не меняет своей реакции. Источником образования
иводы. Моча при этом не меняет своей реакции. Источником образования  , отдающей свои Hˉ-ионы в обмен на
, отдающей свои Hˉ-ионы в обмен на 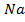 ¯, является
¯, является 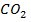 крови в случае повышения его напряжения и
крови в случае повышения его напряжения и  диффундирующий из мочи. Оставшийся в клетках после отщепления ионов водорода HC
диффундирующий из мочи. Оставшийся в клетках после отщепления ионов водорода HC 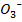 присоединяет реабсорбированный
присоединяет реабсорбированный  восполняет количество гидрокарбоната крови, ушедшего в мочу при фильтрации. Как видно при реабсорбции гидрокарбоната анион HC
восполняет количество гидрокарбоната крови, ушедшего в мочу при фильтрации. Как видно при реабсорбции гидрокарбоната анион HC 


