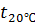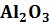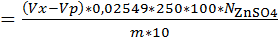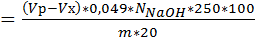Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Метод – йодометрический, основан на титровании выделившегося иода раствор тиосульфата натрия с индикатором крахмалом до обесцвечивания раствора
Массовую концентрацию активного хлора (X), г/дм3, вычисляют по формуле:
Где: V - объем раствора тиосульфата натрия концентрации точно 0,1 моль/дм3, израсходованный на титрование, см3; 8.8625 - масса активного хлора (г), соответствующая 1 см3 раствора тиосульфата натрия концентрации точно 0,1 моль/дм3.
· Массовая концентрация щелочи в пересчете на NaOH Метод – титриметрический, основан на нейтрализации гидроксида натрия соляной кислотой с индикатором фенолфталеином.
Массовую концентрацию щелочи в пересчете на NaOH(X 1), г/дм3, вычисляют по формуле:
Где: V - объем раствора соляной кислоты концентрации точно 0,1 моль/дм3, израсходованный на титрование, см3; 4 - масса гидроксида натрия (г), соответствующая 1 см3 раствора соляной кислоты концентрации точно 0,1 моль/дм3. Хлорное железо FeCl 3 Приложение №5 · Определение плотности хлорного железа
· Определение содержания хлорного железа FeCl 3 Метод – йодометрический, основан на титровании выделевшегося иода раствором тиосульфата натрия с индикатором крахмалом до обесцвечивания. FeCl3 = Где: Vx-объем раствора тиосульфата натрия израсходованный на титрование холостой пробы,см3 Vp- объем раствора тиосульфата натрия израсходованный на титрование анализируемой пробы,см3 m-масса анализируемой пробы, г.
· Определение содержания хлористого железа FeCl 2 Метод – титриметрический, основан на титровании хлорида железа (2) раствором перманганата калия до перехода окраски в розоватую.
FeCl2 = Где: Vx-объем раствора перманганата калия израсходованный на титрование холостой пробы,см3 Vp- объем раствора перманганата калия израсходованный на титрование анализируемой пробы,см3 m-масса анализируемой пробы, г.
· Определение содержания HCl Метод – титриметрический, основан на нейтрализации соляной кислоты раствором гидроксида натрия до выпадения осадка.
Где: V- объем раствора гидроксида натрия израсходованный на титрование,см3 m-масса анализируемой пробы, г. Хлористое железо FeCl 2 Приложение №6 · Определение содержания HCl Метод – титриметрический, основан на нейтрализации соляной кислоты раствором гидроксида натрия с индикатором бромкрезоловым зелёным до перехода окраски из жёлто-рыжей в зелёную.
Где: V- объем раствора гидроксида натрия израсходованный на титрование,см3 m-масса анализируемой пробы, г K-поправочный коэффициент гидроксида натрия, 0,1мольэкв/дм3
· Определение содержания FeCl 2 Метод – титриметрический, основан на титровании хлорида железа (2) раствором перманганата калия до перехода окраски в розоватую.
FeCl2 = Где: Vx-объем раствора перманганата калия израсходованный на титрование холостой пробы,см3 Vp- объем раствора перманганата калия израсходованный на титрование анализируемой пробы,см3 m-масса анализируемой пробы, г. 10. Заключение: Во время прохождения практики в производственной лаборатории: 1. Приобрела опыт работы по исследованию проб с использованием новых методик, требующих серьезной теоретической и практической подготовки для проведения анализа. 2. Закрепила приобретенные во время обучения в техникуме теоретические знания, умения и навыки проведения лабораторных работ, расчетов. 3. Приобрела опыт работы в трудовом коллективе. 4. Изучила структуру предприятия.
11. Вывод: В процессе прохождения производственной практики закрепила навыки и умения, полученные за весь период обучения в техникуме, а также, благодаря выполнения работы лаборанта, формировалась система общих и профессиональных компетенций, которые являются oсновополагающими в дальнейшей профессиональной деятельности. Литературный обзор.
Приложения Приложение№1 Окись амина · Разведение Берём мерную колбу на 250 мл. Наливаем 40 г пробы на технических весах, доводим до метки и перемешиваем. Если из-за пены тяжело довести до метки, то капаем изопропиловый спирт.
· Определение содержания основного вещества
Берём баночку, наливаем 20 мл разведения, 40 мл изопропилового спирта, 5 мл иодистого метила, ставим на 15-20 минут на водяную баню (50°С). Затем ставим остывать до 20°С. Титруем по о,1 мл потенциометрически HCl 0,5н. от pH 5,0-2,5. Осн(л)= Осн(ср)= Осн(т)= Где: V-объем раствора соляной кислоты, израсходованный на титрование,см3 N-концентрация раствора соляной кислоты, моль/дм3 m-масса анализируемой пробы, г. · Определение содержания третичных аминов Берём баночку, наливаем 20 мл разведения, 40 мл изопропилового спирта и титруем по 0,1 мл потенциометрически HCl 0,5н. от pH 5,0-2,5. Т.а(л)= Т.а(ср)= Т.а(т)= Где: V1-объем раствора соляной кислоты израсходованный на титрование третичных аминов, см3 V-объем соляной кислоты израсходованный на титрование основного вещества, см3 N-концентрация раствора соляной кислоты, моль/дм3 m- масса анализируемой пробы, г.
· Определение содержания перекиси водорода Берём коническую колбу на 250 мл, наливаем 20 мл из разведения, добавляем 30 мл изопропилового спирта, 10 мл 4н. H2SO4и 10 мл 10% KI. Ставим в темное место на 15 минут. Титруем Na2S2O3 0,1н. до обесцвечивания. H2O2(л)= Где: V-объем раствора тиосульфата натрия израсходованный на титрование,см3 m-масса анализируемой пробы, г. Приложение №2 Катамин (алкилдиметилбензиламмоний хлоридов) · рН до и после кипячения · Определение массовой доли третичного амина (алкилдиметиламина) Навеску продукта около 5,0 г, взвешенную с точностью до второго десятичного знака, помещают в коническую колбу вместимостью 250 см3,добавляют 20 см3 изопропилового спирта и перемешивают до полного растворения продукта. Добавляют 3-5 капель индикатора метилового красного и титруют 0,1 Н раствором соляной кислоты до перехода окраски из желтой в красную, не исчезающую в течение 1 минуты. Обработка результата анализа:
Где: V-объем раствора соляной кислоты, израсходованный на титрование, см3 0,1 - концентрация раствора соляной кислоты, моль/дм3 М-средняя молекулярная масса алкилдиметиламина, г. m-масса анализируемой пробы, г.
· Определение массовой доли гидрохлорида алкилдиметиламина Навеску продукта массой около 5,00 г., взвешенную с точностью до второго десятичного знака, помещают в коническую колбу вместимостью 250 см3,добавляют 20 см3 изопропилового спирта, и содержимое колбы перемешивают до полного растворения продукта. Добавляют 3-5 капель индикатора тимолового синего и титруют 0,1Н раствором гидроксида натрия до перехода окраски в голубой цвет. Обработка результата анализа:
Где: V-объем раствора гидрокисида натрия, израсходованный на титрование, см3 0,1 - концентрация раствора гидрокисида натрия, равна 0,1моль/дм3 М-средняя молекулярная масса алкилдиметиламина, г. m-масса анализируемой пробы, г.
· Определение основного вещества Навеску продукта массой около 0,2500г,взвешенную с точностью до четвертого десятичного знака, помещают в коническую колбу вместимостью 250 см3.Добавляют 30 см3 воды,20 см3 изопропилового спирта и (1-1,5) см3 раствора калия хромовокислого и проводят титрование раствором нитрата серебра до появления слабой, но вполне заметной красно-коричневой окраски.
Обработка результата анализа:
Где: V-объем раствора нитрата серебра,израсходованный на титрование, см3 0,05 - концентрация раствора нитрата серебра, моль/дм3 М-средняя молекулярная масса алкилдиметилбензиламмонийхлорида, г. m-масса анализируемой пробы, г. X2-массовая доля гидрохлорида алкилдиметиламина,% М1-средняя молекулярная масса гидрохлорида алкилдиметиламина, равная (М-126,5+36,5) За результат анализа принимают среднее арифметическое 3-х определений, абсолютное расхождение между которыми не должно превышать допускаемое расхождение, равное 0,8% Допускаемая относительна суммарная погрешность результата анализа ±2% при доверительном интервале Р=0,95
Приложение №3
Сульфат алюминия Al 2 (SO 4)3
· Перед началом анализа пробу необходимо отфильтровать в стакан, через фильтр синяя лента.
· Определение плотности
Ареометр 1,300-1,360
· Определение рН Берём баночку, наливаем 50 мл пробы и измеряем на иономере
· Определение содержания основного вещества Al 2 O 3 Разведение Берём навеску пробы 14,5 г на аналитических весах и помещаем в мерную колбу на 250 мл, доводим до метки дистиллированной водой и перемешиваем. · Определение содержание основного вещества В коническую колбу на 250 мл помещаем аликвоту из разведения 10 мл и подкисляем 5% H2SO4по метиловому оранжевому. Добавляем 25 мл 0,1н. раствором трилона Б и нейтрализуют аммиаком до изменения окраски на желтую. Раствор кипятят 2-3 минуты, охлаждают до комнатной температуры, добавляют 10 мл буферного раствора рН=5,5-6,0, 4-6 капель индикатора ксиленового оранжевого. Титруют с холостой пробой 0,1н. раствором ZnSO4 до перехода окраски из лимонно-желтой в розово-фиолетовую. Al2O3 Где: Vx-объем раствора сульфата цинка израсходованный на титрование холостой пробы,см3 Vp- объем раствора сульфата цинка израсходованный на титрование анализируемой пробы,см3 N- концентрация раствора сульфата цинка, моль/дм3 m-масса анализируемой пробы, г.
· Определение содержания H 2 SO 4 В коническую колбу на 250 мл приливаем 20 мл из разведения, добавляем 4-5 капель H2O2, даём постоять 3-4 минуты, 5 мл 0,1н. H2SO4, 25 мл 1М K2C2O4, индикатор метиловый красный, добавляем 25 мл 1М MgCl2.
Титруем 0,1н. NaOH от розового до желтого. Одновременно проводим титрование холостой пробы. H2SO4 Где: Vx-объем раствора сульфата цинка израсходованный на титрование холостой пробы,см3
Vp- объем раствора сульфата цинка израсходованный на титрование анализируемой пробы,см3 N- концентрация раствора гидроксида натрия, моль/дм3 m-масса анализируемой пробы, г. Если Vp<,чем Vх, то H2SO4=> отсутствует в пробе Приложение №4
|
||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2019-08-19; просмотров: 209; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.133.141.6 (0.059 с.) |
|||||||||||||||||||||||||||||||||||
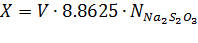
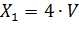
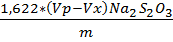
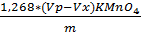
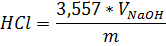
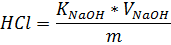
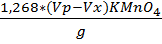
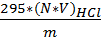
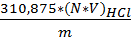
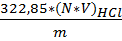

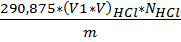
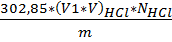
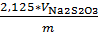
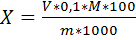 ,
,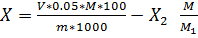 ,
,