
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Определение процессов горения
Горение – это сложный физико-химический процесс, при котором горючие вещества и материалы под воздействием высоких температур вступают в химическое взаимодействие с окислителем (кислородом воздуха), превращаясь в продукты горения, и который сопровождается интенсивным выделением тепла и световым излучением. Условия, необходимые для возникновения процесса горения: - наличие горючего вещества (Г.В.); - наличие окислителя (О.) - кислорода воздуха; - наличие источника зажигания (И.З.). - горючее вещество должно быть нагрето до определенной температуры, при которой начнется процесс окисления; - чтобы нагреть горючее вещество до определенной температуры, необходима определенная мощность источника зажигания; - чтобы поддерживать процесс горения, необходимы определенные концентрации горючего и окислителя. Важнейшие процессы при горении - тепло- и массоперенос. Наиболее общее свойство горения - это возникновение пламени и перемещение его по всей горючей смеси путем передачи тепла или диффузии активных частиц из зоны горения в свежую горючую смесь. Пламя - это видимое проявление горения. Его называют также зоной горения. Это та часть пространства, где происходит превращение горючей смеси в продукты полного и неполного сгорания. Главными параметрами процесса горения, приводящими к гибели людей и наносящими материальный ущерб, являются: - большое количество тепла; - высокая температура; - токсичный состав продуктов горения. Процесс горения с позиций молекулярно-кинетической теории газов
Рис. 2.1. Доля активных молекул в зависимости от температуры: Т2>Т1
При нагревании газовой горючей смеси в ней увеличивается избыточная энергия. Разность между средним уровнем запаса энергии молекул в активном состоянии и средним уровнем неактивном состоянии, называется энергией активации. Это можно представить графически (рис. 2).
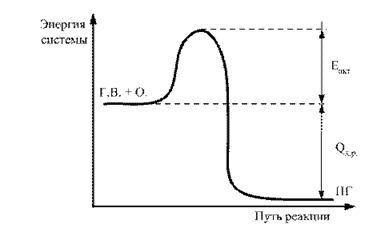
Рис. 2.2. Энергетическая диаграмма хода реакции Г.В. + О. ® П.Г.: Еакт – энергия активации; Qх.р – тепловой эффект реакции горения
Энергия, выделившаяся в результате взаимодействия «первых» прореагировавших молекул передается соседним молекулам. Они возбуждаются, процесс повторяется вокруг прореагировавших молекул с большой частотой и интенсивностью. Начинается самоподдерживающийся, самоускоряющийся на всю реакционную смесь (2Н2 + О2) процесс химического взаимодействия, сопровождающийся образованием молекул воды и выделением в окружающую среду тепла и сопровождающийся свечением, т.е. возникает и распространяется процесс горения.
Чем выше численное значение Еакт, тем труднее заставить данную пару компонентов вступить в химическое взаимодействие. Поэтому величина Еакт является косвенным показателем степени пожарной опасности данной химической системы. Виды и режимы горения Горение можно классифицировать по следующим параметрам: 1. По условию смесеобразования горючих компонентов: а) кинетическое – горение предварительно перемешанных газо- или паровоздушных смесей. Так как смесь горючего и окислителя готова к горению до момента ее воспламенения, то суммарная скорость процесса горения зависит только от скорости химической реакции горения. Если такое горение будет происходить в замкнутом или ограниченном объеме, то тогда может произойти взрыв. Так как энергия, выделяющаяся при сгорании смеси, не успевает отводиться за пределы данного объема, за счет увеличения давления возможно разрушение конструкций; б) диффузионное, диффузионным горением называется горение, когда образование горючей среды (смешение горючего и окислителя) происходит перед зоной горения или в зоне горения. 2. По интенсивности поступления горючих компонентов в зону химической реакции: а) ламинарное, при этом компоненты горючей смеси поступают в зону горения сравнительно спокойно. При этом численное значение критерия Рейнольдса, который характеризует термодинамический режим, будет значительно меньше критического (Re<2300). б) турбулентное, при этом компоненты горючей смеси поступают в зону горения с большой скоростью. Число Рейнольдса в этом случае больше 2300. 3. По агрегатному состоянию компонентов горючей смеси: а) гомогенное горючее и окислитель находятся в одинаковом агрегатном состоянии (газообразном); б) гетерогенное (разнофазное) - горючее и окислитель находятся в различных агрегатных состояниях.
4. По скорости распространения зоны химической реакции горения: а) дефлаграционное (медленное) распространение зоны химической реакции (скорость от 0,5 до 50 м/с); б) детонационное (взрывное), когда зона химической реакции горения распространяется со скоростью ударной волны (от нескольких сотен метров в секунду до нескольких километров в секунду). Пространство, в котором сгорают пары или газы, называется пламенем. Ламинарные пламена предварительно перемешанной смеси. В ламинарных пламенах предварительно перемешанной смеси горючее и окислитель смешиваются до начала горения и поток ламинарен. Пламя предварительно перемешанной смеси называют стехиометрическим, если горючее (углеводород) и окислитель (кислород — О2) расходуют друг друга полностью, образуя двуокись углерода (СО2) и воду (Н2О). Если существует избыток горючего, говорят, что смесь богатая, а в случае избытка окислителя говорят, что смесь бедная [3]. Рассмотрим простейшие примеры: 1) 2Н2 + O2 → 2Н2О — стехиометрическая смесь, 2) ЗН2 + О2 → 2H2O + Н2 — богатая смесь (Н2 в избытке), 3) СН4 + ЗО2 → 2Н2О + СО2 + О2 - бедная смесь (О2 в избытке). Каждый символ в таком уравнении химической реакции соответствует одному молю вещества. Так, первое из этих уравнений означает, что два моля Н2 реагируют с одним молем О2 с образованием двух молей Н2О. Если уравнение химической реакции записано таким образом, что оно описывает реакцию именно одного моля горючего, то мольная доля горючего в стехиометрической смеси может быть легко определена из соотношения хгор,стех = 1/ ((1+v) Здесь v обозначает число молей О2 в уравнении реакции с образованием СО2 и Н2О. Примером служит реакция H2+0,5O2→H2O, v=0,5, xH2,стех = 2/3 Если окислителем является воздух, то следует принимать во внимание, что сухой воздух содержит только 21 % кислорода, а также 78 % азота и 1 % благородных газов. Таким образом, для воздуха XN2 = 3,762 XO2. Отсюда мольные доли для стехиометрической смеси с воздухом будут равны хгор,стех = 1/ ((1+v∙4,762),
где v как и прежде означает количество молей О2 в уравнении реакции полного превращения одного моля горючего в СО2 и Н2О. Ряд примеров значений v и мольных долей горючего для стехиометрических смесей горючего с воздухом приведен в таблице 1. Предварительно перемешанные смеси горючего и воздуха (в этом случае в уравнение реакции должно быть добавлено соответствующее количество N2, см. табл. 1) характеризуются величиной эквивалентного отношения для воздуха: λ = (хвоз/хгор) / (хвоз,стех / хгор,стех) = (wвоз/wгор) / (wвоз,стех / wгор,стех) либо обратной величиной — эквивалентным отношением для горючего Ф (Ф = 1/λ). Эту формулу можно преобразовать для того, чтобы можно было определить величины мольных долей смеси по значению Ф: хгор = 1/ ((1+(4,762∙v) / Ф), хвоз = 1 – хгор,
Примеры значений v и мольных долей горючего x гор, стех для стехиометрических смесей горючего с воздухом
|
||||||
|
Последнее изменение этой страницы: 2017-02-22; просмотров: 326; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.59.218.147 (0.007 с.) |

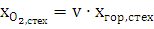 ,
,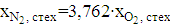
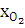 = хвоз / 4,762,
= хвоз / 4,762, 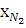 =
= 


