Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Одержання (азото-водневої суміші) (авс) параповітряною конверсією метану на пат «азот» (черкаси)
Хімізм процесів зберігається, але конверсія відбувається не чистим О2, а киснем із повітря. Динітроген залишається у реакційній суміші і продуктами процесу є N2 + Н2 + СО2. СО2 – адсорбується і використовується для виробництва карбаміду (сечовини), залишається суміш, що складається з динітрогену і дигідрогену. Синтез амоніаку N2 + 3H2 ↔ 2NH3 ∆Н = −111,6 кДж. В даному разі має місце основне протиріччя зворотних екзотермічних реакцій. Суть якого полягає в тому, що за принципом Ле Шател’є для зміщення рівноваги реакції вправо температуру необхідно знижувати, а для прискорення швидкості реакції її необхідно збільшувати. Процес проводять за температури 500°С. Вихід: свідомо йдуть на зменшення виходу, але досягають значних швидкостей, цьому ж сприяє застосування каталізатора. Реакція синтезу амоніаку каталізується металами, що мають недобудовані d- i f-електронні підрівні (Fe, Rh, W, Os, Pt та інші). Зараз широко впроваджено використання контактної маси ГИАП: Fe + Al2O3 + R2O + CaO + SiO2 Тзапал. = 450-500°С. Каталізатор промотори носій Механізм дії каталізатора: І стадія: дифузія молекул Н2 і N2 до поверхні каталізатора; ІІ стадія: хемосорбція молекул реагентів на поверхні каталізатора (ця стадія є лімітуючою); ІІІ стадія: хімічна взаємодія Н2 і N2 на зернах каталізатора з переносом електронів від молекул Н2 до молекул N2 з утворенням поверхневих нестійких комплексів; ІV стадія: десорбція утворених молекул NН3 з поверхні каталізатора; V стадія: дифузія молекул NН3 у газову фазу (схема 8.1). Схема 8.1. Механізм каталітичної дії порошкоподібного відновленого заліза при синтезі амоніаку. І ст. (дифузія) ІІ ст. (хемосорбція) ІІІ ст. (хім. взаємодія) ІV ст. (десорбція) Vст. (дифузія у газовий потік)
Fe + N≡N → N≡N → NH=NH → NH2−NH2 → NH3 NH3 → імід амід амоніак
Іст. (дифузія) ІІст. (хемосорбція) ІІІст. (хім.. взаємодія) Каталізатор готують відновленням оксидів заліза дигідрогеном або сумішшю дигідрогену і динітрогену безпосередньо в колоні синтезу.
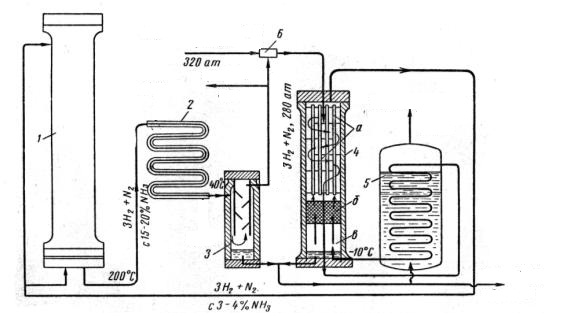
1) зміщенню рівноваги реакції вправо; 2) зростанню швидкості реакції за законом діючих мас. Через парціальні тиски це має вигляд: V = k · PN2 · P3H2 3) покращується конденсація амоніаку, що створює умови для його виведення із реакційного середовища. Склад реакційної суміші вибирається максимально близьким до стехіометричного. Оскільки ступінь перетворення становить 14-20%, то процес проводиться за циркуляційною схемою. Обов’язково необхідно проводити віддувку так званих інертних домішок або продувочних газів (Ar, CH4). Процес здійснюється у відповідності до схеми (рис.8.2).
Рис. 8.2. Технологічна схема виробництва амоніаку: 1 - колона синтезу (трубчастий теплообмінник, центральний газохід, теплообмінник «труба в трубі»);2 - конденсатор «труба в трубі»; 3 -газороздільник; 4 - конденсаційна колона (газороздільник, насадка, трубчастий теплообмінник);5 - випарювач рідкого амоніаку; 6 -інжектор(змішувач).
|
||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-22; просмотров: 184; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.217.4.206 (0.005 с.) |



 Fe Fe Fe Fe
Fe Fe Fe Fe
 Процес синтезу амоніаку проводять за умови підвищеного тиску. Не зважаючи на високу вартість процесів, що відбуваються за умови використання високих тисків, такий режим є вигідним, бо в даному разі відсутня баластна речовина. Підвищений тиск сприяє:
Процес синтезу амоніаку проводять за умови підвищеного тиску. Не зважаючи на високу вартість процесів, що відбуваються за умови використання високих тисків, такий режим є вигідним, бо в даному разі відсутня баластна речовина. Підвищений тиск сприяє: