
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Параметры, характеризующие качество и свойство глин.
1. Объемная концентрация глины – КГ На основе уравнения баланса масс: mк = mисх + Σmдоб mр = mв + mг Vр × r р = Vр × (1 – Кг) × r в + Vр × Кг × r г
mраствора mв mг
r р = 2. Выход раствора – Вр (м3 из 1 т. глины)
= 1т
Выход раствора определяется следующим образом: 1) берутся 3 сосуда с водой по 400 см3 нагретой до 70⁰C; 2) берутся 3 навески глины: 25-30 г, 35-40 г, 50-60г; 3) готовится раствор, используя миксер «Воронеж», перемешивая 5 ¸ 15 минут; 4) измеряем φ600 на приборе ВСН-3 и заносим результаты в таблицу:
5) Строим график φ600 град
Q, г
6) рассчитываем эффективную вязкость μЭ:
7) строим график: mэ МПа×с
mэ=20
Q, г Qст Qст – это та масса навески, при которой мы получаем mэ = 20 МПа×с 8) берем навеску Qст Qст (стандартная масса навески порошка бентонита) для получения 400 см3 раствора, нагреваем до 70⁰С; 9) измеряем условную вязкость, которая должна быть равна 25 с; 10) измеряем плотность раствора (ρст при Qст); 11) определяем выход раствора Вр
12) определяем марку глинопорошка.
3. Способность глины к гидратации. Это способность присоединять (адсорбировать) частичками глины дипольные молекулы воды. Способность к гидратации зависит от вида глин и их характеристик. Na+ - глины, образуются в морском бассейне; Ca++ - глины, образуются в пресноводном бассейне.
1 Å = 1 × 10-10 м Способность взаимодействовать зависит от валентности и размера ионов. Чем выше валентность или заряд иона и меньше поперечный размер этой частицы иона, тем труднее он отделяется от глинистой частицы и труднее идет гидратация. Поэтому Na+ глины более интенсивно гидратируют, отделяя свои частицы от общего объема и замещая их молекулами воды.
Са+2 Са+2 Н2О
Са+2 Са+2
Ca2+-глины менее интенсивно взаимодействуют с молекулами воды, и такие глины в меньшей степени гидратируют
Na+ Na+ Н2О
Na+ Na+ Na+-глины гидратируют более сильно, образуя мощный гидратный слой вокруг глинистых частиц.
Для Na+-глин идет интенсивное отделение чешуек глины от общего объема, которые замещаются молекулами воды – идет эффективная гидратация.
4. Влияние минерализации – содержание хлоридов натрия (NaCl)
а) до ввода NaCl Na+ Н+ Na+ + ОН- = NaОН
ОН- Н2О «Н+ + ОН-
Na+ Н+ Na+ + ОН- = NaОН
ОН- Н2О «Н+ + ОН-
Na+ Н+ Na+ + ОН- = NaОН
гидратная оболочка рН > 7 – щелочная среда Характерно состояние, при котором глинистая частица меняет Обменные катионы Na+, которые замещаются H+. Образуется щелочная среда рН>7, при которой глина хорошо гидратируется. б) после ввода NaCl: Н+ + Cl- = HCl Н+ Na+ NaCl «Na+ + Cl- ОН-
Н+ + Cl- = HCl Н+ Na+ ОН-
ОН- Н+ + Cl- = HCl Н+ Na+ рН < 7 – кислая среда После ввода в раствор NaCl катионы Н+ вытесняют с поверхности глинистых частиц Na+, за пределами адсорбционного и диффузного слоев концентрация Н+ возрастает, образуется кислая среда (рН<7), которая способствует уменьшению гидратации глинистых частиц. Качество раствора ухудшается. В кислой среде взаимодействие частиц глины и воды уменьшается. Для получения глинистого раствора высокого качества должно быть pH = 8 ¸ 9. 5. Схема кристаллической решетки глин Глины имеют слоистое строение. Среди этих слоёв выделяют:
Обменные катионы
Рис.47. Схема кристаллической решетки глин. 6. Обменная ёмкость глин Это количество г-ион. (молей) обменных катионов, которое содержится в одном кг сухой глины. Причинами катионного обмена глин являются следующие факторы: 1) Внутрикристаллическое замещение, связанное с катионным обменом (замещение атомов Al и Li обменными катионами); 2) Нарушение связей на краях глинистых частиц; +
- 3) Наличие катионов водорода и анионов гидроксила (ОН-) внутри кристаллической решетки или в межслоевом пространстве. Монтмориллонит имеет обменную емкость 0,8 ÷ 1,6 г-ион на 1кг сухой глины; Гидрослюды имеют обменную емкость 0,1÷ 0,4 г-ион на 1кг сухой глины; Палыгорскит имеет обменную емкость 0,2 ÷ 0,3 г-ион на 1кг сухой глины; Каолинит имеет обменную емкость 0,03 ÷ 0,15 г-ион на 1кг сухой глины.
7.
NH4+ NH4
NH4+ NH4
NH4 NH4+
При насыщении поверхности глинистых частиц NH+-катионами образуется органофильная глина или олеоглина, или аммонийная глина, которая применяется для получения РУО - растворов на углеводородной основе.
|
|||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-19; просмотров: 356; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.128.94.171 (0.012 с.) |

 отсюда
отсюда 

 ;
; 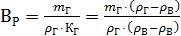
 , м3
, м3




