Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Вопрос 17. Т-клеточная система иммунитета: происхождение, дифференцировка Т-лимфоцитов в тимусе.Содержание книги
Поиск на нашем сайте
Т-система иммунитета включает тимус как центральный орган системы, различные субпопуляции Т-клеток, группу цитокинов, продуцируемых Т-клетками. Основной вопрос, связанный с данной системой, касается изучения роли тимуса в формировании клоноспецифических Т-лимфоцитов, относящихся к разным субпопуляциям. Путь дифференцировки тимоцитов от пре-Т-клеток костного мозга начинается в субкапсулярной зоне органа. Клетки, вступающие в процесс развития, не имеют основных маркеров дифференцировки: корецепторов CD4 и CD8 и Т-клеточного антигераспознающего рецептора (ТКР). Такие тимоциты определяют как двойные негативы. Под влиянием эпителиальных клеток-кормилиц субкапсулярной зоны происходит накопление тимоцитов с умеренной экспрессией CD4 и CD8. Начинается синтез бета-цепи ТКР и последующая экспрессия этого полипептида на клеточной поверхности. Фенотип таких клеток - CD4+-CD8+-бетаТКР+-. Дальнейшее развитие тимоцитов происходит в коре. Здесь под влиянием эпителиальных клеток усиливается экспрессия корецепторов; ТКР представлен полностью сформированной молекулой, хотя его количество на клеточной поверхности умеренно. Основной фенотип клеток коры - CD4+CD8+альфа-бетаТКР+-. Тимоциты этой стадии развития получили название двойных позитивов. В корковой зоне происходит одно из основных событий - положительная селекция клеток на способность узнавать собственные молекулы I или II классов МНС. В процессе селекции отбираются клоны, чьи рецепторы конформационно соответствуют молекулам I или II классов. При распознавании молекул I класса дифференцировка направляется в сторону формированияцитотоксических T-клеток; при распознавании молекул II класса - в сторону T-хелперы. На клеточной поверхности экспрессируется только один из двух корецепторов: CD4 - на поверхности Т-хелперов и CD8 - на поверхности Т-киллеров. Дифференцировка на субпопуляции сопровождается еще одним крайне важным событием для функционирования системы - отрицательной селекцией. Из популяции тимоцитов через процесс апоптозаудаляются клетки, способные реагировать с аутоантигенами, комплексированными с собственными молекулами МНС. Незначительное количество прошедших жесткие условия положительного и отрицательного отбора клеток мигрируют на периферию. Выжившие клетки относят к категории наивных Т-лимфоцитов, т.е. таких клеток, которые еще не вступали в процесс распознавания чужеродных антигенов. В их заселении периферических лифоидных органов и тканей принимают участие адгезивные молекулы клеточной поверхности, экспрессирующиеся как на Т-лимфоцитах, так и на эндотелии кровеносных сосудов, пронизывающих лимфоидные образования. В результате лиганд-рецепторных взаимодействий наивные Т-клетки проникают в паренхиму органа. К Т-системе иммунитета относится также группа цитокинов, продуцируемых клетками этой системы. Их иммунорегуляторное действие начинает проявлятся в основном при антигенной или митогенной стимуляции и носит разнонаправленный характер в зависимости от иммунологической ситуации и типов клеток, принимающих участие в иммунном реагировании. Весь путь доантигенного развития Т-системы иммунитета создает потенциал для возможной в будущем встречи организма с различным антигенночужеродным материалом. 19 вопрос. Все типы лейкоцитов происходят из самоподдерживающейся популяции единой костномозговой полипотентной стволовой кроветворной клетки. В-лимфоциты весь цикл дифференцировки до зрелых В-лимфоцитов проходят в костном мозге. Миграция по организму проходит с током крови.
Система В-лимфоцитов человека: – происхождение, дифференцировка В-лимфоцитов в костном мозге; миграция, круговорот и распределение В-лимфоцитов в организме. Анализ распределения в организме человека В-лимфоцитов показал, что в вилочковой железе доля этих клеток — 0.2 %, в грудном лимфатическом протоке — 15 %, в лимфатических узлах — 25 %, в периферической крови — 30%, в селезенке — 40%, в костном мозгу — 40 %, в пейеровых бляшках — 55 %.
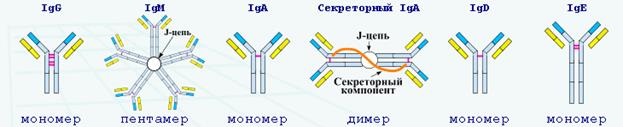
Вопрос 20. Насыщенность иммуноглобулинов чаще всего определяют нефелометрически или турбидиметрически. Но для контроля продукции и секреции иммуноглобулинов В-клетками эти методы недостаточно чувствительны. Например, при определении культуры лимфоцитов с целью дифференциального диагноза первичных иммунодефицитов или оценки тяжести вторичных иммунодефицитов, связанных с низким уровнем антител. Для диагностики высокую чувствительность имеет иммуноферментный метод, который является самым точным и быстрым методом определения анализа. При этом используется автоматические закрытые ферментные системы. Среди 5 классов иммуноглобулинов (IgG, IgA, IgM, IgD и IgE) со средней скоростью синтеза 30 мг/кг веса тела самую высокую концентрацию имеет человеческий иммуноглобулин G (IgG). Время полужизни колеблется между 9 днями для IgG 3 до 21 дня для IgG 1,2 и 4. Благодаря тому что иммуноглобулин G имеет небольшую молекулярную массу, около 150 kD, он может свободно распространяться из сосудистого русла во внесосудистое пространство. Молекулы иммунных комплексов (ИК), в зависимости от субкласса иммуноглобулина G, связывают комплемент с различной силой. ИК связываются Fc -фрагментом с рецепторами на макрофагах, гранулоцитах, лимфоцитах и мастоцитах, обладают свойствами агглютинации и преципитации и запускают реакции, приводящие к лизису и фагоцитозу. Во время беременности фетоплацентарный барьер способен пропускать материнский иммуноглобулина G. Концентрация фетального IgG достигает 10% от взрослых значений к 20-й неделе беременности. Однако его насыщенность к 22-28 неделе стремительно увеличивается. Уровень иммуноглобулина G у матери аналогичен его концентрации у новорожденных. После снижения уровня материнского IgG падает количество антител. Однако потом последовательно растет за счет синтеза, который происходит в организме ребенка. Высокий риск инфекции возникает именно в период, когда снижается концентрация материнских антител. К годовалому возрасту уровень иммуноглобулина G у ребенка достигает 7-8 г/л. Пентамерную структуру имеет человеческий иммуноглобулин M (IgM), масса которого достигает 971 kD. Образуются лимфоцитами, которые соединяются со средней скоростью синтеза 6.7 мг/кг веса тела и временем полужизни 5 дней. Из-за высокой молекулярной массы их количество во внутрисосудистом пространстве достигает уровня 75-80%. Наиболее старым классом иммуноглобулинов являются филогенетические молекулы иммуноглобулин M. Он обладает свойствами полиреактивности и синтезируется как первичный ответ В-клеток на антигенный стимул. В онтогенезе мономер IgM появляется как первый В-клеточный рецептор (sIgM). Молекулы иммуноглобулин M связывают комплемент эффективнее, чем иммуноглобулина G. При этом они обладают свойствами агглютинации и преципитации и значительно усиливают фагоцитоз. Только к 20-й неделе беременности фетальный иммуноглобулин M проявляется в организме. В том случае, если его концентрация в пуповинной крови превышает 0.2 г/л, то это говорит о внутриутробном инфицировании. Насыщенность фетального IgM у новорожденных достигает уровня 105 от взрослого значения и начинает расти только на 2-м году жизни. Иммуноглобулин А (IgA) находится в организме человека чаще всего в виде мономера (85-90%). Его молекулярная масса равна 160 kD. В димерной или полимерной молекуле иммуноглобулина А дополнительно содержится J-цепь. Именно внутри сосудов содержится около 40% IgA. Плазматическими клетками ежедневно синтезируется около 60 мг/кг веса тела иммуноглобулина А. Время полужизни - 5.4 - 5.9 дней. IgA пресекает вирусные антигены и бактериальные токсины. В агрегированном виде может активировать комплемент через альтернативный путь.
IgA – основной иммуноглобулин в биологических секретах. Секреторный иммуноглобулин А находится почти исключительно в виде димера, содержащего секреторный компонент в виде гликопротеина с молекулярной массой 70 kD. Он выполняет защитную функцию на слизистых оболочках. При этом плацентарный барьер непроницаем для иммуноглобулина А, значит, он отсутствует в фетальной крови. Сывороточные концентрации IgA у детей доходит до взрослого уровня только к 12-летнему возрасту.
Вопрос 21. Антитела - иммуноглобулины, продуцируемые В-лимфоцитами (плазматическими клетками). Мономеры иммуноглобулинов состоят из двух тяжелых (Н-цепи) и двух легких (L-цепи) полипептидных цепей, связанных дисульфидной связью. Эти цепи имеют константные (С) и вариабельные (V) участки. Папаин расщепляет молекулу иммуноглобулина на два одинаковых антигенсвязывающих фрагмента - Fab (Fragment anligen binding) и Fc (Fragmenl crislalhzable). По типу тяжелой цепи различают 5 классов иммуноглобулинов IgG, IgM, IgA, IgD, IgE. Активный центр антител - антигенсвязывающий участок Fab-фрагмента иммуноглобулина, образованный гипервариабельными участками Н- и L-цепей, связывает эпитопы антигена. В активном центре имеются специфичные комплементарные участки к определенным антигенным эпитопам Fc-фрагмент может связывать комплемент, взаимодействует с мембранами клеток и участвует в переносе IgG через плаценту.
Домены антител - компактные структуры, скрепленные дисульфидной связью. Так, в IgG различают: V-домены легких (VL) и тяжелых (VH) цепей антитела, расположенные в N-концевои части Fab-фрагмента; С-домены константных участков легких цепей (СL); С-домены константных участков тяжелых цепей (СH1, СH2, СH3). Комплементсвязывающий участок находится в СH2-домене.
|
||||
|
Последнее изменение этой страницы: 2017-02-10; просмотров: 441; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.15 (0.008 с.) |