
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Коэффициенты активности ионов
* * *
В биологических системах широко распространены межионные взаимодействия, которые сильно зависят от ионной силы растворов, что прежде всего сказывается на значениях констант диссоциации ионогенных* групп биологических субстратов, так как они определяются активностями ионов, а не их концентрациями. Незначительное увеличение ионной силы раствора вызывает изменение степени ионизированности белков или нуклеиновых кислот, вследствие чего меняется их конформация, а следовательно, и биологические функции. Поэтому при использовании растворов электролитов в биологических экспериментах крайне необходимо, чтобы их ионная сила была равна ионной силе соответствующей биологической системы. Так, ионная сила плазмы крови человека равна 0,15 моль/л, поэтому физиологический раствор – простейший заменитель плазмы крови – должен иметь соответствующую концентрацию NaCl (0,15 моль/л,или 0,9 %). Таким образом, ионная сила биологических систем, обусловленная содержанием в них сильных электролитов, влияет не только на химическую активность ионов, но и на биологическую функцию белков и нуклеиновых кислот, содержащихся в этих системах, что имеет большое значение в практической медицине. При значительном увеличении ионной силы раствора в нём уменьшается количество свободной воды, не участвующей в гидратации ионов. Другими словами, уменьшается активность воды, участвующей в процессе гидратации растворённых частиц. Это обстоятельство чрезвычайно важно для биологических систем, так как оно приводит к дегидратации природных полиэлектролитов (белков и нуклеиновых кислот), в результате чего вначале изменяется их конформация, а затем происходит даже их высаливание**, то есть выделение белков и нуклеиновых кислот из этих растворов. Влияние ионной силы раствора на растворимость полиэлектролитов имеет большое значение при проведении биохимического эксперимента. Добавление к биологическим жидкостям солей позволяет не только выделить белки и нуклеиновые кислоты, но и фракционировать их по молекулярной массе. При постепенном увеличении ионной силы раствора из него вначале выделяются полиэлектролиты с большей молекулярной массой и меньшей гидрофильностью. Для выделения полиэлектролитов с меньшей молекулярной массой и с большей гидрофильностью требуется создать в растворе более высокую ионную силу.
При выделении природных полимеров из биологических сред наибольшее высаливающее действие проявляют анионы солей, так как структура их гидратной оболочки ближе к структуре гидратной оболочки белков и нуклеиновых кислот, чем катионов. Чем больше заряд аниона и меньше его размер, тем сильнее он гидратируется и тем выше его дегидратирующая способность по отношению к полиэлектролитам. По высаливающему действию анионы могут быть расположены в следующий ряд:
I– < Br– < Сl– < NО3– < SO42– < C2O42–*
В практике для выделения белков обычно используют сульфат аммония (NH4)2SO4. Например, для выделения из крови фибриногена (М = 340 000) требуется ионная сила 2,9, гемоглобина (М =64 450) – 5,8, а миоглобина (М =17 800) – 9,6. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ И ИОННОЕ ПРОИЗВЕДЕНИЕ ВОДЫ
Вода является очень слабым электролитом. Её электролитическая диссоциация выражается равновесием:
Н2О + Н2О ⇄ Н3О+ + ОН– или упрощённо Н2О ⇄ Н+ + ОН– .
При температуре 295 К (22 °С) диссоциирует лишь одна из 5,56 · 108 молекул воды и отсюда степень её электролитической диссоциации составляет α
Константа электролитической диссоциации воды при 22 °С равна:
Это означает, что из 5,6 · 108 молекул воды диссоциирована на ионы только одна. Следовательно, равновесную концентрацию недиссоциированной воды можно считать равной её исходной молярной концентрации, то есть числу молей Н2О в 1 л воды:
Объединив две постоянные величины Каи [Н2О], получим новую постоянную, которую называют ионным произведением воды:
Константа диссоциация воды может быть определена из выражения разбавления Оствальда (2.7):
Ка = α2[H2О] = (l,8 · 10–9)2 · 55,6 = l,82 · 10–16
Подставляя значения в выражение ионного произведения воды в (4.2) значение равновесной концентрации и константы диссоциации воды, находим, что
Ионное произведение воды
Постоянство ионного произведения воды означает, что в любом водном растворе – нейтральном, кислотном или основном – имеются и ионы водорода, и гидроксид-ионы, причём произведение равновесных концентраций этих ионов всегда равно величине
[Н+] = Значения
В чистой воде равновесные концентрации ионов водорода и гидроксид-ионов одинаковы, и при 22 °С их значения равны:
[Н+] = [ОН–] =
Характер водной среды* определяется тем ионом (Н+ или ОН–), концентрация которого преобладает. Для характеристики кислотности водных сред принято использовать величину молярной концентрации ионов водорода [Н+] в этих средах.
Нейтральная среда характеризуется равенством концентраций ионов водорода и гидроксид-ионов:
[Н+] = [ОН–] = 1,0 · 10–7 моль/л (при 22 0С). Кислотная среда характеризуется соотношением:
[Н+] > [ОН–], то есть [Н+] > 10–7 моль/л.
Основная среда характеризуется соотношением:
[Н+] < [ОН–], то есть [Н+] < 10–7 моль/л.
В практике реакцию водной среды принято характеризовать не молярной концентрацией ионов водорода, а водородным показателем.
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-10; просмотров: 240; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.138.204.208 (0.01 с.) |
 1,8 · 10–9.
1,8 · 10–9. . (4.1)
. (4.1) = 18 моль/л. [Н2О] =
= 18 моль/л. [Н2О] =  = 55,56 моль/л = const.
= 55,56 моль/л = const. = Ка[Н2О] = [Н+][ОН–] = соnst. (4.2)
= Ка[Н2О] = [Н+][ОН–] = соnst. (4.2)  – величина постоянная (при данной температуре) для воды и водных растворов, равная произведению равновесных концентраций ионов водорода [Н+] и гидроксид-ионов [ОН–].
– величина постоянная (при данной температуре) для воды и водных растворов, равная произведению равновесных концентраций ионов водорода [Н+] и гидроксид-ионов [ОН–]. при данной температуре. Это позволяет рассчитывать концентрацию ионов Н+ и ОН– в водных растворах, используя следующие формулы:
при данной температуре. Это позволяет рассчитывать концентрацию ионов Н+ и ОН– в водных растворах, используя следующие формулы: и [ОН–] =
и [ОН–] =  . (4.3)
. (4.3) =
= 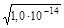 = 10–7 моль/л.
= 10–7 моль/л.


