
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Системы с неограниченной растворимостью
Рассмотрим двухкомпонентную систему A-B, в которой оба компонента неограниченно растворимы в жидком и твёрдом состояниях и не образуют химических соединений (см. рис. 4). В такой системе возможно существование только двух фаз – жидкого раствора Ж и твердого раствора α. Диаграмма в данном случае состоит из трех областей: жидкость (Ж), жидкость + твердый раствор (Ж + α) и твердый раствор (α).
Выше линии AmB находится область, конфигурационные точки которой соответствуют таким значениям температуры и давления, при которых термодинамически равновесным является однофазное жидкое состояние. Эта линия называется линией ликвидус (от liquid – жидкий). Ниже линии AnB расположена область, соответствующая однофазному твердому состоянии. Эта линия называется линией солидус (от solid – твердый). Между линиями ликвидус и солидус расположена область двухфазного (твердое + жидкое) состояния. Температуры плавления подавляющего большинства металла существенно выше температуры, при которой изделия из этих сплавов эксплуатируются. Поэтому технологические процессы получения сплавов обычно содержит нагрев (часто вплоть до перехода в жидкое состояние) и последующее охлаждение. Однако практически значимые свойства сплавов формируются при охлаждении – структуры, формирующиеся при нагреве, разрушаются при плавлении, или изменяются при охлаждении. Поэтому в дальнейшем будем рассматривать процессы (превращения), происходящие в сплавах именно при охлаждении.
1.3.2. Правило отрезков (рычага) Правило отрезков получается как следствие закона сохранения вещества (массы). Применим этот закон к двухфазному сплаву, фазовое состояние которого отображено точкой а на рис. 4. Полное количество (масса) какого-либо компонента в сплаве равна сумме количеств этого компонента во всех фазах. Обозначим массы жидкой и твердой фаз через m1 и m2. Концентрации компонента В в жидкой и твердой фазах определяются точками в и с соответственно, а в сплаве в целом точкой а. Тогда m1в + m2с = (m1 + m2)а, откуда
Нетрудно показать, что
Формулы (5) и (6) и выражают правило отрезков (или рычага). Это правило используют при определении фазового состояния сплава в двухфазной области. Отметим, что, в отличие от правила фаз, применимого только к равновесным состояниям, правило отрезков, как следствие из закона сохранения массы, применимо к любым системам, в том числе и далеким от термодинамического равновесия. Под фазовым состоянием сплава будем понимать совокупность четырех характеристик: − число фаз (в двухфазной области равно 2), − природа фаз (твердый или жидкий раствор, соединение и т. д.), − состав каждой из фаз (т.е. концентрации компонентов в фазе), − соотношение между количествами (долями) фаз. Правило отрезков позволяет определить две последних характеристики фазового состояния сплава в любой точке двухфазной области диаграммы состояний. Для этого через нужную конфигурационную точку проводят горизонтальную линию до пересечения с линиями, ограничивающими данную область. Эта линия называется конодой. Проекции точек пересечения коноды с границами двухфазной области на ось концентраций показывают составы фаз. Так, на рис. 4 сплав, содержащий примерно 38 % компонента В, при температуре, соответствующей конфигурационной точке а, состоит из двух фаз – жидкого и твердого растворов. Состав жидкой фазы определяется проекцией на ось концентраций точки b: 20 % компонента В (и соответственно 80 % компонента А). Состав твердого раствора определяется проекцией точки с, т.е. примерно 63 % В (37 % А). Отрезки коноды между заданной конфигурационной точкой и ее концами, обратно пропорциональны количествам этих фаз. Доля фазы в сплаве определяется отношением длины отрезка коноды, противолежащего области этой фазы, к длине всей коноды. Так, для выбранного сплава в точке а количество жидкой фазы равно ac/bc, количество твердой фазы равно ba/bc.
Во всем интервале кристаллизации из жидкого сплава, имеющего исходную концентрацию К, выделяются кристаллы, более богатые тугоплавким компонентом. Состав первых кристаллов определится проекцией точки s. Закончиться кристаллизация сплава К должна в точке 2, когда последняя капля жидкости, имеющая состав, определяемый проекцией точки l, затвердеет. Отрезок, показывающий количество твердой фазы, равняется нулю в точке 1, когда только началась кристаллизация, и количеству всего сплава в точке 2, когда кристаллизация закончилась. Таким образом, можно говорить, что состав жидкости при кристаллизации выбранного сплава изменяется по кривой 1-l, a состав кристаллов – по кривой s-2, и в момент окончания кристаллизации состав кристаллов такой же, как и состав исходной жидкости.
|
|||||||||
|
Последнее изменение этой страницы: 2017-02-10; просмотров: 339; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.71.142 (0.005 с.) |

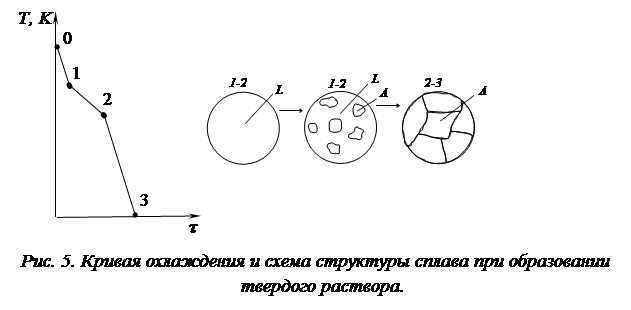



 Рассмотрим процесс охлаждения одного из сплавов рассматриваемой системы, линия сплава которого изображена на рис. 4 штриховой линий. На рис. 5 изображены кривая охлаждения такого сплава и схема его микроструктуры на разных этапах процесса охлаждения. Точка 1 соответствует началу кристаллизации (температура ликвидус), точка 2 – ее концу (температура солидус). Между точками 1 и 2 (т.е. между линиями ликвидус и солидус) сплав находится в двухфазном состоянии. При двух компонентах и двух фазах система моновариантна, т.е. при изменении температуры изменяется и состав фаз, т.е. концентрация компонентов в фазах: каждой температуре соответствуют строго определенные (но отличающиеся друг от друга) составы обеих фаз.
Рассмотрим процесс охлаждения одного из сплавов рассматриваемой системы, линия сплава которого изображена на рис. 4 штриховой линий. На рис. 5 изображены кривая охлаждения такого сплава и схема его микроструктуры на разных этапах процесса охлаждения. Точка 1 соответствует началу кристаллизации (температура ликвидус), точка 2 – ее концу (температура солидус). Между точками 1 и 2 (т.е. между линиями ликвидус и солидус) сплав находится в двухфазном состоянии. При двух компонентах и двух фазах система моновариантна, т.е. при изменении температуры изменяется и состав фаз, т.е. концентрация компонентов в фазах: каждой температуре соответствуют строго определенные (но отличающиеся друг от друга) составы обеих фаз.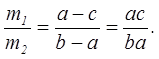 (5)
(5) и
и  (6)
(6)


