
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Требуемое количество пропана на сжигание
Горение пропана протекает по реакции
Предположим, что для достижения температуры в зоне реакции 6500С необходимо сжечь х кмоль пропана. 1) теплоемкости продуктов горения пропана при 6500С
2) физическое тепло продуктов Q = n*c*t
åQФ = 554306*х (По соотношению О2 и N2 в воздухе на 1 кмоль О2 приходится 3,76 кмоль N2) По справочным данным горение 1 кмоль С3Н8 сопровождается выделением 2223000 кДж тепла. На основании этих данных определяется, какое количество пропана необходимо сжечь, для того, чтобы в зону реакции дополнительно подать 2853244,1 кДж (см. табл. теплового баланса основной реакции) х*2223000 = 2853244,1 + 554306*х х = 1,7 Состав продуктов
Состав продуктов СО – 10,6%об Н2 – 24,8%об СО2 – 18,0%об Н2О(Г) - 24,0%об N2 – 22.6%об Изменение энергии Гиббса системы DG = DH - T*DS Значение энтропии веществ
SCO = 151,2 Дж/моль*град
Изменение энтропии реакции DS = 3*151,2 + 7*130,6 – 269,6 – 3*188,74 = 531,98 Дж/моль*град Изменение энергии Гиббса системы при 650°С (923 К) DG = 497920 – (923*531,98) = -6902,46 кДж/кмоль При 6500С протекание реакции на вызывает затруднений.
Некоторые константы наиболее употребляемых газов [1]
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-09; просмотров: 153; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.220.64.128 (0.008 с.) |
 С3Н8 + 5О2 3СО2 + 4Н2О(Г) - DН
С3Н8 + 5О2 3СО2 + 4Н2О(Г) - DН = 46,0 кДж/кмоль*град
= 46,0 кДж/кмоль*град = 36,3 кДж/кмоль*град
= 36,3 кДж/кмоль*град = 30,3 кДж/кмоль*град
= 30,3 кДж/кмоль*град = 3х*46,0*650 = 89700*х
= 3х*46,0*650 = 89700*х = 4х*36,3*650 = 94380*х
= 4х*36,3*650 = 94380*х
 = 5*3,76х*30,3*650 = 370266*х
= 5*3,76х*30,3*650 = 370266*х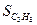 = 269,9 Дж/моль*град
= 269,9 Дж/моль*град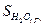 = 188,74 Дж/моль*град
= 188,74 Дж/моль*град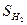 = 130,6 Дж/моль*град
= 130,6 Дж/моль*град
 * Для равновесного состояния 2NO2 N2O4
* Для равновесного состояния 2NO2 N2O4


