
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Диаграммы состояния двойных сплавовСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
В процессе охлаждения (нагревания) или при изменении концентрации какого-либо компонента в сплавах происходят фазовые и структурные изменения. Эти изменения можно проследить с помощью диаграмм состояния, представляющих графическое изображение состояния сплавов в зависимости от температуры и концентрации. Фазовые диаграммы строятся для равновесного состояния с минимумом свободной энергии системы, которое достигается при достаточно медленном охлаждении (или нагревании), что на практике трудно реализовать. При быстром охлаждении (нагреве) система может остановиться на промежуточном (метастабильном) уровне. Структура неустойчива и при соответствующих условиях может вернуться в равновесное состояние. Диаграммы состояния позволяют прогнозировать фазовые и структурные изменения в сплавах и в метастабильном состоянии. Закономерности сосуществования равновесных фаз определяются правилом фаз: c = k – f + 2, где k – число компонентов, f – число фаз, c – число степеней свободы (вариантность системы), т. е. число внутренних и внешних факторов (температура, давление, концентрация), которые можно изменять без изменения количества фаз в системе. При c = 1 возможно изменение одного из факторов в некоторых пределах, без изменения числа фаз. При c = 0 внешние факторы нельзя изменить без изменения числа фаз. Если превращения происходят при постоянном давлении, то число переменных уменьшается, (единица учитывает изменение температуры): c = k – f + 1. Изменяя соотношение компонентов, получают сплавы, имеющие свою структуру и свойства, температуру плавления и затвердения. Диаграмма состояния сплавов с полной нерастворимостью компонентов в твердом состоянии (диаграмма I рода) Сначала получают термические кривые охлаждения сплавов. Соединив точки начала и конца кристаллизации сплавов (рис. 2.3), получают диаграмму состояния (рис. 2.4). Линия на диаграмме, выше которой сплавы находятся только в жидком состоянии, называется ликвидус – геометрическое место точек температур начала кристаллизации (Т н). Линия солидус – геометрическое место точек температур конца кристаллизации (Т к). Ниже сплавы находятся только в твердом состоянии. Строение сплавов механической смеси компонентов показано на рис. 2.5.
Чистые компоненты и эвтектический сплав Э кристаллизуются при постоянной температуре (точки О, P и C на диаграмме). Эвтектический сплав соответствует концентрации компонентов А и B в точке C. Механическая смесь двух кристаллов, одновременно кристаллизующихся из жидкости при самой низкой и постоянной температуре, называется эвтектикой: Э = А + B (рис. 2.5,б). Линия, на которой в сплавах образуется эвтектика, – линия эвтектического превращения.
Число фаз и их концентрацию в любой точке двухфазной области диаграммы можно определить, используя правило отрезков. При охлаждении сплава I на линии CP (рис. 2.4) образуются кристаллы компонента В. Состав жидкости изменяется (обогащается компонентом А), достигая эвтектической концентрации на линии CN. 1. Чтобы определить процентное соотношение компонентов A и B в сплаве I в точке Е (рис. 2.4), необходимо через эту точку опустить перпендикуляр на основную ось концентраций. Проекция точки Е – точка Е 1. Отрезок АВ определяет общее количество сплава (100 %), отрезок АЕ 1 – количество компонента В (85 %), отрезок Е 1 В – количество компонента А (15 %). Сплав I в точке Е имеет двухфазную структуру: жидкая фаза Ж и кристаллы чистого компонента В. 2. Чтобы определить количество фаз в точке Е, необходимо через эту точку провести изотермическую линию (коноду). Первые точки пересечения конноды с линиями диаграммы (D и F) определяют присутствующие фазы. Количественная масса фаз обратно пропорциональна отрезкам проведенной конноды. Общее количество сплава Q = Q ж + Q тв определяется отрезком DF (принимается за 100 %). Количество твердой фазы Q тв Для проверки количественного соотношения фаз необходимо понизить температуру сплава. Точка Е опускается до точки Е ¢. Соотношение отрезков изменяется. Количество всего сплава определяет отрезок D¢F¢ (принимается за 100 %), количество твердой фазы – отрезок D¢Е¢ (55 %), жидкой – отрезок ЕF (45 %). В процессе кристаллизации количество твердой фазы увеличивается, жидкой – уменьшается. 3. Для определения состава фаз при температуре, соответствующей точке Е, из точек пересечения коноды с линиями диаграммы D и F опускаются перпендикуляры на основную ось концентраций. Проекция точки D точка D 1 покажет состав жидкой фазы Ж. Отрезок АВ – 100 %, отрезок АD 1 – 70 % компонента В, отрезок D 1 B – 30 % компонента А. Состав жидкости: Ж = 70 % В + 30 % А. Проекция точки F точка F 1 покажет состав твердой фазы. Точка F 1 на диаграмме совпадает с точкой В, которая соответствует чистому компоненту В – 100 %, при этом количество компонента А – 0 %. Состав твердой фазы сплава: 100 % В + 0 % А. Для сплавов механических смесей компонентов характерна ликвация (химическая неоднородность). При медленном процессе кристаллизации в нижней части слитка преобладают кристаллы с большим удельным весом. Чтобы предотвратить ликвацию применяют ускоренное охлаждение слитка, механическое перемешивание, вибрацию и т. д. Примеры сплавов с полной нерастворимостью компонентов – Al–Si, Pb–Sb. Диаграмма состояния сплавов с полной растворимостью компонентов в твердом состоянии (диаграммаII рода) Количество компонентов k = 2 (химические элементы А, В). Число фаз f = 2 (кристаллы a-твердого раствора, жидкая фаза). Линия АаВ – ликвидус, АбВ – солидус.
Число фаз и их соотношение. Через выбранную точку (m) проводят изотерму (коноду) до пересечения с линиями диаграммы ликвидус и солидус. Состав жидкой (твердой) фаз определяется проекциями точек пересечения изотермы с линией ликвидус (солидус) на ось концентрации. Состав жидкой фазы изменяется по линии ликвидуса, твердой – по линии солидуса. С понижением температуры состав фаз изменяется в сторону уменьшения содержания компонента В и увеличения содержания компонента А. Соотношение жидкой и твердой фаз. Количественная масса фаз обратно пропорциональна отрезкам проведенной коноды. Количество всего сплава (Q) определяет отрезок (pq),твердой фазы (Q тв) – отрезок (mp), прилегающий к линии ликвидус, жидкой (Q ж) – отрезок (mq), прилегающий к линии солидус: Q тв Неравновесная кристаллизация. Линия (Вn'nq'б') на рис. 2.6 – линия неравновесного солидуса. При неравновесной кристаллизации, при температуре соответствующей точке n',будут выделяться кристаллы a-твердого раствора. Состав твердой фазы будет соответствовать точке n', лежащей на линии равновесного солидуса. При температуре, соответствующей точке n,концентрациякристаллов a-твердого раствора отличается от равновесной. В сплаве содержится некоторое количество жидкой фазы: Q ¢ж
Диаграмма состояния сплавов с эвтектическим превращением встречается в составе сложных диаграмм распространенных промышленных сплавов (Fe–C, Al–Cu). Количество компонентов k = 2 (А и B). Число фаз f = 3: жидкая фаза и кристаллы a- и b-твердых растворов. Линии и точки диаграммы. Линия ликвидус – GCH, солидус – GEDH. Точки E и N указывают предельную постоянную растворимость a-твердого раствора, точки D и F – предельную переменную растворимость b-раствора. Сплавы системы Компоненты А и B образуют твердые растворы слева от линии EN (a-раствор) и справа от линии DF (b-раствор). Процесс аналогичен тому, который происходит в сплавах с диаграммой состояния II рода. Выше линии солидус в областях диаграммы GEC и CDH все сплавы имеют двухфазную структуру: (a+Ж) и (b+Ж). Точка С – эвтектическая точка. Линия EСD – линия, в пределах которой протекает эвтектическое превращение аналогично тому, как это имеет место на диаграммах состояния I рода. Отличие в том, что в данном случае эвтектика состоит механической смеси a- и b-твердых растворов, а не механической смеси кристаллов А и B. Кристаллизация доэвтектических сплавов (между точками С и Е) начинается с выделения кристаллов a-твердого раствора и заканчивается эвтектической реакцией: a+Ж®a+Э(a+b).
Диаграмма состояния сплавов с устойчивым химическим соединением компонентов (диаграмма IV рода). Компоненты сплава при определенном соотношении вступают в реакцию и образуют химическое соединение типа АmBn с собственной кристаллической решеткой (рис. 2.9). На диаграмме появляется вертикальная линия. Точка С соответствует температуре плавления химического соединения. Если АmBn обозначить как компонент С, то вертикальная линия разбивает диаграмму на две части. Левая часть – диаграмма с полной нерастворимостью компонентов, правая – с ограниченной растворимостью компонента С в решетке В, в которой b-фаза является твердым раствором химического соединения в решетке компонента В.
На рис. 2.10,а показана диаграмма состояния, когда оба компонента обладают полиморфизмом. Компонент А кристаллизуется с образованием a-решетки при температуре А a, которая при температуре А b меняется на b-решетку. Аналогичное превращение происходит с компонентом В. На рис. 2.10,б приведена диаграмма состояния для сплава, в которой только компонент А обладает полиморфизмом. Низкотемпературные фазы на диаграммах выделяются из твердого раствора, но закономерности формирования структуры сплава те же, что и при кристаллизации из жидкости. Зародыши новой фазы образуются и растут до полного завершения фазового превращения. Механическая смесь, состоящая из одновременно выделяющихся из a-твердого раствора в точке Д кристаллов b- и g-твердых растворов (рис. 2.10,в), называется эвтектоидом. Правила Курнакова Н.С. Если известны свойства чистых компонентов и вид диаграммы состояния для этой системы сплавов, то можно предсказать свойства любого сплава данной системы (см. рис. 2.11). 1. В твердых растворах с неограниченной растворимостью свойства сплавов изменяются по криволинейной зависимости. Механические и электрические свойства будут значительно отличаться от свойств чистых компонентов.
3. В твердых растворах с ограниченной растворимостью в интервале концентраций, отвечающих однофазным твердым растворам, свойства изменяются по криволинейному закону, в двухфазной области – по линейному закону. Крайние точки отражают свойства чистых фаз, предельно насыщенных твердых растворов, образующих данную смесь. 4. При образовании химических соединений точка концентрации компонентов соответствующих химическому соединению отвечает максимуму на кривой.
|
||
|
Последнее изменение этой страницы: 2017-02-08; просмотров: 3783; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.01 с.) |


 Анализ диаграммы состояния. Количество компонентов k = 2: химические элементы А, B. Число фаз f = 3: кристаллы А и B, жидкая фаза Ж. Линия солидус MN параллельна оси концентраций. Ветви ликвидуса ОC и CР пересекаются в точке эвтектики C, состав сплава, соответствующий этой точке, называют эвтектическим.
Анализ диаграммы состояния. Количество компонентов k = 2: химические элементы А, B. Число фаз f = 3: кристаллы А и B, жидкая фаза Ж. Линия солидус MN параллельна оси концентраций. Ветви ликвидуса ОC и CР пересекаются в точке эвтектики C, состав сплава, соответствующий этой точке, называют эвтектическим. Сплавы системы.
Сплавы системы. Кристаллизация доэвтектических сплавов начинается на линии ликвидуса с образования зародышей кристаллов А. По мере их роста жидкая фаза обедняется компонентом А. При охлаждении до температуры, соответствующей линии диаграммы MN, состав жидкой фазы изменяется по ветви ликвидуса OC до эвтектического. На линии MC происходит одновременная кристаллизация компонентов А и B (эвтектики). Структура сплава: кристаллы А +Э (рис. 2.5,а). Кристаллизация заэвтектических сплавов подобна кристаллизации доэвтектических. Структура: кристаллы В +Э (рис. 2.5,в).
Кристаллизация доэвтектических сплавов начинается на линии ликвидуса с образования зародышей кристаллов А. По мере их роста жидкая фаза обедняется компонентом А. При охлаждении до температуры, соответствующей линии диаграммы MN, состав жидкой фазы изменяется по ветви ликвидуса OC до эвтектического. На линии MC происходит одновременная кристаллизация компонентов А и B (эвтектики). Структура сплава: кристаллы А +Э (рис. 2.5,а). Кристаллизация заэвтектических сплавов подобна кристаллизации доэвтектических. Структура: кристаллы В +Э (рис. 2.5,в). – отрезок DЕ, прилегающий к линии ликвидус (40 %). Количество жидкой фазы Q ж
– отрезок DЕ, прилегающий к линии ликвидус (40 %). Количество жидкой фазы Q ж  – отрезок ЕF, прилегающий к оси ординат (60 %).
– отрезок ЕF, прилегающий к оси ординат (60 %).
 Сплавы системы. Чистые компоненты кристаллизуются при постоянных температурах. Кристаллизация любого сплава начинается на линии ликвидуса (рис. 2.6, точка а) с образования зародыша a-твердого раствора, обогащенного тугоплавким компонентом В. При понижении температуры до точки (б) количество жидкой фазы уменьшается, твердой – увеличивается. За счет процессов диффузии состав этих фаз постоянно изменяется. Периферийная часть растущего зерна обогащена легкоплавким компонентом А, а центральная компонентом В, что приводит к внутрикристаллической (дендритной) ликвации. Кристаллизация заканчивается в точке (б) на линии солидус. Строение сплавов с полной растворимостью компонентов показано на рис. 2.7. Примеры сплавов – системы Cu–Ni, W–Nb, V–Mo.
Сплавы системы. Чистые компоненты кристаллизуются при постоянных температурах. Кристаллизация любого сплава начинается на линии ликвидуса (рис. 2.6, точка а) с образования зародыша a-твердого раствора, обогащенного тугоплавким компонентом В. При понижении температуры до точки (б) количество жидкой фазы уменьшается, твердой – увеличивается. За счет процессов диффузии состав этих фаз постоянно изменяется. Периферийная часть растущего зерна обогащена легкоплавким компонентом А, а центральная компонентом В, что приводит к внутрикристаллической (дендритной) ликвации. Кристаллизация заканчивается в точке (б) на линии солидус. Строение сплавов с полной растворимостью компонентов показано на рис. 2.7. Примеры сплавов – системы Cu–Ni, W–Nb, V–Mo. ; Q ж
; Q ж  .
. . При неравновесной кристаллизации сплавы затвердевают ниже равновесной температуры затвердевания.
. При неравновесной кристаллизации сплавы затвердевают ниже равновесной температуры затвердевания. Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии (диаграмма III рода) характеризует систему сплавов, образующих твердые растворы в ограниченной области составов, за пределами которой образуется механическая смесь из кристаллов твердых растворов. Диаграмма состояния представляет собой комбинацию первых двух типов диаграмм.
Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии (диаграмма III рода) характеризует систему сплавов, образующих твердые растворы в ограниченной области составов, за пределами которой образуется механическая смесь из кристаллов твердых растворов. Диаграмма состояния представляет собой комбинацию первых двух типов диаграмм. Кристаллизация заэвтектических сплавов (между точками С и D) начинается с выделения b-твердого раствора. На линии CD идет эвтектическая реакция: b+Ж®b+Э(a+b). При охлаждении сплавов от эвтектической температуры предельная растворимость атомов компонента А в решетке компонента B падает, b-твердый раствор пересыщен компонентом А. Чтобы система пришла в равновесие, излишек атомов А из b-раствора должен выделиться. Чистые компоненты не могут существовать в виде отдельной фазы. Образуется a-твердый раствор, который в b-твердом растворе располагается в виде мелкодисперсных включений. Избыточные кристаллы, выделяющиеся не из жидкости, а из твердого раствора, обозначаются aII (вторичные a-кристаллы). Выделение новой фазы – вторичная кристаллизация.
Кристаллизация заэвтектических сплавов (между точками С и D) начинается с выделения b-твердого раствора. На линии CD идет эвтектическая реакция: b+Ж®b+Э(a+b). При охлаждении сплавов от эвтектической температуры предельная растворимость атомов компонента А в решетке компонента B падает, b-твердый раствор пересыщен компонентом А. Чтобы система пришла в равновесие, излишек атомов А из b-раствора должен выделиться. Чистые компоненты не могут существовать в виде отдельной фазы. Образуется a-твердый раствор, который в b-твердом растворе располагается в виде мелкодисперсных включений. Избыточные кристаллы, выделяющиеся не из жидкости, а из твердого раствора, обозначаются aII (вторичные a-кристаллы). Выделение новой фазы – вторичная кристаллизация.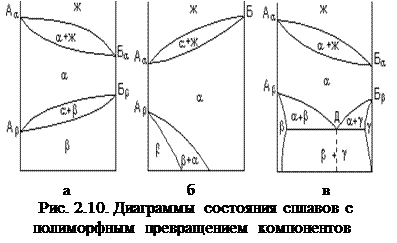 Диаграмма состояния сплавов с полиморфным превращением компонентов. Полиморфные превращения – превращения в твердом состоянии одного типа кристаллической решетки компонента в другой при изменении температуры или давления. На диаграмме полиморфные превращения проявляются в виде системы линий ниже линии солидус.
Диаграмма состояния сплавов с полиморфным превращением компонентов. Полиморфные превращения – превращения в твердом состоянии одного типа кристаллической решетки компонента в другой при изменении температуры или давления. На диаграмме полиморфные превращения проявляются в виде системы линий ниже линии солидус.






 2. Свойства механических смесей изменяются по линейному закону. Значения характеристик свойств каждого сплава находятся в интервале между характеристиками чистых компонентов.
2. Свойства механических смесей изменяются по линейному закону. Значения характеристик свойств каждого сплава находятся в интервале между характеристиками чистых компонентов.


