
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Магнезиальные вяжущие вещества
Магнезиальные вяжущие бывают: каустический магнезит и каустический доломит. Каустический магнезит получают при обжиге магнезита MgCO3 в шахтных или вращающихся печах при t = 650-8500С, при этом образуется оксид магния, который затем измельчается в порошок. Каустический доломит получают обжигом доломита с последующим измельчением в порошок. При обжиге доломита CaCO3 не разлагается, что снижает активность по сравнению с магнезитом. Магнезиальные вяжущие затворяют не водой, а водными растворами MgCl2 и MaSO4. Магнезиальные вяжущие слабо сопротивляются действию воды, их используют в местах с относительной влажностью воздуха не более 60%, на основе магнезиальных вяжущих изготавливают кальцит, фибролит и другие теплоизоляционные материалы. Кислотоупорные цементы состоят из смеси водного раствора силиката Na и К (растворимое стекло), кислотоупорного наполнителя и добавки – ускорителя твердения. В качестве наполнителя используют кварц, андезит, диабаз. Ускорителем служит кремнефтористый натрий. Вяжущим служит растворимое стекло Na2O SiO2 или K2O nSiO2, n = 2,5-3,5. Добавка кремнефтористого натрия также повышает водостойкость и кислотоупорность. Растворимое стекло получают сплавлением в стекловарочных печах в течение 7-10 ч при t = 1300-14000С кварцевого песка, измельченного и тщательно смешанного с кальцинированной содой, сульфатом натрия или потешем K2CO3. Полученную силикатную глыбу растворяют в воде при Р = 0,5-0,6 МПа и t = 1500С. Твердеет растворимое стекло на воздухе вследствие выделения и высыхания аморфного кремнезема под действием СО2: Na2SiO3 + CO2 + 2H2O → Si(OH)4 + Na2CO3. Глубина проникновения углекислоты невелика, и положительное действие наблюдается только на поверхности. Ускоряет процесс твердения кремнефтористый натрий Na2SiF6, который взаимодействует с растворимым стеклом, в результате получается гель кремневой кислоты и фторид натрия: Na2SiF6 + Na2SiO3 + 6H2O → 6NaF + 3Si(OH)4. Применение: кислотоупорные и жаростойкие обмазки. Гидравлические вяжущие Цемент стали производить в позапрошлом столетии. В начале 20-х годов 19 века Егор Челнев получил обжиговое вяжущее из смеси извести с глиной и опубликовал результаты своей работы в книге, изданной в Москве в 1825 г. В 1856 г. был пущен первый в России завод портландцемента.
Цемент является одним из важнейших строительных материалов. На его основе изготавливают бетон и ж/б и т.д. Цемент – это собирательное название группы гидравлических вяжущих веществ, главной составной частью которых являются силикаты и алюминаты кальция, образовавшиеся при высокотемпературной обработке сырьевых материалов, доведенные до частичного или полного плавления. В группу цемента входят все портландцементы, пуццолановый ПЦ, ШПЦ, глиноземистый, расширяющийся и т.д. Цемент каждого вида может при твердении развивать различную прочность, характеризуемую меркой. Выпускаются преимущественно цементы марок 300, 400, 500, 600. С повышением марки цемента возрастает эффективность его применения в бетонах за счет уменьшения удельного расхода вяжущего. Из числа цементов различных видов наиболее большое значение имеет ПЦ. Химический и минералогический (минеральный) состав клинкера Химический состав клинкера выражает содержания оксидов (% по массе). Главными оксидами являются: CaO – 63-66%, SiO2 – 21-24%, Al2O3 – 4-8%, Fe2O3 – 2-4%, суммарное количество которых составляет 96-97%. В небольшом количестве в виде различных соединений могут входить MgO, SO3, Na2O, K2O, TiO2, Cr2O3, фосфорный ангидрит P2O5. В процессе обжига, доводимого до спекания, главные оксиды образуют силикаты, алюминаты и алюмофериты кальция в виде минералов кристаллической структуры, а некоторая часть их входит в стекловидную фазу. Минералогический состав клинкера. Основными минералами клинкера являются: алит, белит, трехкальцевый алюминат, четырехкальцевый алюмоферит. Алит – 3CaO SiO2 (C3S) – 45-60%; белит – 2CaOSiO2 (C2S) – 20-30%; трехкальциевый алюминат – 3CaOAl2O3 (C3A) – 4-12%; четырехкальциевый алюмоферит – 4CaOАl2O3Fe2O3 (C4AF) – 10-20%. Зная свойства клинкерных минералов и минералогический состав клинкера, можно в первом приближении выявить основные особенности цемента, полученного из этого клинкера. Алит C3S – самый важный минерал клинкера, определяющий быстроту твердения, прочность и другие свойства. Алит представляет собой твердый раствор трехкальциевого силиката и небольшого количества (2-4%) MgO, Al2O3, P2O5, Cr2O3 и других примесей, которые могут существенно влиять на структуру и свойства. Кристаллы алита обычно имеют шестиугольную или прямоугольную форму.
Алит химически очень активен в реакции с водой, за трое суток выделяет 75-80% от всего тепла гидратации. Он обладает особенностью быстро твердеть и при твердении развивает большую прочность. Поэтому высокомарочные и быстротвердеющие цементы должны содержать большое количество алита. Белит C2S – второй по важности силикатный минерал клинкера. Он значительно менее активен (тепловыделение за 3-е суток – 10%). Твердеет медленно, но достигает высокой прочности при длительном твердении ПЦ. Белит в клинкере представляет собой твердый раствор β-C2S и небольшого количества (1-3%) Al2O3, Fe2O3, MgO, Cr2O3 и др. Регулируя скорость охлаждения клинкера, получают белит в виде округлых плотных кристаллов. Трехкальциевый алюминат C3A – в клинкере при благоприятных условиях обжига, получают в виде кубических кристаллов, образует твердые растворы сложного состава. C3A очень быстро гидратируется (за 3-е суток выделяет не менее 80% тепла гидратации) и твердеет, но имеет небольшую прочность. C3A является причиной сульфатной коррозии бетона, поэтому его содержание в ПЦ ограничено 5%. Четырехкальциевый алюмоферит C4AF в клинкере представляет собой твердый раствор алюмоферитов кальция разного состава. По скорости гидратации минерал занимает промежуточное положение между алитом и белитом, поэтому он не оказывает определяющего влияния на скорость твердения и тепловыделение ПЦ, но придает ему ударную вязкость. Клинкерное стекло присутствует в промежуточном веществе в количестве 5-15%, оно состоит в основном из CaO, Al2O3, Fe2O3, MgO, K2O, Na2O. MgO присутствует также в свободном состоянии в виде кристаллов периклаза – медленно гидратируется в течение нескольких лет, и переход в Mg(OH)2 сопровождается увеличением объема твердой фазы в уже затвердевшем цементном камне. При содержании MgO более 5% это явление может явиться причиной неравномерности изменения объема и растрескивания бетона. CaOСВ находится в свежеобожжонном клинкере в виде зерен, его содержание не должно превышать 1%. При более высоком содержании CaOСВ снижается качество цемента, и может появиться неравномерное изменение его объема при твердении, связанное с переходом СаО в Ca(OH)2. Щелочи (Na2O, K2O) входят в алюмоферитную фазу клинкера, а также присутствуют в цементе в виде сульфатов. Содержание щелочей в ПЦ ограничивается в случае применения заполнителя (песка, гравия), содержащего реакционноспособные модификации SiO2, из-за опасности растрескивания бетона в конструкции. Портландцемент называют гидравлическое вяжущее вещество, в составе которого преобладают силикаты кальция (70-80%). ПЦ – продукт тонкого измельчения клинкера с добавкой гипсового камня (3-5%). Клинкер представляет собой зернистый материал, получаемый обжигом до спекания (при t = 14500С) сырьевой смеси, состоящей в основном из известняка, глины. Добавка гипсового камня регулирует сроки схватывания ПЦ. Все свойства ПЦ определяются качеством клинкера, поэтому в свою очередь зависят от химического и минералогического состава. Основы производства. Основным сырьевым материалом для производства клинкера служат известняки с высоким содержанием СаСО3 (мел, мергель, плотный известняк) и глинистые породы (глины, глинистые сланцы), содержащие SiO2, Al2O3, Fe2O3. Примерное соотношение между карбонатными и глинистыми составляющими сырьевой смеси 3:1 (т.е. ~ 75% известняка и 25% глины). В сырьевую смесь вводят также корректирующие добавки, регулирующие температуру спекания смеси и кристаллизацию минералов клинкера. Для повышения SiO2 вводят в сырьевую смесь трепел, опоку. Для Fe2O3 - колчеданные огарки.
Для производства ПЦ все шире начинают использовать отходы промышленности. Для обжига в качестве топлива наиболее распространен газ, хотя есть и печи, работающие на мазуте. Стоимость топлива ~ 25% себестоимости цемента. Производство ПЦ – сложный технологический процесс, включающий следующие операции: 1) добыча сырья в карьере и доставка его на завод; 2) приготовление сырьевой смеси; 3) обжиг сырьевой смеси до спекания – получение клинкера; 4) помол клинкера с добавками; 5) магнезирование готового продукта. 2 Приготовление сырьевой смеси состоит в тонком измельчении и смешении взятых в установленном соотношении компонентов, что обеспечивает полноту прохождения химических реакций между ними и однородность клинкера. Приготовление сырьевой смеси осуществляется сухим, мокрым и комбинированным способами. Сухой способ заключается в измельчении и тесном смешении сухих (или предварительно высушенных сырьевых материалов), поэтому сырьевая смесь получается в виде минерального порошка, называемого сырьевой мукой. Тонкое измельчение совместно известняка и глины осуществляют в трубных (шаровых) мельницах, которых совмещаются помол и сушка материалов до остаточной влажности 1-2%. Сырьевую муку направляют в силосы, в них корректируется состав сырья и содержится запас, необходимый для бесперебойной работы печей. При сухом способе производства затраты тепла на обжиг в 1,5-2 раза меньше, чем при мокром. Сухой способ наиболее выгоден при использовании известняка и глины с повышенной влажностью (10-15%), однородного состава. Мокрый способ применяют, если мягкое сырье (мел, глина) имеют значительную влажность. Тонкое измельчение и смешение исходных материалов осуществляется в водной среде, поэтому сырьевая смесь получается в виде жидкотекучей массы – шлама с большим содержанием воды (35-45%). Глина перерабатывается в водную суспензию в глиноболтушках. Известняк после дробления направляется на совместный помол с глиняным шламом в шаровую мельницу через дозаторы непрерывного действия, что позволяет выдерживать точное соотношение между компонентами сырьевой смеси. Помол сырья производят до остатка на сите 008 не более 8-10%, следовательно, 90% частиц шлама имеют размер менее 80 мм.
Из трубных мельниц известняково-глиняный шлам перекачивается в горизонтальные, а затем в вертикальные шлам-бассейны. В них усредняется и корректируется состав. Основной недостаток – высокая энергоемкость получения клинкера. Комбинированный способ заключается в том, что приготовленный шлам до поступления в печь обезвоживается на специальных установках. Это дает возможность на 20-30% снизить расход топлива при обжиге по сравнению с мокрым. Но при этом возрастает расход электроэнергии на приготовление сырья, энергоемкость в целом высокая. 3 Обжиг при любом способе производства осуществляется во вращающихся печах. Вращающаяся печь представляет собой длинный цилиндр, сваренный из листовой стали с огнеупорной футеровкой. Длина печей 95-185-230 м, диаметр 5-7 м. Для улучшения теплообмена внутри печей ближе к верхнему (холодному) концу устраивают цепные завесы, устанавливают теплообменники различной конструкции. Вращающиеся печи работают по принципу противотока. Сырье в виде порошка или шлама подается в печь со стороны верхнего конца, а со стороны нижнего конца вдувается топливо, сгорающее в виде факела на протяжении 20-30 м. Горячие газы поступают навстречу сырью. Сырье занимает только часть речи по поперечному сечению. При вращении печи со скоростью 1-2 об/мин сырье медленно движется к нижнему концу, проходя различные температурные зоны. По Юнгу, разработавшему основы обжига, условно разделяют печь на 6 зон. I зона испарения (сушки). Происходит высушивание поступившего сырья при постепенном повышении t с 70-800С до 2000С. Подсушенный материал комкуется при перекатывании комья распадаются на более мелкие гранулы. II зона подогрева. В этой зона при постоянном нагревании сырья с 200 до 7000С сгорают находящиеся в нем органические примеси, из глинистых материалов, удаляется кристаллизационная вода (t = 450-5000С), и образуется каолиновый ангидрит Al2O3 2SiO2 и другие подобные соединения. III зона кальцинирования. При t = 700-11000С завершается процесс диссоциации карбонатов кальция и магния, и появляется значительное количество свободного оксида кальция. Этот процесс – эндотермический, идущий с большим поглощением тепла, поэтому потребление тепла в этой зоне наибольшее. В этой зоне происходит распад дегидратированных минералов на оксиды SiO2, Al2O3, Fe2O3. IV зона экзотермических реакций (е = 1100-12500C). Здесь происходят твердофазовые реакции между СаО и другими оксидами. В результате этих реакций, происходящих в твердом состоянии, образуются: 3CaOAl2O3 – трехкальциевый алюминат, 4CaOАl2O3Fe2O3 – четырехкальциевый алюмоферит и 2CaOSiO2 (белит) – двухкальциевый силикат. Эти реакции сопровождаются выделением большого количества тепла.
V зона спекания (1300-1450-13000С). Температура обжигаемого материала достигает наивысшего значения (14500С), необходимого для частичного плавления материала и образования главного минерала клинкера 3CaOSiO2 (алита) – трехкальциевого силиката. В начале спекания, начиная с 13000С, образуется расплав из относительно легкоплавких минералов C3A, C4AF, а также MgO и легкоплавких примесей в количестве 20-30% объема обжигаемой массы. При повышении температуры до 14500С в клинкерной жидкости растворяются С2S и CaO, из них в расплаве происходит процесс образования C3S, проходящий почти до полного связывания СаО. Алит плохо растворяется в расплаве и вследствие этого выделяется из него в виде мелких кристаллов, что влечет растворение в расплаве новых порций C2S и СаО. Процесс образования алита заканчивается за 15-20 мин пребывания материала в зоне спекания. Т.к. при вращении печи частично расплавленный материал непрерывно перекатывается, создаются условия для слипания мелких частичек в более крупные гранулы. Понижение температуры до 13000С вызывает кристаллизацию из расплава C3A, C4AF, C2S и MgO в идее периклаза. VI зона охлаждения. Температура клинкера понижается с 1300 до 10000С. Здесь полностью формируется его структура и состав, включающий алит, белит, C3A, C4AF, MgO, стекловидную фазу и второстепенные составляющие. Цементный клинкер выходит из печи в виде мелких гранул темно-серого или зеленовато-серого цвета. По выходе из печи клинкер интенсивно охлаждается с 1000 до 100-2000С в барабанных, рекуперативных и т.д. холодильниках воздухом, идущим навстречу клинкеру или просасыванием его через слой горячего клинкера. После этого клинкер выдерживается на складе 1-2 недели. Резкое охлаждение клинкера необходимо для стабилизации β-C2S и недопущения его перехода в 4 Помол клинкера в тонкий порошок производится преимущественно в трубных (шаровых) мельницах, работающих по открытому или замкнутому циклу. Трубная мельница представляет собой стальной барабан, облицованный внутри стальными броневыми плитами и разделенный дырчатыми перегородками на 2-4 камеры. Материал в трубных мельницах измельчается под действием загруженных в барабан мелющих тел – стальных шаров (в камере грубого помола) и цилиндров - цильпипсов (в камерах тонкого помола). При вращении мельницы мелющие тела поднимаются на некоторую высоту и падают, дробя и истирая зерна материала. При помоле к клинкеру добавляют гипс (так, чтобы общее содержание SO3 в цементе было не более 3,5%), служащий для замедления схватывания ПЦ. Готовый ПЦ – очень тонкий порошок темно-серого или зеленовато-серого цвета, по выходе из мельницы он имеет высокую температуру t = 80-1200С и направляется пневмотранспортом для хранения в силосы емкостью 4000-10000 т. В силосах цемент выдерживают до его охлаждения и гашения остатков свободного СаО, которое происходит под действием влаги воздуха. Из силосов ПЦ погружается в цементовозы или пакуется в упаковочные мешки по 50 кг.
Теория твердения Теория твердения ПЦ развивается на базе основополагающих работ Ле-Шателье, Михаэлиса, А.А. Байкова, Ребиндера и других. Цементное тесло, приготовленное путем смешивания цемента с водой имеет три периода твердения. В начале, в течение 1-3 ч после затворения цемента водой, оно пластично и легко формуется. Потом наступает схватывание, заканчивающееся через 5-10 ч после затворения, в это время цементное тесто загустевает, утрачивает подвижность, но его механическая прочность невелика. Переход загустевшего цементного теста в твердое состояние означает конец схватывания и начало твердения, которое характерно заметным возрастанием прочности. Твердение бетона при благоприятных условиях длится годами. Химические реакции. Сразу после затворения цемента водой начинаются химические реакции. Уже в начальной стадии процесса гидратации происходит быстрое взаимодействие алита с водой с образованием гидросиликата кальция и его гидроксида. 2(3CaO SiO2) + 6H2O → 3CaO 2SiO2 3H2O + 3Ca(OH)2 После затворения Са(ОН)2 образуется из алита, т.к. белит гидратируется значительно медленнее алита с образованием значительно меньшего количества Са(ОН)2. 2(2CaO SiO2) + 4H2O → 3CaO 2SiO2 3H2O + Ca(OH)2 Гидросиликат кальция 3CaO 2SiO2 3H2O образуется при полной гидратации чистого C3S в равновесии с насыщенным раствором Са(ОН)2. Молярное соотношение между СаО/SiO2 в гидросиликатах, образующихся в цементном тесте, может изменяться в зависимости от состава, условий твердения и других обстоятельств. Поэтому применяется термин СSH для всех полукристаллических и аморфных гидросиликатов. Основной алюмосодержащей фазой в ПЦ является 3CaO Al2O3. Он представляет и самую активную фазу среди клинкерных минералов. Немедленно после соприкосновения с водой С3А на поверхности непрореагировавших частиц образуется рыхлый слой метастабильных (неустойчивых) гидратов – 4CaO Al2O3 19H2O и 2CaO Al2O3 8H2O. Стабильная форма – шестиводный гидроалюминат, кристаллизуется в кубической форме, образуется в результате быстро протекающей реакции: 3CaO Al2O3 + 6H2O → 3CaO Al2O3 6H2O. Для замедления схватывания при помоле добавляют небольшое количество гипса (3-5% от массы цемента). Сульфат кальция играет роль химической активной составляющей цемента, реагирующей с 3CaO Al2O3 и связывающей его в гидросульфоалюминат кальция – эттрингит в начале гидратации ПЦ. 3CaO Al2O3 + 3CaSO4 2H2O + 26H2O → 3CaO Al2O3 3CaSO4 32 H2O. В насыщенной растворе Са(ОН)2 эттрингит сначала выделяется в коллоидном тонкодисперсном состоянии, осаждаясь на поверхности частиц С3А, замедляет их гидратацию и оттягивает начало схватывания цемента. Кристаллизация Са(ОН)2 из пересыщенного раствора понижает концентрацию Са(ОН)2 в растворе, и эттрингит образуется уже в виде длинных иглоподобных кристаллов. Кристаллы эттрингита и обуславливают раннюю прочность затвердевшего цементного камня. Эттрингит, содержащий 31-32 молекулы кристаллизационной воды, занимает примерно вдвое больший объем по сравнению с суммой объемов реагирующих веществ, заполняя поры цементного камня, эттрингит повышает его механическую прочность и стойкость. Структура затвердевшего цементного камня улучшается еще и потому, что предотвращается образование в нем слабых мест в виде рыхлых гидросиликатов кальция. Эттрингит взаимодействует с С3А, оставшимся после израсходования добавки гипса, с образованием моносульфата кальция. 2(3CaOAl2O3) + 3CaO Al2O3 3CaSO4 32H2O+ 22H2O → 3(3CaO Al2O3 CaSO4 18H2O). В результате введения в ПЦ сульфата кальция гидроалюминаты кальция заменяются гидросульфоалюминатом. C4AF при взаимодействии с водой расщепляется на гидроалюминат и гидроферрит. 4CaO Al2O3 Fe2O3 + mH2O → 3CaO Al2O3 6H2O + CaO Fe2O3 nH2O. Гидроалюминат связывается добавкой гипса, как указано выше, а гидроферрит входит в состав цементного камня. Структура цементного камня В.Н. Юнг ввел представление о цементном камне, как о микробетоне, состоящим из гелевых и кристаллических продуктов гидратации цемента и многочисленных включений в виде негидратированных зерен клинкера. Основная масса новообразований при взаимодействии цемента с водой получается в виде гелевидной массы, состоящей в основном из субмикрокристаллических частичек гидросиликата кальция. Гелеподобная масса пронизана относительно крупными кристаллами Са(ОН)2. Такое своеобразное строение предопределяет специфические свойства цементного камня, резко отличающееся от свойств других материалов. Цементный камень включает: гидросиликаты кальция (гель); кристаллы Са(ОН)2, эттрингита, гидроферриты, гидроалюминаты, непрореагировавшие зерна клинкера, макро- и микропоры. Капиллярная вода, воздух, вовлеченный в камень вследствие контракции, вовлеченный в тесто при укладке и при введении воздухововлекающих добавок. Свойства цементного камня Прочность цементного камня, приготовленного из ПЦ и выдержанного в определенных условиях, зависит от пористости. Прочность и пористость связаны экспоненциальной зависимостью:
где ПО – пористость при нулевой прочности, ~ 60%; k – коэффициент пропорциональности. На практике применяют в основном бетонные смеси с В/Ц = 0,4-0,8, которые поддаются уплотнению вибрированием, поэтому пористость цементного камня реальных бетонов составляет 30-50%. На прочность цементного камня влияют: 1) минералогический состав; 2) тонкость помола. Увеличение удельной поверхности до 5000 см2/г увеличивает прочность, дальнейшее увеличение тонкости помола к росту прочности не приводит, а иногда и к снижению из-за повышения водопотребности. Тонкость помола оценивается по остатку на сите 008, и для обычного ПЦ не должна превышать 15%. Морозостойкость зависит от минералогического состава клинкера, вещественного состава ПЦ и капиллярной пористости цементного камня, понижает морозостойкость С3А, поэтому его ограничивают до 5-7 %. Добавки осадочного происхождения (трепел, диатомит) увеличивают водопотребность цементного камня и, следовательно, понижают морозостойкость. Для повышения морозостойкости вводят ПАВ. Воздухостойкость – способность цементного камня сохранять прочность в сухих условиях, при сильном нагреве солнечными лучами, а так же в условиях попеременного увлажнения и высушивания. Цементы, содержащие АМД осадочного происхождения, не только менее морозостойки, но и менее воздухостойки. Из-за дегидратации (выветривания) части воды из низкоосновных гидросиликатов кальция. Химическая стойкость. Коррозия вызывается воздействием агрессивных газов и жидкостей на составные части затвердевшего ПЦ. Встречаются десятки веществ, оказывающие влияние на цементный камень. По В.М. Московину коррозию цементного камня можно разделить на три группы: 1) разложение составляющих цементного камня, растворение и вымывание Са(ОН)2 под воздействием мягких вод, содержащих мало растворенных веществ. К ним относятся воды оборотного водоснабжения, конденсат, дождь и т.д. Наиболее растворимым компонентом цементного камня является Са(ОН)2, образующийся при гидратации С2S. При действии воды, особенно проточной, концентрация Са(ОН)2 снижается и в результате уменьшения СаО (менее 1,1 г/л) разрушаются гидросиликаты кальция и гидроалюминаты. Выщелачивание можно обнаружить по появлению белых пятен на поверхности бетона. Для борьбы с данным видом коррозии (коррозия выщелачивания) применяют ПАВ, АМД, искусственную карбонизацию, уменьшение C3S, применение белитовых цементов, повышение плотности, покрытие водоотталкивающих материалов; 2) коррозия, связанная с образованием легкорастворимых солей (коррозия обменных реакций): а) углекислотная развивается при действии на цементный камень воды, содержащей СО2: Ca(OH)2 + CO2 + H2O → CaCO3 + H2O. Избыточный оксид углерода разрушает карбонатную пленку бетона вследствие образования легкорастворимого бикарбоната кальция: CaСО3 + CO2 + H2O → Са(НСО3)2. Понижение концентрации Са(ОН)2 приводит к разложению гидросиликатов кальция. Для борьбы – повышение плотности, гидроизоляция; б) кислотная коррозия происходит при действии любых растворов кислот, кроме поликремневой и кремнефтористоводородной. Свободные кислоты встречаются в сточных водах промышленных предприятий и т.д. Кислоты взаимодействуют с гидроксидом кальция, образуя легкорастворимые соли, или образование соли связано с увеличением объема. Помимо того, кислоты разрушают CSH. Защита: покрытие кислотостойкими материалами; в) магнезиальная коррозия происходит при воздействии на Са(ОН)2 солей магния, растворенных в воде. Разрушение протекает вследствие обменных реакций: Ca(OH)2 + MgCl2 → CaCl2 + Mg(OH)2, Ca(OH)2 + MgSO4 → Mg(OH)2 + CaSO4 2H2O. Соли CaCl2, CaSO4 2H2O вымываются из бетона, а Mg(OH)2 – не растворим в воде и не обладает вяжущими свойствами; г) коррозия под действием минеральных удобрений. Особенно вредны аммиачные удобрения: Ca(OH)2 + 2NH4 NO3 + 2H2O → Ca(NO3)2 4H2O + 2NH3. Нитрат кальция растворим, а NH3 – газ. Защита: повышение плотности, гидроизоляция, АМД; 3) сульфоалюминатная коррозия возникает при действии на гидроалюминаты воды, содержащей ионы 3CaOAl2O3 6H2O + 3CaSO4 2H2O + 23H2O → 3CaOAl2O3 3CaSO4 31H2O. Образование эттрингита в порах цементного камня сопровождается увеличением объема ~ в 2 раза, что приводит к разрушению цементного камня. Защита: повышение плотности цементного камня, гидроизоляция, сульфатостойкие цементы.
|
|||||||||
|
Последнее изменение этой страницы: 2017-02-07; просмотров: 489; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.147.54.6 (0.064 с.) |
 -C2S. Также при медленном охлаждении С3S разлагается на C2S и СаО.
-C2S. Также при медленном охлаждении С3S разлагается на C2S и СаО. ,
,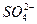 более 250 кг/л.
более 250 кг/л.


