Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Задачи с участием газовых смесей ⇐ ПредыдущаяСтр 5 из 5
11 Смесь двух газов, один из которых легче воздуха, пропущена последовательно через трубки, заполненные оксидом меди (II) (при 400 °С), оксидом фосфора (V) и твердым гидроксидом калия, нанесенными на инертный носитель и взятыми в избытке. Масса первой трубки уменьшилась на 0,192 г, а массы второй и третьей трубок возросли, соответственно, на 0,144 г и 0,088 г. После пропускания газов через трубки было получено 23,4 мл газообразного вещества, измеренного при температуре 17 °С и давлении 103 кПа. Установите объем исходной газовой смеси (при н.у.) и массовые доли газов в ней, если известно, что масса смеси составляла 0,068 г. 12 Имеется смесь азота и кислорода, которая легче воздуха. После пропускания через смесь электрического разряда при нагревании образовался оксид азота (IV) с выходом 60 %, в результате чего смесь стала тяжелее воздуха. Определите области возможных объемных концентраций азота в исходной и конечной смесях. 13 Имеется смесь оксида углерода (II) и хлора, которая на 20 % легче оксида серы (IV). После пропускания смеси над нагретым катализатором образовался фосген, в результате чего смесь стала тяжелее оксида серы (IV) при тех же условиях. Рассчитайте область допустимых значений для выхода реакции. 14 Уксусную кислоту массой 4,20 г поместили в сосуд объемом 5,70 л и нагрели до температуры 210 °С. Давление паров при этом составило 28,2 кПа. Определите число молекул димера уксусной кислоты в газовой фазе. 15 К 40 л смеси, состоящей из азота и аммиака, добавили 20 л хлороводорода, после чего плотность газовой смеси по воздуху стала равной 0,871. Вычислите объемные доли газов в исходной смеси. 16 Имеется смесь паров бензола и водорода, которая на 10 % легче неона. После пропускания смеси над нагретым до
Задачи на выход и степень превращения 17 Имеется смесь азота и водорода, которая легче гелия. После пропускания смеси над нагретым катализатором образовался аммиак с выходом 60 %, в результате чего смесь стала тяжелее гелия. Определите области возможных объемных концентраций азота в исходной и конечной смесях.
18 Плотность по пропану газовой смеси, состоящей из этилена и паров воды, до пропускания через контактный аппарат для синтеза этанола была равна 0,5, а после пропускания стала равна 0,6. Определите объемную долю паров в реакционной смеси и процент превращения этилена в этанол.
Задачи на избыток и недостаток 19 К 200 г 5,0%-ного раствора хлорида кальция добавили 20 К 200 г 10,6%-ного раствора нитрата стронция добавили 16,5 г сульфида калия. Через образовавшуюся смесь пропустили при перемешивании 2,24 л сероводорода (н.у.). Определите массу полученного осадка и массовые доли веществ в образовавшемся растворе.
Задачи на вывод формулы 21 (хим. ф-т МГУ, 1990). Образец вещества массой 1,8 г в реакции с избытком калия при комнатной температуре дает 489 мл водорода (измерено при 298 К и 101,3 кПа). При сожжении 67,5 мг того же вещества получили 99 мг оксида углерода (IV) и 40,5 мг воды. При полном испарении образца этого вещества массой 22 (олимпиада «Ломоносов-2007»). При термическом разложении 14,4 г неорганического вещества образовалось 10,08 л смеси газов (в пересчете на н.у.), имеющей плотность по гелию 6,5. После пропускания смеси над твердым оксидом кальция объем газа уменьшился в 1,5 раза. Оставшееся газообразное вещество легче воздуха. В определенных условиях оно реагирует с калием, образуя ионное соединение, содержащее 70,9 % калия по массе. Установите формулы всех перечисленных веществ и напишите уравнения всех реакций. 23 (олимпиада «Ломоносов-2007»). Массовая доля углерода в неизвестном углеводороде Х равна 94,12 %. Этот углеводород, обладающий слабыми кислотными свойствами, способен образовывать соль Y, в которой массовая доля металла составляет 76,60 %. Определите структурные формулы веществ Х и Y. Напишите уравнение превращения Х в Y и уравнение полной каталитической гидратации Х.
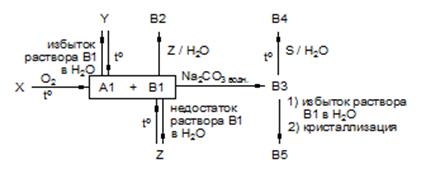
24 (олимпиада «Ломоносов-2007). При термическом разложении 18,0 г органического вещества образовалось 8,96 л смеси газов (в пересчете на н.у.), имеющей плотность по водороду 18,0. После пропускания смеси через известковую воду объем газа уменьшился вдвое. Оставшееся газообразное вещество легче воздуха. При нагревании оно реагирует с железом, образуя летучее соединение, содержащее 28,6 % железа по массе. Установите формулы всех перечисленных веществ и напишите уравнения всех реакций. 25 (41 Международная Менделеевская олимпиада). При обжиге на воздухе 100 мг вещества Х образуется 25,7 мл (н.у.) газа В1 и твердое вещество А1 массой 100 мг. Х кристаллизуется в трех модификациях, изоструктурных вюртциту (гексагональный ZnS), сфалериту (кубический ZnS) и каменной соли (NaСl) соответственно. Некоторые превращения с участием Х (любой из его модификаций) представлены на схеме:
Взаимодействие А1 и В1 протекает с образованием только Y и Z, соотношение которых в конечной смеси зависит от условий проведения реакции. Анион Y имеет более сложное строение, чем анион Z. Чтобы избавиться от последнего, смесь Y и Z можно обработать солью бария, при этом выпадает белый осадок, нерастворимый в кислотах, что служит для аналитического определения аниона Z. Любое из соединений на схеме содержит не более трех элементов в своем составе. Элементы А и В, содержащиеся в Х – Z, образуют соединения А1 и В1 – В5 соответственно. Состав анионов Y, В2, В4 и В5 отличается только числом атомов кислорода. 1. Определите состав неизвестных соединений, представленных на схеме. 2. Напишите уравнение реакций, приведенных на схеме. 3. Изобразите строение анионов Y, В2, В4, В5 и ионов, содержащих такое же число атомов В, но большое число атомов кислорода. ПРИЛОЖЕНИЕ 1
|
||||||
|
Последнее изменение этой страницы: 2017-02-06; просмотров: 789; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.136.97.64 (0.006 с.) |