
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Физиологическое действие АДГ
Вазопрессин (АДГ) действует на дистальные извитые канальцы и собирательные трубочки нефрона, усиливая реабсорбцию воды, оказывая, таким образом, антидиуретический эффект. Влияние вазопрессина (АДГ)на проницаемость эпителия собирательных трубок нефрона обусловлено наличием рецепторов к гормону, относящихся к V-2 типу, на поверхности базолатеральной (Б-Л) мембране клеток эпителия. Образование гормон-рецепторного комплекса, влечет за собой через посредство G-белка и гуанилового нуклеотида активацию аденилатциклазы и образование цАМФ у базолатеральной мембраны (рис. 4.2.2). После этого цАМФ пересекает клетку эпителия и, достигнув апикальной (А) мембраны, активирует цАМФ-зависимые протеинкиназы. Под влиянием этих ферментов происходит фосфорилирование мембранных белков, приводящее к повышению проницаемости для воды. Перестройка ультраструктур клетки ведет к образованию специализированных вакуолей, переносящих большие потоки воды по осмотическому градиенту от апикальной к базолатеральной мембране, не позволяя самой клетке набухать. Кроме того, в дистальных канальцах вазопрессин обусловливает активацию и выход из клеток гиалуронидаз, вызывающих расщепление гликозаминогликанов основного межклеточного вещества и межклеточный пассивный транспорт воды по осмотическому градиенту. Стимуляция V-1- рецепторов, локализованных в стенке кровеносных сосудов, через вторичные посредники инозитол-3-фосфат и кальций-кальмодулин вызывает сужение сосудов, отсюда и название “вазопрессин”. Этот эффект в физиологических условиях выражен слабо из-за низких концентраций гормона в крови. В больших дозах гормон вызывает сокращение кровеносных сосудов. Вазопрессин как нейропептид поступает и в ликвор, и по аксонам экстрагипоталамной системы в другие отделы мозга, что обеспечивает его участи в формировании чувства жажды и питьевого поведения, в нейрохимических механизмах памяти, запоминания и обучения (гормон памяти).
Рис. 4.2.2. Механизм действия вазопрессина (АДГ) на проницаемость собирательных трубочек для воды. Б-Л мембрана — базолатеральная мембрана клеток; А мембрана — апикальная мембрана; ГН — гуанидиновый нуклеотид; АЦ — аденилатциклаза.
Таблица 4.2.1.
Регуляция секреции АДГ Осмомолярность крови и внеклеточной жидкости является одним из жестких параметров внутренней среды. Изменение этого показателя регистрируют осморецепторы. Существование осморецепции было установлено Вернеем в 1947 году. Им показано, что интракаротидное введение гипертонических растворов сопровождается отчетливым торможением диуреза. У людей, собак, крыс была установлена строгая линейная зависимость между осмомолярностью плазмы крови и концентрацией АДГ. Сдвиги осмотического давления воспринимаются осморецепторами. Эти рецепторы расположены в сосудах печени, почек, селезенки, поджелудочной железы, некоторых мышц (периферические осморецепторы). Они воспринимают изменение осмотического давления и передают эту информацию к супраоптическому ядру гипоталамуса (центральное звено осморецепции). Помимо осморецепторов, в механизмах осмотического гомеостаза имеют значение волюморецепторы, реагирующие на изменение объема внутрисосудистой и внеклеточной жидкости. Волюморецепторы расположены во многих крупных сосудах, венах, артериях, а также в обоих предсердиях. От них информация передается к нейронам гипоталамуса и продолговатого мозга (к центру волюморегуляции). Ведущее значение в регуляции секреции АДГ имеют те волюморецепторы, которые реагируют на изменение напряжения сосудистой стенки в области низкого давления - барорецепторы, которые локализуются в афферентных артериолах почечных клубочков, в сонной артерии, дуге аорты, правом желудочке в каротидном синусе. Активация волюморецепторов, возникающая в ответ на увеличение объема жидкости, приводит к повышению экскреции солей натрия и воды.
Осморецепторы чутко реагируют на сдвиги концентраций осмотически активных веществ плазмы крови. При увеличении осмолярности плазмы крови на 1%, концентрация АДГ возрастает на 1 пг/мл (пикограмм равен миллионной доле микрограмма). Переход к состоянию максимального осмотического концентрирования мочи требует 10-кратного возрастания количества АДГ в крови.
Нейрогипофизарный механизм В условиях дефицита воды увеличивается концентрация осмотически активных веществ, увеличивается осмотическое давление, возбуждаются осморецепторы, барорецепторы и волюморецепторы, от которых информация достигает центра регуляции ионного состава, который расположен в области супраоптического ядра, где усиливается секреция АДГ. Механизм антидиуретического действия АДГ (вазопрессина) состоит в усилении обратного всасывания воды стенками собирательных трубочек нефрона. Таким образом, происходит экономия воды организмом. При избыточном содержании воды в организме, концентрация растворенных осмотически активных веществ снижается и ее осмотическое давление падает. Это уменьшает активность периферических и центральных осморецепторов, что снижает выделение АДГ из нейрогипофиза в кровь и приводит к усилению выделения воды почками (рис. 4.2.3.) Кроме того, АДГ стимулирует центр жажды, т.е. вызывает повышение поступление воды в организм, что также способствует нормализации осмотического давления. Важную роль в обеспечении осмотического гомеостаза играет: ренин-ангиотензин-альдостероновая система.
Рис. 4.2.3. Механизмы, регулирующие секрецию АДГ задней долей гипофиза
Окситоцин Синтез окситоцина в гипоталамических нейронах и его секреция нейрогипофизом в кровь стимулируется рефлекторным путем при раздражении рецепторов растяжения матки и механорецепторов сосков молочных желез. Усиливают секрецию гормона эстрогены. Основные эффекты окситоцина заключаются в стимуляции сокращения матки при родах, сокращении гладких мышц протоков молочных желез, что вызывает выделение молока, а также в регуляции водно-солевого обмена и питьевого поведения. Окситоцин является одним из дополнительных факторов регуляции секреции гормонов аденогипофиза, наряду с либерилинами. Таблица 4.2.2.
Окситоцин – антагонист АДГ и АГ. Он угнетает процессы запоминания. Доказательство: при черепно-мозговых травмах – амнезия, при этом в ликворе имеет место увеличение содержания окситоцина и снижение АДГ.
Окситоцин усиливает доверие (склонность человека доверять незнакомцу, в случае если тот посылает сигналы, не содержащие угрозы). Окситоцин составляет положительную сторону межличностного взаимодействия. Человек буквально чувствует, что ему доверяют и это мотивирует его на ответные шаги. Окситоцин усиливает сопереживание по отношению к другим людям и мотивирует наше желание помогать им. У самок млекопитающих окситоцин стимулирует заботу о потомстве, вызывает выделение дофамина в областях, связанных с таким вознаграждающим поведением как секс и принятие пищи. Уровень оситоцина резко возрастает при оргазме, чем объясняют взаимные любовные чувства. Это «гормон объятий».
Нарушения секреции АДГ От 3 до 5-% всех случаев несахарного диабета являются так называемыми первичными (идиопатическими) формами его. У 25-30 % больных развитие несахарного диабета связано с наличием первичной или вторичной опухоли в области гипоталамуса. Растущая опухоль гипофиза, сдавливая гипоталамус, также может быть причиной развития несахарного диабета. Среди первичных опухолей гипоталамуса наиболее частыми причинами заболевания являются краниофарингиома, менингиома, глиома, а также метастазы бронхогенного рака или рака молочной железы в область гипоталамуса, контролирующую секрецию вазопрессина. Недостаточность секреции вазопрессина может быть следствием перенесенного базального менингита, энцефалита, сифилиса, травмы с переломом основания черепа, аневризмы сосудов, саркоидоза, гистиоцитоза и других поражений гипоталамической области. Несахарный диабет при переломах основания черепа продолжается 7-14 дней, а после нейрохирургических операций (криохиругия, имплантация радиоактивного иттрия, гипофизэктомия) – от нескольких недель до 1 года. Основными клиническими симптомами болезни являются полиурия (экскреция большого количества мочи) полидиксия и связанное с ними нарушение сна. Выделение мочи колеблется от 5 до 20 л в сутки, ее плотность 1,001-1,003. Попытка уменьшить полиурию ограничением приема жидкости приводит к сильной жажде и дегидротации. НАДПОЧЕЧНИКИ
Надпочечники – парные органы, расположенные забрюшинно, выше и медиальнее верхних полюсов почек, иногда охватывая его наподобие шапочки (рис. 5.1). Форма и размеры надпочечников неодинаковы у различных видов и подвержены значительным возрастным изменениям. В первые дни после рождения надпочечники значительно уменьшаются в размерах и их поверхность становится складчатой. Затем они вновь начинают увеличиваться. У взрослой лошади вес одного надпочечника равен 20 г, у коровы – 15 г, у овцы – 1,4 г. У взрослого человека правый надпочечник имеет форму, напоминающую пирамиду, а левый – форму полумесяца. В среднем длина надпочечника человека достигает 45 мм, ширина – 25-30 мм, толщина – 6-10 мм, вес – 5-7 г.
Снаружи каждый надпочечник покрыт соединительнотканной капсулой. От капсулы перпендикулярно вдаются внутрь коркового слоя прослойки соединительной ткани, внутри которой проходят кровеносные сосуды и нервные волокна. Вещество железы состоит из двух слоев: коркового, составляющего 90% массы надпочечника, и мозгового слоя, находящегося в центре, в окружении коры надпочечника.
Рис. 5.1. Расположение надпочечника.
Удаление обоих надпочечников неизменно ведет к смерти, т.е. эти железы имеют витальное значение. Последствия адреналэктомии. Изменения касаются практически всех физиологических процессов. Слабость, быстрая утомляемость, гипотония, нарушения деятельности ЖКТ, ЦНС: депрессия. Резко падает сопротивляемость к травмам, инфекциям и т.д. Последствия адреналэктомии традиционно связывают с нарушениями: 1. метаболизма углеводов, белков и способностью противостоять различным стрессам; 2. с изменениями водно-солевого обмена отсутствие альдостерона → потеря Na+ с мочой → дегидратация → недостаточность периферического кровообращения → тканевая гипоксия → распад белка.
Основной признак недостаточности надпочечников – неспособность справляться с водной нагрузкой. Важно также, что при этом состоянии задерживается К+ и его концентрация во внеклеточной жидкости повышается, т.к. он выходит из клеток (из-за тканевой гипоксии), накапливаются также фосфаты и небелковый азот. Как следствие – рвота, диарея, что усиливает потерю соли и воды. Потеря соли происходит и через потовые железы, ЖКТ. Влияние минералокортикоидов на состав пота расширяет представления о значении коры надпочечников для выживания организмов в процессе эволюции, так как тепловые воздействия – мощный стимул для секреции адреналина, который задерживает выделение соли с потом. Надпочечники являются жизненно важным органом именно из-за соль-задерживающей функции. Мозговой слой надпочечников
Мозговой слой находится в центральной части надпочечника и составляет 10% его массы. Мозговое вещество образует сероватую «сердцевину» железы и состоит из групп клеток, окруженных кровеносными сосудами. Мозговой и корковый слои являются полностью разными структурами. Корковый слой имеет эктодермальное происхождение, а мозговой происходит от первичного нервного гребешка и в конечном итоге является высоко специализированной частью симпатической нервной системы.
Рис. 5.1.1. Макро- (А) и микроскопическое (Б) строение надпочечника (секреция соответствующих гормонов): 1 – капсула; 2 – клубочковая зона коры; 3 – пучковая зона коры; 4 – сетчатая зона коры; 5 – мозговое вещество; 6 – вена мозгового вещества; 7 и 8 – смещенные участки коркового вещества.
Железистые клетки мозгового вещества получили название хромаффинных или феохромных. Хромаффинные клетки содержат гранулы с электроплотным содержимым, которое с бихроматом калия дает хромаффинную реакцию. Хромаффинные клетки содержат многочисленные митохондрии, комплекс Гольджи, элементы гранулярной эндоплазматической сети, многочисленные электроноплотные гранулы, содержащие преимущественно норадреналин и/или адреналин (по этому признаку хромаффинные клетки подразделяются на две субпопуляции), а также АТФ, энкефалины и хромогранины (рис. 5.1.2). Кроме катехоламинов, гранулы содержат липиды, нуклеотиды (АТФ), белки, ионы Са2+ и Mg2+. Катехоламины хромаффинных клеток содержатся в гранулах, одетых липоидной оболочкой и заполненных мелкой зернистостью. Эти гранулы являются специфическими органоидами хромаффинной ткани, на которых протекает биосинтез катехоламиновых секреторных продуктов. В гранулах мозгового слоя надпочечников содержится 80% адреналина и 20% норадреналина. Норадреналиновые клетки расположены в центре, а адреналиновые – по периферии мозгового слоя надпочечников. Относительное содержание этих двух гормонов варьирует в зависимости от вида и от стадии развития организма. У большинства млекопитающих норадреналин преобладает до рождения и на первых стадиях неонатального периода, однако, с возрастом в количественном отношении начинает преобладать адреналин. Скорость наступления этого сдвига у различных видов различна: у человека он происходит не ранее трехлетнего возраста.
Рис.5.1.2. Строение хромаффинной клетки: 1 – просвет капилляра; 2 – пространство между капилляром и хромаффинной клеткой; 3 – хромаффинная гранула; 4 – аппарат Гольджи; 5 – митохондрия; 6 – эндоплазматическая сеть; 7 – ядро; 8 – нервное окончание.
Хромаффинные клетки — основной клеточный элемент не только мозговой части надпочечников. Мелкие скопления и одиночные хромаффинные клетки находят также в сердце, почках, симпатических ганглиях. Скопление вненадпочечниковой хромаффинной ткани на передней поверхности аорты настолько велико и постоянно, что оно получило даже особое название – орган Цукеркандля. Это так называемая экстрамедуллярная (вненадпочечниковая) хромаффинная ткань (рис. 5.1.3).
Рис. 5.1.3. Схема распределения хромаффинной ткани в организме. Вненадпочечниковая («экстрамедуллярная») ткань располагается вдоль симпатической нервной цепочки (ганглии не показаны) и вблизи сосудов брюшной полости и таза. 1 – мозговое вещество надпочечников; 2 – параганглии; 3 – хромаффинная ткань вблизи аорты.
Все хромаффинные клетки имеют общее происхождение в эмбриогенезе, возникая из нейробластов (первичных нервных клеток), расположенных главным образом в грудном отделе центральной нервной системы. Эти первичные нервные клетки мигрируют из места своего возникновения по ходу симпатических нервов. Экстрамедуллярная хромаффинная ткань секретирует, главным образом, норадренали, напоминая в этом отношении постганглионарные нейроны симпатической нервной системы. Функция хромаффинной клетки регулируется симпатической нервной системой. Морфологическая связь нервных волокон с хромаффинной клеткой различна. Нервные окончания могут просто подходить к поверхности клетки, а могут и вдавливаться в клеточную мембрану так, что оказывается более или менее окруженными ею. Однако независимо от их взаимного расположения между мембраной нервного окончания и мембраной клетки всегда есть щель шириной ≈ 150Å. Наружная пограничная мембрана этих двух компонентов на месте сближения утолщена. Таким образом, здесь формируется синапс. В пресинаптической части, образованной аксоном, расположены синаптические пузырьки, в которой находится ацетилхолин. В момент передачи возбуждения от симпатического волокна хромаффинным клеткам (например, при раздражении чревного нерва) в синаптическую щель 1) выделяется ацетилхолин, который диффундирует через узкую синаптическую щель к мембране хромаффинной клетки; 2) далее ацетилхолин взаимодействует со специфическими рецепторными участками мембраны хромаффинной клетки и активирует ее; 3) через активированную мембрану в клетку мигрируют ионы кальция, который взаимодействует с определенными реактивными участками цитоплазмы; 4) этот процесс стимулирует выделение из клетки катехоламинов и АТФ.
В связи с этим хромаффинную ткань можно рассматривать как модифицированное периферическое звено симпатической нервной системы, осуществляющее свои эффекты гуморально. Мозговой слой надпочечников и симпатическая нервная система функционируют в тесной связи друг с другом и представляют единую систему регуляции, обычно обозначаемую симпатоадреналовой.
Рис. 5.1.4. Схема нервной регуляции функций мозгового слоя надпочечников:
1 – мозговой слой надпочечника; 2 – ветвь большого чревного нерва; 3 – солнечное сплетение; 4 − вазомоторный нерв; 5 − симпатический ганглий; 6 – спинномозговой симпатический центр; 7 – симпатические центры гипоталамуса; 8 – кора больших полушарий; 9 – ретикулярная формация; 10 – рецептивное поле; 11 − сосуд.
Биосинтез катехоламинов Как надпочечниковая («медуллярная»), так и вненадпочечниковая («экстрамедуллярная») хромаффинная ткань выделяют гормоны адреналин и норадреналин, объединенных под общим названием катехоламины. Адреналин синтезируется только в надпочечниках; норадреналин и дофамин образуются также в параганглиях и многочисленных нейронах симпатической нервной системы. Эти эндокринные клетки иннервируются волокнами симпатической нервной системы. Таким образом, синтезированные в нейронах катехоламины являются нейротрансмиттерами, которые опосредуют функцию ЦНС и симпатической нервной системы. Катехоламины синтезируются из аминокислоты тирозин путем ряда превращений, регулируемых определенными энзимами, который в мозговом слое надпочечников в хромаффинных клетках под влиянием энзима тирозингидроксилазы превращается в дегидрооксифенилаланин (ДОФА) (рис. 5.1.5). Далее ДОФА под влиянием энзима декарбоксилазы превращается в дофамин, а последний гидроксилируется энзимом дофаминбетагидроксилазой в норадреналин. В окончаниях периферических симпатических нервов синтез дофамина и норадреналина – идет тем же путем и под влиянием тех же энзимов, что и в мозговом слое надпочечников и в мозге. В мозговом слое надпочечников норадреналин под влиянием энзима N-метилтрансферазы превращается в адреналин. В симпатической нервной системе (в основном, в постганглионарных окончаниях симпатических нервов) адреналин не образуется, так как энзим, необходимый для его образования (N-метилтрансфераза) имеется только в мозговом слое надпочечников.
Рис. 5.1.5. Регуляция синтеза катехоламинов в мозговом слое надпочечников.
При увеличении образования дофамина декарбоксилаза тормозит активность тирозингидроксилазы и синтез катехоламинов уменьшается. При уменьшении образования дофамина активность тирозингидроксилазы возрастает и синтез катехоламинов увеличивается. Кроме того, синтез адреналина регулируется кортизолом, который поступает вмозговой слой из кортикомедуллярного венозного синуса. Кортизол активирует энзим N-метил-трансферазу, превращающую норадреналин в адреналин. Секреция катехоламинов осуществляется путем экзоцитоза; при этом содержание гранул “изливается” во внеклеточное пространство. Высвобождение катехоламинов как из мозгового слоя надпочечников, так и из окончаний симпатической нервной системы происходит под влиянием таких физиологических стимуляторов, как стресс, физическая и психическая нагрузка, повышение уровня инсулина в крови, гипогликемия, гипотония и др. Высвобождение катехоламинов происходит при участии ионов Са2+, который поступает в клетку или в окончания симпатической нервной системы. Поступающие в кровь катехоламины достигают периферических тканей, где накапливаются или метаболизируются прямо пропорционально симпатической иннервации тканей. Механизм действия катехоламинов Адреналин и норадреналин вызывают эффекты, которые различны во многих отношениях. Эффекты катехоламинов при их воздействии, например, на сосуды различных органов, различаются (сосуды мышц – расширяются, кишечника – суживаются, коронарный кровоток под влиянии адреналина снижается, норадреналина - возрастает). Для объяснения этих эффектов была предложена теория клеточных рецепторов (Алквист, 1948). Согласно Алквисту существует 2 типа рецепторов, реагирующих с катехоламинами – α и β. α-адренэргическое действие охватывает такие быстрые эффекты, как вазоконстрикцию, сокращение капсул селезенки, матки, семявыносящих протоков, а также торможение гладкой мускулатуры ЖКТ, мочевого пузыря. Через α-адренорецепторы действует, в основном, норадреналин, адреналин значительно слабее (табл. 5.1.1).
Таблица 5.1.1.
|
|||||||||||
|
Последнее изменение этой страницы: 2017-01-26; просмотров: 931; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.9.141 (0.09 с.) |



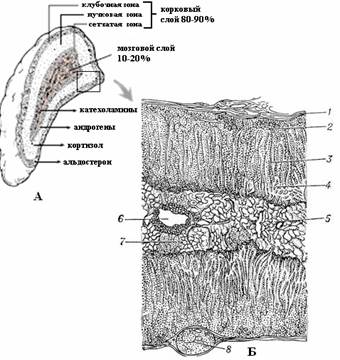 Мозговое вещество отделено от коркового вещества тонкой прерывистой прослойкой соединительной ткани (рис. 5.1.1). У мозгового и коркового вещества надпочечника имеется общее кровоснабжение. Артерии, входящие в надпочечник, разветвляются на артериолы, образующие густую субкапсулярную сеть, от которой отходят капилляры, снабжающие кровью кору. Их эндотелий фенестрирован, что облегчает поступление кортикальных стероидных гормонов из клеток коркового слоя в ток крови. Из сетчатой зоны капилляры вступают в мозговую часть, где принимают вид синусоидов и сливаются в венулы, которые переходят в венозное сплетение мозгового вещества.
Мозговое вещество отделено от коркового вещества тонкой прерывистой прослойкой соединительной ткани (рис. 5.1.1). У мозгового и коркового вещества надпочечника имеется общее кровоснабжение. Артерии, входящие в надпочечник, разветвляются на артериолы, образующие густую субкапсулярную сеть, от которой отходят капилляры, снабжающие кровью кору. Их эндотелий фенестрирован, что облегчает поступление кортикальных стероидных гормонов из клеток коркового слоя в ток крови. Из сетчатой зоны капилляры вступают в мозговую часть, где принимают вид синусоидов и сливаются в венулы, которые переходят в венозное сплетение мозгового вещества.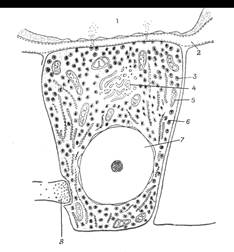

 В период интенсивной симпатической стимуляции (холод, чрезмерная физическая активность) мозговой слой надпочечников прогрессивно увеличивает секрецию катехоламинов (рис. 5.1.4.). В других ситуациях симпатическая нервная система и мозговой слой надпочечников стимулируются независимо друг от друга. Например, вертикальное положение тела стимулирует симпатическую нервную систему, а гипогликемия стимулирует только мозговой слой надпочечников. В ситуациях, когда симпатическая нервная система подавлена, мозговой слой надпочечников снабжает организм катехоламинами и поддерживает его жизненно важные функции.
В период интенсивной симпатической стимуляции (холод, чрезмерная физическая активность) мозговой слой надпочечников прогрессивно увеличивает секрецию катехоламинов (рис. 5.1.4.). В других ситуациях симпатическая нервная система и мозговой слой надпочечников стимулируются независимо друг от друга. Например, вертикальное положение тела стимулирует симпатическую нервную систему, а гипогликемия стимулирует только мозговой слой надпочечников. В ситуациях, когда симпатическая нервная система подавлена, мозговой слой надпочечников снабжает организм катехоламинами и поддерживает его жизненно важные функции.



