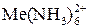Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Определение кальция и магния
Цель работы: определить комплексонометрическим методом: – проба А – общую жесткость воды, ммоль экв/л; – проба Б – массу кальция и магния в пробе, г. Сущность работы. Ионы Са2+ и Mg2+ образуют комплексонаты, которые устойчивы в щелочной среде, поэтому их титруют стандартным раствором ЭДТА в присутствии аммиачного буфера. Если использовать индикатор эриохром черный Т, то в к. т. т. наблюдается переход окраски раствора от сиреневой (комплексы индикатора с Са2+ и Mg2+) к синей (свободная форма индикатора в этих условиях). Жесткость воды – это суммарный показатель качества воды. Она обусловлена наличием ионов Са2+ и Mg2+. Общая жесткость воды показывает, сколько миллимоль эквивалентов Са2+ и Mg2+ в сумме содержится в 1 л воды. Суммарное содержание Са2+ и Mg2+ определяют прямым титрованием пробы воды в аммонийном буфере стандартным раствором Me2+ + H2Y2– = MeY2– + 2H+ Þ f экв(Me2+) = Поскольку концентрация Са2+ и Mg2+ в воде незначительна, для титрования берут большие аликвоты анализируемой воды (50,00 или 100,00 мл) с помощью специальных пипеток большой вместимости. Раздельное определение Са2+ и Mg2+ при совместном присутствии в растворе основано на титровании пробы с разными индикаторами в разных условиях. Сначала определяют суммарное содержание кальция и магния в пробе. С этой целью титруют аликвоту анализируемого раствора комплексоном III с индикатором эриохромом черным Т в среде аммиачного буфера. При этом протекают следующие реакции: Ca2+ + H2Y2– = CaY2– + 2H+, Mg2+ + H2Y2– = MgY2– + 2H+ Þ Þ f экв(Ca2+) = Затем определяют содержание кальция, титруя такую же аликвоту раствором ЭДТА с индикатором мурексидом в сильнощелочной среде. При добавлении щелочи ионы магния маскируются за счет осаждения в виде Mg(OH)2¯ и не реагируют с ЭДТА. Следовательно, титруются только ионы кальция: Ca2+ + H2Y2– = CaY2– + 2H+ Свободная форма индикатора мурексида в этих условиях имеет сиренево-фиолетовую окраску, а комплекс его с кальцием – кирпично-красную. Содержание магния в пробе находят по разности. Оборудование и реактивы: бюретка, мерный цилиндр (25 мл), стандартный раствор ЭДТА, аммиачный буфер с рН 9, индикатор эриохром черный Т в смеси с NaCl (1: 100). Для анализа пробы А дополнительно: пипетка Мора большой вместимости (50,00 или 100,00 мл), конические колбы большой вместимости (250 мл). Для анализа пробы Б дополнительно: мерная колба, пипетка Мора, конические колбы, гранулированный NaOH, мурексид в смеси с NaCl (1: 100).
Выполнение работы Проба А. Определение общей жесткости воды. Получают у лаборантов анализируемый раствор в коническую колбу. Отбирают пипеткой аликвоту 50,00 или 100,00 мл и переносят в другую коническую колбу. Прибавляют 20–25 мл аммонийного буфера, индикатор на кончике шпателя и титруют раствором комплексона III до перехода окраски раствора от сиреневой к синей. По результатам титрования рассчитывают общую жесткость воды (ммоль-экв/л):
Делают вывод о характеристике воды, используя справочные данные (см. &). Проба Б. Раздельное определение кальция и магния. Получают у лаборантов анализируемый раствор в мерную колбу, доводят до метки и перемешивают. Для определения суммарной концентрации кальция и магния отбирают пипеткой аликвоту анализируемого раствора в колбу для титрования, добавляют 20–25 мл аммиачного буфера и индикатор эриохром черный Т на кончике шпателя. Титруют раствором ЭДТА до перехода сиреневой окраски раствора в синюю. Усредняют полученные близкие объемы ЭДТА и получают среднее значение объема титранта V 1(Na2H2Y), который затрачен на титрование Ca2+ и Mg2+ в сумме. Для определения кальция отбирают пипеткой такую же аликвоту анализируемого раствора, вносят в него 2–3 гранулы NaOH (для создания сильнощелочной среды, проверить с помощью универсальной индикаторной бумаги!), мурексид на кончике шпателя и титруют раствором ЭДТА до перехода кирпично-красной окраски в сиренево-фиолетовую. Усредняют полученные близкие объемы ЭДТА и получают среднее значение объема титранта V 2(Na2H2Y), который затрачен на титрование Ca2+. По разности находят объем титранта, пошедший на титрование Mg2+: V 3(Na2H2Y) = V 1(Na2H2Y) – V 2(Na2H2Y). Исходя из полученных значений объемов V 2(Na2H2Y) и V 3(Na2H2Y), рассчитывают массу кальция и магния в пробе (г).
Лабораторная работа № 20
Комплексонометрическое определение ионов поливалентных Цель работы: определить по указанию преподавателя массу определяемого иона металла в растворе (г) или массовую долю (%) соли металла в образце (табл. 15). Таблица 15 Задания для выполнения лабораторной работы
Сущность работы. Важнейшим достоинством комплексонометрии является возможность определения практически всех катионов поливалентных металлов. В зависимости от устойчивости комплексонатов металлов и их комплексов с индикатором, а также других особенностей титруемой системы применяют методы прямого, обратного титрования или титрования по замещению. Прямым титрованием определяют Mg2+, Ca2+, Zn2+, Cd2+, Pb2+, Co2+, Ni2+, Cu2+, Mn2+, Fe3+ и др. Если реакция с ЭДТА протекает слишком медленно (Al3+, Cr3+), отсутствует подходящий индикатор для условий существования иона в растворе (Hg2+), то применяют обратное титрование. Определение Co2+, Ni2+, Cu2+ основано на прямом комплексонометрическом титровании в присутствии мурексида при значении рH 7–8, которое поддерживается с помощью аммиачного буфера. При более высоких значениях pH происходит образование аммиачных комплексов Me2+ + 6NH3 = и разрушение комплекса металла с индикатором, что снижает точность титрования. Определение Fe3+ проводится прямым титрованием в присутствии сульфосалициловой кислоты при pH < 3. Для увеличения скорости реакции комплексообразования титрование лучше вести при температуре 60оС. Определение Al3+ проводится обратным титрованием солью цинка (II) в присутствии ксиленолового оранжевого или солью меди(II) в присутствии индикатора ПАН. Оборудование и реактивы: технические и аналитические весы, мерные колбы, бюретка, пипетка Мора, мерный цилиндр, конические колбы, стандартный раствор ЭДТА. Для анализа пробы А: аммиачный буферный раствор, мурексид. Для анализа пробы Б: ацетатный буферный раствор pH 2,5, Для анализа пробы В: кристаллический ZnSO4 · 7H2O, 0,25 М раствор ацетата натрия, 1 М раствор HCl, ксиленоловый оранжевый, водяная баня. Выполнение работы. Если проводят анализ раствора, то получают его в мерную колбу, доводят до метки дистиллированной водой и перемешивают. Затем отбирают отдельные аликвоты анализируемого раствора в колбы для титрования, создают необходимые условия и проводят титрование в соответствии с описанными ниже методиками. По результатам титрования рассчитывают массу определяемого иона в пробе (г).
Если для анализа предложена сухая смесь соли с индифферентными примесями, то рассчитывают навеску соли, необходимую для приготовления раствора заданной концентрации в имеющейся мерной колбе. Затем берут навеску, переносят в мерную колбу, растворяют в дистиллированной воде (в случае солей Fe3+ – с добавлением кислоты), доводят до метки и перемешивают. Затем отбирают отдельные аликвоты полученного раствора в колбы для титрования, создают необходимые условия и проводят титрование в соответствии с описанными ниже методиками. По результатам титрования рассчитывают массовую долю кристаллогидрата в образце (%). Проба А. Определение Co2+, Ni2+, Cu2+. К аликвоте раствора медленно, по каплям, при перемешивании добавляют аммиачный буферный раствор. При этом вначале протекает образование осадка гидроксида металла, а затем его растворение с образованием аммиачного комплекса. Как только осадок растворится, добавление буферного раствора прекращают. К раствору добавляют мурексид на кончике шпателя и титруют раствором ЭДТА до перехода окраски к яркой фиолетово-сиреневой. Проба Б. Определение Fe 3+. К аликвоте раствора добавляют 5 мл ацетатного буферного раствора, нагревают до 60оС, добавляют 1 мл раствора сульфосалициловой кислоты и титруют раствором ЭДТА до перехода окраски от красно-фиолетовой к бледно-желтой. Проба В. Определение Al 3+. Готовят 0,05 н. стандартный раствор сульфата цинка по точной навеске, как описано в лабораторной работе № 18. К аликвоте раствора, содержащего Al3+, добавляют 20,00 мл стандартного раствора ЭДТА и 2 мл 1 М HCl. Нагревают до кипения и оставляют на кипящей водяной бане на 10 минут. После охлаждения добавляют в колбу 10 мл раствора ацетата натрия, ксиленоловый оранжевый на кончике шпателя и титруют раствором сульфата цинка до перехода окраски от желтой к красной.
Программа курса
ВВЕДЕНИЕ Предмет аналитической химии. Значение аналитической химии. Аналитический контроль технологических процессов. Классификация методов аналитической химии: методы разделения, методы обнаружения и методы определения. Цели и задачи методов. Общая схема аналитического определения. Выбор метода анализа. Отбор пробы и пробоподготовка. Метрологические основы аналитической химии. Статистическая обработка результатов анализа.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-25; просмотров: 5543; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.224.53.202 (0.019 с.) |
 , f экв(H2Y2–) =
, f экв(H2Y2–) = 
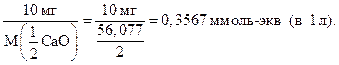 1 °d = 0,3567 ммоль-экв/л.
1 °d = 0,3567 ммоль-экв/л.