Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Основная статья: Литий-ионный аккумулятор
Литий-ионный аккумулятор состоит из электродов (катодного материала на алюминиевой фольге и анодного материала на медной фольге), разделенных пропитанными электролитом пористыми сепараторами. Переносчиком заряда в литий-ионном аккумуляторе является положительно заряженный ион лития, который имеет способность внедряться (интеркалироваться) в кристаллическую решетку других материалов (например, в графит, окислы и соли металлов) с образованием химической связи, например: в графит с образованием LiC6, окислы (LiMO2) и соли (LiMRON) металлов. Литий-полимерный аккумулятор Основная статья: Литий-полимерный аккумулятор В качестве электролита используется полимерный материал с включениями гелеобразного литий-проводящего наполнителя. Используется в мобильных телефонах, цифровой технике и пр. Характеристики Максимально возможный полезный заряд аккумулятора называется зарядной ёмкостью, или просто ёмкостью. Ёмкость аккумулятора — это заряд, отдаваемый полностью заряженным аккумулятором при разряде до наименьшего допустимого напряжения. В системе СИ ёмкость аккумуляторов измеряют в кулонах, на практике часто используется внесистемная единица — ампер-час. 1 А⋅ч = 3600 Кл.Реже на аккумуляторах указывается энергетическая ёмкость — энергия, отдаваемая полностью заряженным аккумулятором при разряде до наименьшего допустимого напряжения. В системе СИ она измеряется в джоулях, на практике иногда используется внесистемная единица — ватт-час. 1 Вт⋅ч = 3600 Дж.Электрические и эксплуатационные характеристики аккумулятора зависят от материала электродов и состава электролита. Сейчас наиболее распространены следующие аккумуляторы: По мере исчерпания химической энергии напряжение и ток падают, аккумулятор перестаёт действовать. Зарядить аккумулятор (батарею аккумуляторов) можно от любого источника постоянного тока с бо́льшим напряжением при ограничении тока. Наиболее распространённым считается зарядный ток (в амперах) в 1/10 номинальной ёмкости аккумулятора (в ампер⋅часах), однако эта величина не имеет никакого научного обоснования. Многие типы аккумуляторов имеют различные ограничения, которые необходимо учитывать при зарядке и последующей эксплуатации, например NiMH-аккумуляторы чувствительны к перезаряду, литиевые — к переразряду, напряжению и температуре. NiCd- и NiMH-аккумуляторы имеют так называемый эффект памяти, заключающийся в снижении ёмкости, в случае когда зарядка осуществляется при не полностью разряженном аккумуляторе. Также эти типы аккумуляторов обладают заметным саморазрядом, то есть они постепенно теряют заряд, даже не будучи подключенными к нагрузке. Для борьбы с этим эффектом может применяться капельная подзарядка.
Типы аккумуляторов · Никель-солевой аккумулятор · Железо-воздушный аккумулятор · Железо-никелевый аккумулятор · Лантан-фторидный аккумулятор · Литий-железно-сульфидный аккумулятор · Литий-железно-фосфатный аккумулятор · Литий-ионный аккумулятор (Li-Ion) · Литий-полимерный аккумулятор · Литий-титанатный аккумулятор · Литий-фторный аккумулятор · Литий-хлорный аккумулятор · Литий-серный аккумулятор · Натрий-никель-хлоридный аккумулятор · Натрий-серный аккумулятор · Никель-кадмиевый аккумулятор (NiCd) · Никель-металл-гидридный аккумулятор (NiMH) · Никель-цинковый аккумулятор · Свинцово-водородный аккумулятор · Свинцово-кислотный аккумулятор · Серебряно-кадмиевый аккумулятор · Серебряно-цинковый аккумулятор · Цинк-бромный аккумулятор · Цинк-воздушный аккумулятор · Цинк-хлорный аккумулятор · Никель-водородный аккумулятор История Первые советские пальчиковые аккумуляторы Д-0,26 и НКГЦ собирались на заводе «Аналог» (г. Ставрополь), практически вручную Схемы
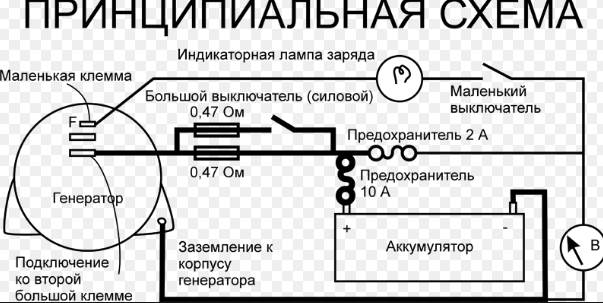
Заключение В этом отчете мы объяснили принцип работу электрический аккумулятора. Электрический аккумулятор — химический источник тока многоразового действия, основная специфика которого заключается в обратимости внутренних химических процессов, что обеспечивает его многократное циклическое использование (через заряд-разряд) для накопления энергии и автономного электропитания различных электротехнических устройств и оборудования, а также для обеспечения резервных источников энергии в медицине, производстве и в других сферах. А так же мы разработали индивидуальную схему для этого отчета.
Отчет №3 Топливние элементы Впервые этот тип источника энергии был использован на космическом аппарате Джемини в 1956 году. Топливные элементы имеют высокие показатели по массо-габаритным характеристиками и удельной мощности по сравнению с парой солнечные батареи и химический аккумулятор, устойчивы к перегрузкам, имеют стабильное напряжение, бесшумны. Однако они требуют запаса топлива, потому применяются на аппаратах со сроком нахождения в космосе от нескольких дней до 1—2 месяцев.Используются в основном водород-кислородные топливные элементы, так как водород обеспечивает наивысшую калорийность, и, кроме того, образовавшаяся в результате реакции вода может быть использована на пилотируемых космических аппаратах. Для обеспечения нормальной работы топливных элементов необходимо обеспечить отвод образующихся в результате реакции воды и тепла. Ещё одним сдерживающим фактором вляетяся относительно высокая стоимость жидкого водорода и кислорода, сложность их хранения.Топливный элемент — электрохимическое устройство, подобное гальваническому элементу, но отличающееся от него тем, что вещества для электрохимической реакции подаются в него извне — в отличие от ограниченного количества энергии, запасенного в гальваническом элементе или аккумуляторе.Топливные элементы осуществляют превращение химической энергии топлива в электричество, минуя малоэффективные, идущие с большими потерями, процессы горения. Это электрохимическое устройство в результате высокоэффективного «холодного» горения топлива непосредственно вырабатывает электроэнергию.Естественным топливным элементом является митохондрия живой клетки. Митохондрии перерабатывают органическое «горючее» — пируваты и жирные кислоты, синтезируя АТФ — универсальный источник энергии для всех биохимических процессов в живых организмах, одновременно создавая разность электрических потенциалов на своей внешней мембране. Однако копирование этого процесса для получения электроэнергии в промышленных масштабах лишено смысла, т. к. на долю электрической разности потенциалов приходится ничтожная доля химической энергии исходных веществ: почти вся энергия передаётся молекулам АТФ.
Устройство ТЭ Топливные элементы — это электрохимические устройства, которые теоретически могут иметь очень высокий коэффициент преобразования химической энергии в электрическую (~80 %)[источник не указан 1497 дней].КПД, определённый по теплоте химической реакции, может быть и выше 100 % из-за того, что в работу может превращаться и теплота окружающей среды. Здесь тем не менее нет никакого противоречия с ограничениями на КПД тепловых машин, поскольку топливные элементы не работают по замкнутому циклу и реагирующие вещества не возвращаются в начальное состояние. При химической реакции в топливном элементе в электрическую энергию превращается в конечном счёте не теплота реагентов, а их внутренняя энергия и, возможно, некоторое количество теплоты из окружающей среды
|
||||||
|
Последнее изменение этой страницы: 2017-01-25; просмотров: 135; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.216.32.116 (0.008 с.) |