
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
III. Реакции окисления и восстановления
1) Окисление альдегидов Альдегиды чрезвычайно легко окисляются до соответствующих кислот. а) реакция серебряного зеркала: O O СH3-C +2[Ag(NH3)2]OH H ONH4 Реакцию эту дают только альдегиды, поэтому она применяется как качественная реакция на альдегиды. б) реакция Фелинга Реактив Фелинга – это Cu(OH)2, растворенный в сегнетовой соли, с которой она образует комплексный алкоголят. O O CH3-C +2Cu(OH)2 H OH закись меди (осадок красного цвета) Качественная реакция на альдегиды. в) окисление перекисью водорода O O 2H-С + H2O2 H OH В этой реакции альдегид тоже ведет себя как восстановитель настолько активный, что восстанавливает перекись не до воды, а до водорода. г) окисление на воздухе при освещении идет по цепному свободно-радикальному механизму. O O u: CH3-C H O O p: CH3-C. + O2 O-O. O O O O CH3-C + CH3-C O-O. H O-O-H надуксусная кислота 2) Окисление кетонов протекает значительно труднее. Кетоны не окисляются слабыми окислителями (аммиакат гидроокиси серебра – реактив Фелинга). Сильными окислителями они окисляются с разрывом цепи. Окисление кетонов происходит в соответствии с правилами Попова: 1. Действие окислителя направлено в основном на соседний с карбонилом атом углерода, что приводит к разрыву цепи и образованию двух молекул кислот. 2. У несимметричных кетонов главным направлением реакции является окисление менее гидрированного соседнего звена. CH3-C-CH2-CH3+O O O OH -H2O O O O оксикетон дикетон
Реакции восстановления 1) Восстановление литийалюминий гидридом приводит к образованию первичных или вторичных спиртов. AlH4 Действующий реагент Н-. Механизм реакции – нуклеофильное присоединение. O O- CH3-C + H- H H Восстановление до спиртов может проводиться действием молекулярного водорода в присутствии катализаторов: Ni, Pt, Pd. 2) Восстановление до пинаконов по свободно-радикальному механизму. OH OH OH 2CH3-C-CH3 + 2H. O CH3 CH3 CH3 3) Восстановление до углеродов по Клеменсону. CH3-C-CH3 + 2Zn + 4HCl(HgCl2) O Роль HgCl2 – образование амальгамы цинка. 4) Восстановление до углеводородов по Кижнеру – через гидразоны (см. взаимодействие с гидразином).
IV. РЕАКЦИИ В РАДИКАЛЕ
Атомы Н в 1) Замещение галогенами O O CH3-C +3Cl2 H H CH3-C-CH3 + Br2 O Br O
|
|||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 134; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.138.174.195 (0.006 с.) |
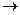 3NH3 + H2O + 2Ag + CH3-C
3NH3 + H2O + 2Ag + CH3-C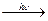 H. + CH3-C.
H. + CH3-C.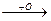 CH3-C-C-CH3
CH3-C-C-CH3 
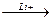 CH3-CH2OLi
CH3-CH2OLi  CH3-CH2-OH + LiOH
CH3-CH2-OH + LiOH -положении к группе С=О под ее индукционным влиянием становятся очень подвижными и легко замещаются.
-положении к группе С=О под ее индукционным влиянием становятся очень подвижными и легко замещаются.


