
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Факторы, влияющие на скорость ферм. реакции
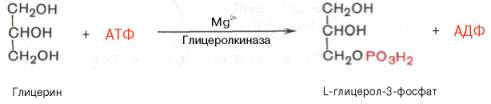
Скорость ферментативной реакции, как и активность фермента, в значительной степени определяется также присутствием в среде активаторов и ингибиторов: первые повышают скорость реакции, а вторые тормозят эту реакцию. Активирующее влияние на скорость ферментативной реакции оказывают разнообразные вещества органической и неорганической природы. одним из наиболее существенных факторов, определяющих скорость ферментативной реакции, является концентрация субстрата (или субстратов) и продукта (продуктов). При постоянной концентрации фермента скорость реакции постепенно увеличивается, достигая определенного максимума, когда дальнейшее увеличение количества субстрата практически не оказывает влияния на скорость ферментативной реакции. Ограничивающим скорость реакции фактором в последнем случае становится концентрация фермента. Именно при этих условиях определяют величину максимальной скорости (Vmax) и значения константы Михаэлиса (Km) Скорость любой ферментативной реакции непосредственно зависит от концентрации фермента. Существующая линейная зависимость между этими величинами, когда скорость реакции прямо пропорциональна количеству присутствующего фермента, справедлива только в определенных условиях, например в начальный период ферментативной реакции, так как в этот период практически не происходит обратной реакции, а концентрация продукта оказывается недостаточной для обратимости реакции. Именно в этом случае скорость реакции (точнее, начальная скорость реакции v) будет пропорциональна концентрации фермента. Биосинтез триглицерина и глицеролфосфолипидов БИОСИНТЕЗ ТРИГЛИЦЕРИДОВ Известно, что скор биосинтеза ЖК во многом определяется скоростью обр-ния триглицеридов и фосфолипидов, так как свободные ЖК присутствуют в тканях и плазме крови в небольших количествах и в норме не накапливаются. Синтез триглицеридов происходит из глицерина и жирных кислот (главным образом стеариновой, пальмитиновой и олеиновой). Путь биосинтеза триглицеридов в тканях протекает через образование α-глице-рофосфата (глицерол-3-фосфата) как промежуточного соединения. В почках, а также в стенке киш-ка, где акт-сть фермента глицеролкиназы высока, глицерин фосфорилируется за счет АТФ с образованием глицерол-3-фосфата:
В жировой ткани и мышцах вследствие очень низкой активности глицеролкиназы образование глицерол-3-фосфата в основном связано с процессами гликолиза и гликогенолиза. Известно, что в проц гли-колитического распада глюкозы образуется дигидроксиацетонфосфат. Последний в присутствии цитоплазматической глицерол-3-фос-фатдегидрогеназы способен превращаться в глицерол-3-фосфат:
Отмечено, что если содержание глюкозы в жир ткани понижено, то обр-ся лишь незначит кол-во глицерол-3-фосфата и освободившиеся в ходе липолиза свободные ЖК не мб использ для ресинтеза триглицеридов, поэтому ЖК покидают жировую ткань. Напротив, активация гликолиза в жировой ткани способствует накоплению в ней триглицеридов, а также входящих в их состав жирных кислот. В печени наблюдаются оба пути образования глицерол-3-фосфата. Образовавшийся глицерол-3-фосфат последовательно ацилируется двумя молекулами КоА-производного ЖК (т.е. «активными» формами жирной кислоты – ацил-КоА). В результате образуется фосфатидная кислота (фосфатидат):
Как отмечалось, ацилирование глицерол-3-фосфата протекает последовательно, т.е. в 2 этапа. Сначала глицерол-3-фосфат-ацилтрансфераза кат-ет обр-ние лизофосфатидата (1-ацилглицерол-3-фосфата, а затем 1-ацилглицерол-3-фосфат-ацилтрансфераза кат-ет обр-ние фосфатидата (1,2-диацилглицерол-3-фосфата). Далее фосфатидная кислота гидролизуется фосфатидат-фосфогидро-лазой до 1,2-диглицерида (1,2-диацилглицерола):
Затем 1,2-диглицерид ацилируется третьей молекулой ацил-КоА и превращается в триглицерид (триацилглицерол). Эта реакция катализируется диацилглицерол-ацилтрансферазой:
Синтез триглицеридов (триацилглицеролов) в тканях происходит с учетом двух путей образования глицерол-3-фосфата и возможности синтеза триглицеридов в стенке тонкой кишки из β-моноглицеридов, поступающих из полости кишечника в больших количествах после расщепления пищевых жиров. На рис. 11.6 представлены глицерофосфатный, дигидроксиацетон-фосфатный и β-моноглицеридный (моноацилглицероловый) пути синтеза триглицеридов.
Установлено, что большинство ферментов, участвующих в биосинтезе триглицеридов, находятся в эндоплазматическом ретикулуме, и только некоторые, например глицерол-3-фосфат-ацилтрансфераза,– в митохондриях Стр. нуклеотида
Все прокариоты и эукариоты располагают особыми ферментативными системами как биосинтеза нуклеотидов de novo, так и их разрушения. Причем не существует отдельного пути биосинтеза дезоксинуклеотидов, а они являются продуктами биохимического преобразования готовых нуклеотидов. В водных растворах нуклеотиды подвергаются таутомерии. Основная таутомерная форма азотистых оснований – лакт а мная форма. Появление лакт и мной формы азотистых оснований в составе ДНК влечет невозможность правильного спаривания азотистых оснований разных нитей ДНК в процессе репликации и, следовательно, может привести к мутации. Изредка встречаются минорные нуклеозиды - продукты О-, С- или N-алкилирования азотистых оснований, а также продукты алкилирования ОН-групп остатков моносахарида.
Вит. РР Витамин РР (никотиновая кислота, никотинамид, ниацин) получил также название антипеллагрического витамина (от итал. preventive pellagra – предотвращающий пеллагру), поскольку его отсутствие является причиной заболевания, называемого пеллагрой. Никотиновая к-та предст собой соединение пиридинового ряда, содержащее карбоксильную группу (никотинамид отличается наличием амидной группы).
Наиболее характерными признаками авитаминоза РР, т.е. пеллагры (от итал. pelle agra – шершавая кожа), являются поражения кожи (дерматиты), пищеварительного тракта (диарея) и нарушения нервной деятельности (деменция). Дерматиты чаще всего симметричны и поражают те участки кожи, которые подвержены влиянию прямых солнечных лучей: тыльную поверхность кистей рук, шею, лицо; кожа становится красной, затем коричневой и шершавой. Поражения кишечника выражаются в развитии анорексии, тошнотой, болями в области живота, поносами. Диарея приводит к обезвоживанию организма. Слизистая оболочка толстой кишки сначала воспаляется, затем изъязвляется. Специфичными для пеллагры являются стоматиты, гингивиты, поражения языка со вздутием и трещинами. Поражения мозга проявляются головными болями, головокружением, повышенной раздражимостью, депрессией и другими симптомами, включая психозы, психоневрозы, галлюцинации и др. Симптомы пеллагры особенно резко выражены у больных с недостаточным белковым питанием. Установлено, что это объясняется недостатком триптофана, который является предшественником никотинамида, частично синтезируемого в тканях человека и животных, а также недостатком ряда других витаминов (пиридоксина; см. главу 12).
Биологическая роль. Витамин РР входит в состав НАД или НАДФ, являющихся коферментами большого числа обратимо действующих в ОВР дегидрогеназ. Показано, что ряд дегидрогеназ использует только НАД и НАДФ (соответственно малатдегидрогеназа и глюкозо-6-фосфатдегидрогеназа), др могут кат-вать ОВР в присутствии любого из них (например, глутаматдегидрогеназа). В проц био окисления НАД и НАДФ выполняют роль промежут переносчиков электронов и протонов между окисляемым субстратом и флавиновыми ферментами. Распространение в природе и суточная потребность. Никотиновая кислота также относится к витаминам, широко распространенным в растительных и животных организмах. Для человека основными источниками никотиновой кислоты и ее амида являются рис, хлеб, картофель, мясо, печень, почки, морковь и другие продукты. Суточная потребность для взрослого человека составляет 18 мг. Горм. гипофиза В гипофизе синтезируется ряд биологически активных гормонов белковой и пептидной природы, оказывающих стимулирующий эффект на различные физиологические и биохимические процессы в тканях-мишенях (табл. 8.2). В зависимости от места синтеза различают гормоны передней, задней и промежуточной долей гипофиза. Вазопрессин и окситоцин Гормоны вазопрессин и окситоцин синтезируются рибосомальным путем. Вазопрессин отличается от окситоцина двумя АМКами: он содержит в положении 3 от N-конца фенилаланин вместо изолейцина и в положении 8 – аргинин вместо лейцина. Указанная последовательность 9 АМК характерна для вазопрессина человека, обезьяны, лошади, крупного рогатого скота, овцы и собаки. В молекуле вазопрессина из гипофиза свиньи вместо аргинина в положении 8 содержится лизин, отсюда название «лизин-вазопрессин». Основной био эффект окситоцина у млекопитающих связан со стимуляцией сокращения гладких мышц матки при родах и мышечных волокон вокруг альвеол молочных желез, что вызывает секрецию молока. Вазопрессин стимулирует сокращение гладких мышечных волокон сосудов, оказывая сильное вазопрессорное действие, однако основная роль его в орг-ме сводится к регуляции водного обмена, откуда его второе название антидиуретического гормона. В небольших концентрациях (0,2 нг на 1 кг массы тела) вазопрессин оказывает мощное антидиуретическое действие – стимулирует обратный ток воды через мембраны почечных канальцев. В норме он контролирует осмотическое давление плазмы крови и водный баланс орг-ма человека. При патологии, в частности атрофии задней доли гипофиза, развивается несахарный диабет – заболевание, характеризующееся выделением чрезвычайно больших количеств жидкости с мочой. При этом нарушен обратный проц всасыв воды в канальцах почек. Относительно механизма действия нейрогипофизарных гормонов известно, что гормональные эффекты, в частности вазопрессина, реализуются через аденилатциклазную систему.
|
||||||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 362; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.172.146 (0.018 с.) |




 Нуклеотиды (нуклеозидфосфаты) - это фосфорные эфиры нуклеозидов обычно по 3'- и 5'-ОН группам остатка моносахарида. Большинство природных нуклеотидов имеют β-конфигурацию N-гликозидной связи. В живых объектах встречаются моно-, ди-, три- (реже тетра- и поли-) фосфопроизводные нуклеозидов. Пуриновые и пиримидиновые нуклеотиды представлены в виде рибонуклеотидов и дезоксирибонуклеотидов. Основные представители нуклеотидов перечислены в таблице, а принцип строения показан на рисунке. Поскольку нуклео-тиды могут реаги-ровать друг с дру-гом, их класси-фицируют по чис-лу структурных мономеров на мо-нонуклеотиды, олигонуклеотиды (ди-, три-, тетра- и т.д.) и полинук-леотиды. В природ-ных мононуклео-тидах доминирует 5'-фосфоэфирная связь, как показано на рисунке.Причем такое общеизвестное соединение, как АТФ, обычно реализует свою биологическую активность в виде координационного комплекса с ионом магния. К числу важнейших полинуклеотидов относят ДНК и РНК. При физиологических знач рН среды нуклеотиды заряжены
Нуклеотиды (нуклеозидфосфаты) - это фосфорные эфиры нуклеозидов обычно по 3'- и 5'-ОН группам остатка моносахарида. Большинство природных нуклеотидов имеют β-конфигурацию N-гликозидной связи. В живых объектах встречаются моно-, ди-, три- (реже тетра- и поли-) фосфопроизводные нуклеозидов. Пуриновые и пиримидиновые нуклеотиды представлены в виде рибонуклеотидов и дезоксирибонуклеотидов. Основные представители нуклеотидов перечислены в таблице, а принцип строения показан на рисунке. Поскольку нуклео-тиды могут реаги-ровать друг с дру-гом, их класси-фицируют по чис-лу структурных мономеров на мо-нонуклеотиды, олигонуклеотиды (ди-, три-, тетра- и т.д.) и полинук-леотиды. В природ-ных мононуклео-тидах доминирует 5'-фосфоэфирная связь, как показано на рисунке.Причем такое общеизвестное соединение, как АТФ, обычно реализует свою биологическую активность в виде координационного комплекса с ионом магния. К числу важнейших полинуклеотидов относят ДНК и РНК. При физиологических знач рН среды нуклеотиды заряжены  Витамин РР малорастворим в воде (примерно 1%), но хорошо растворим в водных растворах щелочей. Никотиновая кислота кристаллизуется в виде белых игл.
Витамин РР малорастворим в воде (примерно 1%), но хорошо растворим в водных растворах щелочей. Никотиновая кислота кристаллизуется в виде белых игл.


