Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
О повреждении какой ткани можно думать, если в крови больного повышена активность алт, лдг и аргиназы. За счет каких изоферментов лдг можно предполагать повышение активности фермента.
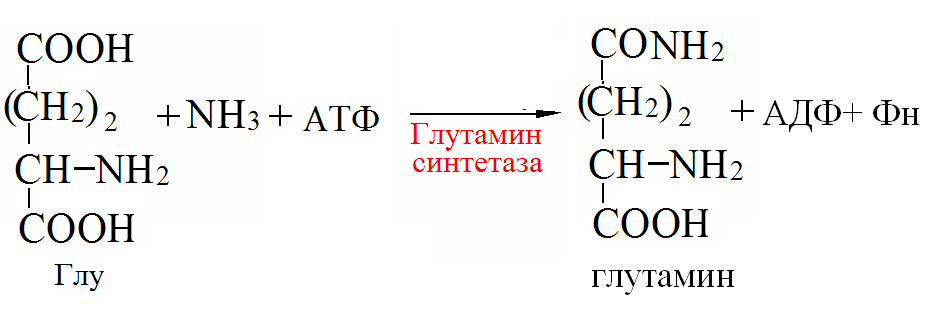
Пути обезвреживания аммиака в организме Токсичность аммиака связана с его действием на ЦНС: аммиак проходит сквозь мембраны и проникает в клетки мозга, аммиак взаимодействует с α-кетоглутаратом, что приводит к снижению скорости окисления глюкозы, угнетение обмена АМК из-за снижения концентрации α-кетоглутарата, аммиак усиливает синтез глутамина в нервной ткани, повышается осмотическое давление, развивается отёк мозга, снижение концентрации глу приводит к нарушению обмена нейромедиаторов (ГАМК), это нарушает проведение нервного импульса и вызывает судороги, аммиак в крови и цитозоле образует ион NH4+, накопление которого нарушает трансмембранный перенос ионов натрия и калия, что влияет на проведение нервных импульсов. Источники аммиака в организме: дезаминирование АМК, амидов АМК, биогенных аминов, пуриновых оснований, распад пиримидиновых оснований, образуется в кишечнике с участием бактерий из пищевого белка. Пути обезвреживания аммиака: синтез мочевины, образование амидов АМК, восстановительное аминирование, образование аммонийных солей. Образование амидов АМК
у детей раннего возраста это основной путь обезвреживания аммиака. Глутамин и аспарагин образуются в местах образования аммиака: печень, мозг, мышцы. Глутамин нетоксичен, свободно проходит через клеточную мембрану, форма, в которой транспортируется аммиак, временное хранилище аммиака, используется для синтеза белка, аминосахаров, пуриновых и пиримидиновых нуклеотидов, фолиевой кислоты, аминокислот (глу, три, гис, аспарагин), донор аммиака. Образование аммонийных солей глутамин используется почками в качестве источника аммиака, необходимого для нейтрализации кислых продуктов. Удаление аммиака происходит в виде аммонийных солей с мочой (до 1 г в сутки). Экскреция аммиака с мочой увеличивается при ацидозе. При ацидозе повышается активность глутаминазы и усиливается глюконеогенез. Глутамат после дезаминирования может превращаться в глюкозу путём глюконеогенеза. Восстановительное аминирование
Биосинтез мочевины: из кишечника аммиак с воротной веной идёт в печень, главный путь экскреции азота у человека в составе мочевины, протекает в печени, в синтезе мочевины 5 реакций, 2 из которых протекают в митохондриях.
Орнитиновый цикл - основной путь обезвреживания аммиака и главная форма выделения азота из организма взрослых и детей старшего возраста. Бицикл Кребса - связь с ЦТК через митохондрии, СО2, АТФ, общие фрагменты (фумарат), Мочевина. В синтезе мочевины участвует 6 АМК: орнитин, цитруллин, аргинин, аспарагиновая кислота, аргининосукцинат, N-ацетилглутамат – активатор первой реакции. Орнитин регенерирует в каждом обороте цикла мочевины. В мочевине одна аминогруппа поступает в цикл в митохондриях при окислительном дезаминировании глутамата, вторую аминогруппу поставляет аспартат из цитозоля. Цикл мочевины участвует в регуляции рН крови. В орнитиновом цикле расходуется 4 макроэргические связи трёх молекул АТФ на каждый оборот цикла. Процесс сам себя обеспечивает энергией - при регенерации аспартата из фумарата образуется молекула НАДН2, которая даёт 3 АТФ, при окислительном дезаминировании глутамата образуется 3АТФ. Экскреция мочевины. В норме выделяется 25 г мочевины в сутки, мочевина – основной конечный продукт азотистого обмена. Для транспорта азота из тканей в печень используется 3 соединения: глутамин, аланин, аммиак. Аланин как переносчик азота Функции орнитинового цикла: превращение азота аминокислот в мочевину, которая предотвращает накопление аммиака, синтез аргинина. Содержание аммиака в крови определяется ионообменным методом, составляет 25 – 40 мкмоль/л. Гипераммониемия – повышенное содержание аммиака в крови. Рвота, сонливость, раздражительность, нарушение координации, судороги, потеря сознания, отёк мозга. Метаболические нарушения цикла мочевины. Лимитирующие скорость стадии в синтезе мочевины: 1, 2, 3, 5. Гипераммониемия типа I наследственная, при недостатке карбамоилфосфатсинтетазы1. Гипераммониемия типа II наследственная, при недостатке орнитинкарбамоилтрансферазы. УГЛЕВОДНЫЙ ОБМЕН Функции углеводов: Энергетическая функция. 60-70% энергии организм получает за счёт углеводов. Суточная потребность в углеводах 400 – 500 г. Мозг, кровь, почки, надпочечники живут за счёт углеводов. При окислении 1 г углеводов выделяется 4,1 ккал энергии. Резерв энергии – гликоген в мышцах и печени. Структурная функция. Углеводы входят в состав мембран, сухожилий. Защитная функция. Углеводы содержатся в слизи и антителах. Углеводы входят в состав биологически активных веществ: нуклеиновых кислот, коферментов, гормонов, гликолипидов, гликопротеидов.
|
|||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 118; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.14.121.242 (0.004 с.) |