
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Физические и химические свойстваСодержание книги
Поиск на нашем сайте Низшие члены ряда гликолей, а также глицерин – густые жидкости. Температуры кипения гликолей и глицерина значительно выше температуры кипения спиртов,ляется следствием ассоциации. Гликоли и глицерин хорошо растворимы в воде в любых соотношениях. Имеют сладкий вкус. Плотность полиолов больше единицы. Химические свойства соответствуют химическим свойствам одноатомных спиртов. Однако наличие нескольких гидроксильных групп в одной молекуле спирта накладывает особенности на свойства полиолов.
2.3.1. Образование солей с металлами Со щелочными металлами гликоли и глицерин образуют полные и неполные гликоляты: СН2ОNа-СН2ОNа, СН2ОNа-СН2ОН и глицераты СН2ОNа-СН2ОNа-СН2ОNа, СН2ОNа-СН2ОН-СН2ОNа. Гликоли и глицерин могут реагировать с гидроокисями тяжелых металлов с образованием комплексных соединений:
2.3.2. Образование сложных эфиров С минеральными и органическими кислотами гликоли и глицерин образуют сложные эфиры. При этом в образовании сложноэфирной системы могут участвовать одна или несколько гидроксильных групп. Т.е. образуются полные и неполные эфиры. Например:
Полный азотнокислый эфир глицерина – глицеринтринитрат (тривиальное название тринитроглицерин) – взрывчатое вещество, на основании которого изготавливаются динамит и пороха. Для глицерина характерно образование сложных эфиров с карбоновыми кислотами. Например, с уксусной кислотой:
Неполные эфиры будут называться моноацетат и диацетат. 2.3.3. Дегидратация Отщепление воды от гликолей может иметь внутримолекулярный и межмолекулярный характер. Примеры внутримолекулярной дегидратации:
Отщепление воды от глицерина соответствует дегидратации 1,2-гликоля и 1,3-гликоля:
Примеры межмолекулярной дегидратации:
2.3.4. Окисление Этиленгликоль окисляется до щавелевой кислоты. В качестве промежуточных продуктов образуются гликолевый альдегид и глиоксаль. Глицерин окисляется до мезоксалевой кислоты. В качестве промежуточного продукта образуется глицериновый альдегид.
ФЕНОЛЫ Ароматические гидроксисоединения – производные ароматических углеводородов – разделяются на две большие группы: фенолы и ароматические спирты Ароматические гидроксисоединения, в которых гидроксильная группа связана с ароматическим ядром, называются фенолами.
Классификация, номенклатура. Тривиальное название «фенол» принято в номенклатуре ИЮПАК. По числу гидроксильных групп фенолы разделяются на одноатомные, атомные и т.д., для бензола возможны шестиатомные:
Способы получения 1. Сплавление со щелочами:
этот метод широко применяется в промышленности. Реакцию ведут при 320-3500С. Более вывысокие выхода получаются при применении едкого кали.
2. Гидролиз галогенопроизводных. Например получение фенола из хлорбензола:
Процесс ведут в присутствии солей меди.
3. Разложение гидропероксидов: Самый выгодный способ получения фенола основан на кислотном разложении гидропероксида изопропил бензола (кумола):
4. Окислительное декарбоксилирование карбоновых кислот. Реакцию проводят при 200-3000С в присустывии солей меди (II):
5. Действие на первичные ароматические амины азотистой кислотой и дальнейший гидролиз образовавшейся соли диазония:
6. Гомологи фенола можно получить аналогичными реакциями из сульфо- галогено- или аминопроизводных гомологов бензола. Гомологи также можно получать алкилированием фенола.
Физические свойства Фенолы обычно являются кристаллическими веществами, малорастворимые в воде. Хорошо перегоняются с водяным паром. Обладает характерным запахом. Являются антисептиками. Сильно ядовиты. При попадании на кожу вызывает ожоги.
Химические свойства 1. Кислотные свойства. Фенолы являются кислотами более сильными, чем спирты и вода, но слабее угольной кислоты. Поэтому фенолы легко реагируют с раствором едкого натра с образованием фенолята:
Электронодонорные заместители в пара- орто-положениях понижают кислотные свойства. Электроноакцепторные заместители в пара- и орто-положениях повышают кислотные свойства. Так 2,4,6-тринитрофенол обладает выраженными кислотными свойствами. Поэтому называется пикриновой кислотой. Способен вытеснять угольную кислоту из ее солей, т.е. способен образовывать фенолят в растворе соды. Связь между углеродом бензольного кольца и атомом кислорода гидроксильной группы обладает повышенной прочностью за счет частичной двоесвязанности. Поэтому реакции с разрывом связи С-О для фенола не характерны.
Восстановление К числу реакций, протекающих с разрывом связи С-О, относится восстановление фенола цинковой пылью при перегонке. В ходе реакции гидроксильная группа замещается водородом:
Другим примером разрыва связи С-О является нуклеофильное замещение гидроксильной группы в активированных фенолах. Например, замещение гидроксильной группы в 2,4,6-тринитрофеноле на галоид по механизму «присоединение-отщепление»:
В основном химические свойства фенола формируют реакции, протекающие с разрывом связи С-Н, а также реакции замещения ароматическое кольцо.
О-алкилирование Сам фенол является слабым основанием, поэтому в реакции алкилирования с галоидными алкилами обычно используют фенолят натрия:
О-ацилирование Кислотные свойства фенола играют позитивную роль в реакциях фенола с хлорангидридами и ангидридами карбоновых кислот:
В форме фенолята фенол ацилируется хлорангидридом бензойной кислоты, поскольку у хлорангидрида бензойной кислоты связь хлора и углерода более прочная, чем такая связь в хлорангидридах алифатических кислот:
С хлорангидридами минеральных кислот также образуются эфиры. Причем с пятихлористым фосфором образуются эфиры, хлорированные в ароматическое кольцо.
Реакции замещения Галогены реагируют с фенолом без катализатора. Фенол взаимодействует с бромом в водном растворе. Причем реакция не останавливается на стадии монобромирования. В начале образуется 2,4,6-трибромфенол, а затем тетрабромпроизводное:
Аналогично под действием концентрированной азотной кислоты в присуствии серной кислоты фенол превращается в тринитрофенол (пикриновую кислоту):
Мононитрофенолы образуются при нитровании фенола разбавленной азотной кислотой в среде уксусной кислоты при комнатной температуре:
Два полученные изомера существенно различаются по своим свойствам. орто -нитрофенол, в отличие от пара-изомера, не растворяется в воде, имеет более низкую температуру кипения и перегоняется с водяным паром. Эти особенные свойства орто- нитрофенола обусловлены наличием внутримолекулярной водородной связи:
Ориентация электрофильного замещения в орто-положение характерно для фенола. Так сульфирование фенола при температуре 15-200С приводит к образованию орто -фенолсульфокислоты, а при температуре 1000С образуется пара -фенолсульфокислота:
Различие условий указывает, что орто -фенолсульфокислота явяляется продуктом кинетически контролируемым, а образование пара -фенолсульфокислоты контролируется термодинамически.
Реакция Реймера-Тимана: При взаимодействии фенола со щелочным раствором хлороформа образуется салициловый альдегид:
Реакция Кольбе-Шмитта При взаимодействии сухого фенолята натрия с углекислым газом образуется салициловая кислота:
Реакция с формальдегидом Фенолы легко конденсируются с формальдегидом (а также уксусным альдегидом, бензальдегидом, фталевым ангидридом, ацетоном) в присутствии кислот или щелочей. Конденсация с формальдегидом проходит по следующему механизму:
Окисление При окислении фенола пероксидом водорода в присутствии железного катализатора образуется пирокатехин:
При действии хромовой кислоты на фенол и гидрохинон образуется п -бензохинон, из пирокатехина получается о -бензохинон:
Восстановление Пр гидрировании водородом в присутствии катализатора фенолы превращаются в спирты, производные циклогексана:
|
||
|
Последнее изменение этой страницы: 2017-01-18; просмотров: 451; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.11 (0.009 с.) |

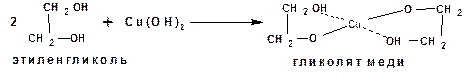






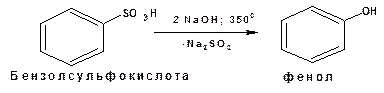
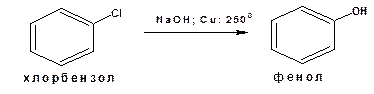









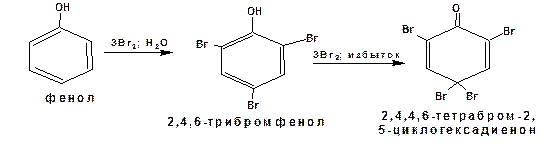
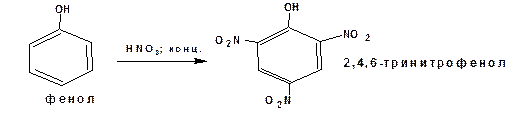

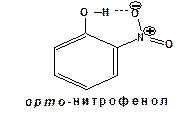



 При низкой температуре образуется полимер линейного строения, замещение только в орто-положение. При высокой температуре образуются продукты пара-замещения что приводит к пространственной сшивке полимера. Таким образом, получают фненолформальдегидные смолы.
При низкой температуре образуется полимер линейного строения, замещение только в орто-положение. При высокой температуре образуются продукты пара-замещения что приводит к пространственной сшивке полимера. Таким образом, получают фненолформальдегидные смолы.





