Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Первоначальные химические понятияСодержание книги Поиск на нашем сайте МОАУ «СОШ №3»
Рабочая тетрадь по химии Ученика(цы) 8 класса (дополнительные задания для закрепления ЗУН)
Бузулук 2016 г. ЗНАТЬ ____________________________________________________________________ ПЕРВОНАЧАЛЬНЫЕ ХИМИЧЕСКИЕ ПОНЯТИЯ Предмет химии. Вещества и их свойства. Химия занимает центральное место в ряду естественных наук, поскольку она изучает элементы и образуемые ими соединения, которые составляют Вселенную, и помогает нам понять окружающий нас мир. В химии, как и в любой науке, есть информация, которую нужно запомнить и подружиться с некоторыми понятиями как:
Химия – это наука о ………………………………………………………………….. …………………………………………………………………………………………..…………………………………………………………………………………………
Химия изучает ……………………………………………………………………….. ………………………………………………………………………………………….………………………………………………………………………………………….
Вещество – это………………………………………............................................... …………………………………………………………………………………………..…………………………………………………………………………………………
Свойства – это признаки……………………………………………........................... …………………………………………………………………………………………………………………………………………………………………………………….
В природе вещества встречаются в…………………………………………………. …………………………………………………………………………………………
Смеси по агрегатному состоянию делятся на ……………………………………... ………………………………………………………………………………………….
Определите однородные и неоднородные смеси: молоко, камень, песок, чай, мед, варенье, поваренная соль, бензин, воздух, известковая вода, спирт и заполните таблицу:
____________________________________________________________________ ЗНАТЬ ____________________________________________________________________ Физические и химические явления. Признаки химических реакции.
Изменения, которые происходят с окружающими нас веществами и предметами называются явлениями.
Различают два вида явлении: ………………………………………………………..
При физическом явлений изменяется……………………………………………….. ………………………………………………………………………………………но его …..………………………………………………………………………………….
При химическом явлении происходит ……………………………………………... …………………………………………………………………………………………. и изменяется ………………………………………………………………………….
Подчеркните явления, которые относятся к химическим:
Плавление, облачность, гниение, горение, ржавление, искривление гвоздя, испарение, изменение цвета, получение бензина из нефти, скисание молока.
Протекание химической реакции можно определить по следующим признакам: …………………………………………………………………………………………………………………………………………………………………………………….
Приведите примеры признаков химической реакции:
Выделение тепла:……………………………………………………………………………… …………………………………………………………………………………………………… Выделение газа…………………………………………………………………………………. …………………………………………………………………………………………………… Поглощение тепла…………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………………………………………………………….. Выпадение осадка …………………………………………………………………………… …………………………………………………………………………………………………… Появление запаха …………………………………………………………………………… ……………………………………………………………………………………………………. Изменение цвета ……………………………………………………………………………… …………………………………………………………………………………………………………………………………………………………………………………………………………. ____________________________________________________________________ ЗНАТЬ ____________________________________________________________________
Простые и сложные вещества. Атомы и молекулы. Из курса физики вы знаете, что молекулы состоят из атомов и молекул.
Молекула – мельчайшая частица. Атомы, соединяясь, образуют молекулу, а молекула, распадаясь, превращается в атомы. Атомы и молекулы невидимы, но на примере разложения воды можно убедиться в их существовании:
Сложные вещества – это …………………………………………………………….. ………………………………………………………………………………………….
Простые вещества – это ……………………………………………………………... ………………………………………………………………………………………….
Обобщите данные о простых и сложных веществах и заполните таблицу: Вещества и их характеристики
____________________________________________________________________ ЗНАТЬ ____________________________________________________________________ Химические элементы и их знаки. ЗНАТЬ ___________________________________________________________________
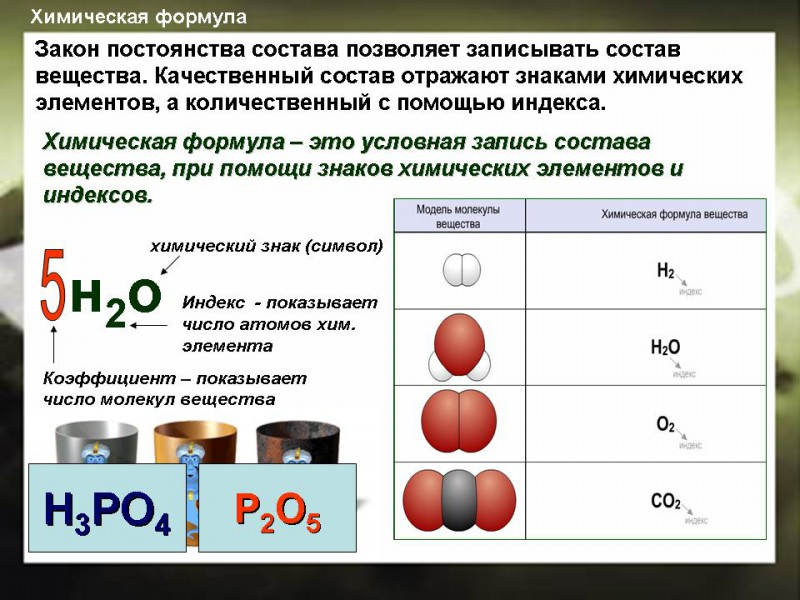
Химические формулы. Относительная молекулярная масса вещества. Массовая доля.
Относительная молекулярная масса обозначается буквой - Мr, является безразмерной величиной и вычисляется следующим образом: Мr (Н2 О) = 2 х А r (Н) + А r (О) = 1х2 + 16 = 18.
Массовая доля – это отношение массы атомов элемента, входящего в состав химического соединения, к массе молекулы данного вещества. Она выражается в - % или в массовых долях, и обозначается греческой буквой - ω ( омега).
n(э) х А r (э) ω (э) = ---------------------- х 100% Мr (вещества)
ω (э) – массовая доля элемента n (э) – число атомов элемента
____________________________________________________________________ САМОСТОЯТЕЛЬНАЯ РАБОТА ____________________________________________________________________ Опишите качественный и количественный состав молекул следующих веществ: Na2CO3 - cода, Cl2 - хлор, Al 2 (SO4)3 - сульфат алюминия. …………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
Чему равны массовые доли элементов в следующих веществах: NH3, N2O, HCl, P2O5, K2S, CuO. ………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….
Сколько химических элементов встречается в природе? ……………………………………………………………………………………………………………………………………………………………………………………. Какие химические элементы наиболее распространены: а) в земной коре; б) в морской воде? …………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
Напишите, как произносятся следующие формулы: HCl…………………………………………………………………………………….
H2SO4 …………………………………………………………………………………..
NaNO3 …………………………………………………………………………………
Mg (NO3)2……………………………………………………………………………… ____________________________________________________________________ ЗНАТЬ ____________________________________________________________________
III II Например: Al O Ø находим наименьшее кратное число выражающее валентность обоих элементов: 2х3 = 6; Ø Это число делим на валентность каждого элемента: 6:3=2; 6:2=3; Ø определим отношение атомов – 2:3; Ø эти индексы проставим рядом с элементами и записываем формулу оксида алюминия - Al2O3. _______________________________________________________________ _ ____ ЗАПОМНИ
Образец оформления решения задачи с объяснением:
Задача: Вычислите массовую долю фосфора в оксиде фосфора (V). Дано: Решение: 1) находим относительную молекулярную массу оксида фосфора (V): Р2 О5 Мr(Р2О5) = 2Аr(Р) + 5 Аr(О) = 2х31 + 5х16 = 142. ω -? 2) вычисляем массовую долю фосфора в данном оксиде:
Ответ: ω(Р) = 43,7% ____________________________________________________________________
Задача: Выведите простейшую формулу соли, если известны массовые доли элементов, входящих в состав: К – 39,69%; Mn – 27.87%; O – 32,46%. Дано: Решение: ω (К)- 39,69% 1) находим отношение атомов. Для этого массовые ω (Mn)-27,87% доли каждого элемента делим на его атомную массу: ω (O) – 32,46% Аr(К) = 39; Аr(Mn)= 55; Аr(O)=16.
найти формулу Кх Mnу Oz -? 2) в формулах веществ отношение количества атомов представляет собой отношение целых чисел, поэтому полученные дроби делим на наименьшее число и получаем:
3) подставляем в формулу вместо обозначений х: у: z их численные значения: К2 Mn O4 Ответ: Формула соли- К2 Mn O4 ____________________________________________________________________ УМЕТЬ
Решите задачу: 1. Вычислите массовые отношения элементов, входящих в состав следующих веществ: а) Н2 О; б) СаО; в) Са(ОН)2 ………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………..
2. В формулах соединений: а) СаСО3; б) С2 Н5 ОН; в) Аg NO3; г) NaClO3 рассчитайте массовую долю кислорода. …………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….. …………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… 3. Напишите формулы водородных соединений следующих элементов, согласно их валентности: а) фосфора (III) ………………………………………………………… б) кремния (IV)……………………………………………… в) хлора (I)…………………………………………………... г) серы (II)……….…………………………………………… 4. Определите валентность всех элементов в следующих соединениях: H2 S; H2 SO4 ; NaOH; FeSO4; H3 PO4; CrBr3; FeCl2; CuO; PH3; B2 O3. над символами элементов напишите значения валентности. 5. Относительная молекулярная масса кислородного соединения серы в два раза больше относительной молекулярной массы молекулы кислорода. Определите формулу этого удушливого газа. …………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………………………………………………………….. 6. Определите формулу серосодержащей кислоты, если массовые отношения водорода, серы и кислорода равны 1:16:32 …………………………………………… ………………………………………………………………………………………………………………………………………………………………………………………………………….. ____________________________________________________________________ 9 ЗНАТЬ
Состав.
Зная атомное отношение элементов в формуле, можно вычислить……………… ......................................................................................................................................... Пример: Рассмотрим образование оксида магния (MgO) из магния и кислорода. Из формулы оксида магния видно, что на 1 атом магния приходится 1 атом кислорода. Зная атомные массы магния и кислорода можно определить, в каких массовых отношениях соединяются между собой эти элементы: т (Mg): т (O) = 56а.е.м.: 32 а.е.м. = 56г:32г = 7:4 Ar (Mg): Ar (S) = 56: 32 = 7:4 ____________________________________________________________________ ЗНАТЬ
ЗНАТЬ
Количество вещества. Моль. САМОСТОЯТЕЛЬНАЯ РАБОТА
1. Образец вещества массой 6,6г содержит 9,03 х 1023молекул. Определите молярную массу этого вещества. …………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………. 2. Количество вещества сульфида натрия Na2S равно 0,6 моль. Определите массу натрия, необходимого для получения данного образца сульфида. ………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….. 3. На одной чаше весов находится 30г мела СаСО3. Если на другую чашу положить серу в количестве 1 моль, уравновесятся ли весы, если нет, то какого вещества больше. ………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….. 4. Заполните таблицу:
5. Сколько будет весить 1 моль комаров, если один комар весит 0,2г……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….. _________________________________________________________________ ЗНАТЬ
Типы химических реакций.
Реакции соединения – это………………………………………………………………… ……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….. Реакции разложения – это ……………………………………………………………....... ……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… Реакции замещения – это ………………………………………………………………… ……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… Реакции обмена – это ……………………………………………………………………… ……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….. Самостоятельно заполните таблицу: а) реакции разложения малахита, б) взаимодействия алюминия с раствором хлорида меди, в) реакцию между растворами сульфата меди и гидроксида натрия, г) сжигание фосфора
_______________________________________________________________ УМЕТЬ
Задание на закрепление усвоенных знаний: Расставить коэффициенты и определить тип реакции:
CaCO3 = Ca + CO2 …………………………........................................................
H2 + O2 = H2O……………………………………………………..........................
Zn + H2SO4 = ZnSO4 + H2………………………………………..........................
NaCl + AgNO3 = NaNO3 + AgCl ……………………………………………….
H2 + Cl2 = HCl ……………………………………………………………………..
CaBr2 + Cl2 = CaCl2 + Br2........................................................................................
H2SeO4 = H2O + SeO3 ……………………………………………........................
H2S + K2O = K2S + H2O ………………………………………………………..... Дописать уравнения реакций и определить их тип: III II Al + O2 = Al O ……………………………………………………………………
III II Fe O + H2 = Fe + H2O ……………………………………………………………
II II II II IV II Zn S + O2 = Zn O + S O ………………………………………………………... I I III I Al + H Cl = Al Cl + H2 ……………………………………………………………...
III II I I III I Fe O + H Cl = Fe Cl + H2O ……………………………………………………...
III II II II Fe O + C = Fe + C O …………………………………………………………….
____________________________________________________________________ УМЕТЬ
Решение разноуровневых задач: А. 1. Найти массу Al2O3 по уравнению: 4Al + 3O2 = 2Al2O3, если объем кислорода равен 11,2 литра……………………………………………………………………………… ……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… 2. Найти количество вещества HCl по уравнению: H2 + Cl2 = 2HCl, если объем водорода равен 44,8 литра. ………………………………………………………. ……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… 3. Найти количество вещества FeCl3 по уравнению реакции: 2Fe + 3Cl2 = 2FeCl3, если масса железа равна 5,6 грамм………………………… ……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… 4. Найти объем, количество вещества и количество молекул 440 граммов СО2. ……………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
5. Состав вещества выражен формулой SO3. Определите: ………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………. ____________________________________________________________________ УМЕТЬ В. 1. В 160 г образца соединения содержится 128 г меди и 32 г кислорода. Установите формулу соединения……………………………………………………........ ………………………………………………………………………………………………………………………………………………………………………………………………………… 2. Составить формулы соединений элемeнтов: K (I); Al (III); Mg (II); S (IV); As (V)с каждым из элементов: O (II); F (I); C (VI); N (III). ………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… 3. Заполните таблицу:
4.Какая масса HCl потребуется для реакции с 5 молями NaOH по уравнению: NaOH + HCl = NaCl + H2O……………………………………………………………… …………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… 5. Какой объем водорода получится из 8 граммов кальция в реакции: H2SO4 + Ca = CaSO4 + H2. ………………………………………………………………...... …………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… 6. Дополнительное задание - определить валентности:
Fe2O3, SO2, SO3, Cl2O7, Cr2O3, NH3, CH4
____________________________________________________________________ УМЕТЬ
1. Заполните таблицу. 2. Какой объем H2S выделяется в реакции: Zn + H2SO4 = H2S + ZnSO4, если в реакции участвует 3 моль H2SO4…………………………………………………………............................... …………………………………………………………………………………………………………………………………………………………………………………………………………..…………………………………………………………………………………………………..……………………………………………………………………………………………………........................... Найти массу, количество вещества и объем, занимаемый 9,03х1023 молекул NO.…………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………............................................................................... 4. Масса золы составляет 1,2% от массы сожженного дерева, а массовая доля кальция в золе равна 25%. Вычислить массу магния в дереве массой 700 кг. …………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………........ Составить формулы оксидов (бинарных соединений с двухвалентным кислородом) и хлоридов (бинарных соединений с одновалентным хлором) серы (IV) и (VI), азота (I), (II), (III), (IV) и (V), марганца (I), (II), (IV), (V) и (VII). …………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………….. Найдите ошибку. I II IV I V I I V II IV Ag2O, FeO, Fe2O3, N2O, SO2, CaO, Mn2O7, RuO4 ____________________________________________________________________
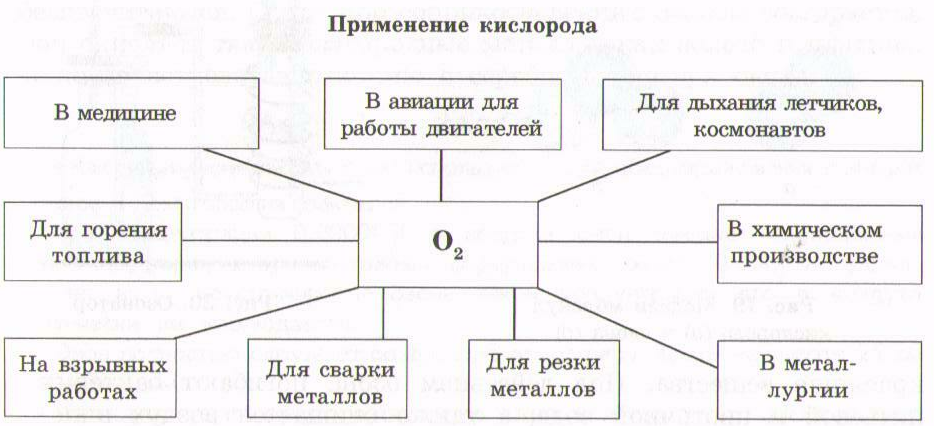
ЗНАТЬ КИСЛОРОД. ОКСИДЫ. ГОРЕНИЕ.
Лавуазье Антуан Лоран Французский химик. Один из основоположников классической химии. Ввел в химию строгие количественные методы исследования. Получил кислород. Доказал сложный состав атмосферного воздуха, содержащего кислород и «удушливый воздух» (азот). Доказал сложный состав воды, установив, что она состоит из кислорода и водорода. Ø Кислород – «оxygenium» – рождающий кислоты. Ø O2 – газообразное вещество, молекула которого имеет кратные связи, (O=O). Ø Горение – это реакции, при которых происходит окисление веществ с выделением тепла и света. Ø Оксиды – это сложные вещества, состоящие из двух элементов, один из которых кислород.
____________________________________________________________________ УМЕТЬ
1. Опишите химические и физические свойства кислорода и напишите уравнения соответствующих реакций: ………………………………………………….. ………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
Li + O2 = СН4 + О2 =
Cu + O2 = С2Н5ОН + О2 =
Н2S + O2 = NH3 + O2 =
2. Составьте уравнения реакций, с помощью которых можно осуществить следующие превращения: KClO3 → O2 → CO2 → O2 → H2O → O2 → P2O5 …………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………. 3. Какую роль играет кислород в жизни живых организмов? …………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………................................................ 4. Какое явление называется аллотропией?............................................................ ........................................................................................................................................................................................................................................................................................................................................................................................................................ 5. Какие инертные элементы содержатся в составе воздуха?............................ ....................................................................................................................................................................................................................................................................................................................................................................................................................... 6. Какие газы опасные газы могут присутствовать в воздухе и какие меры защиты предлагаете?.................................................................................................. .......................................................................................................................................................................................................................................................................................................................................................................................................................... ____________________________________________________________________ ЗНАТЬ
ЗНАТЬ Нормальные условия (н.у.)
УМЕТЬ
Практические задачи При решении практических задач необходимую информацию найдите в учебнике.
Задание к этапу актуализации знаний: I. Найти массу, количество молекул 5 моль Mg2C. Найти количество вещества, количество молекул 9,8 г. H2SO4. II. Найти количество вещества, количество молекул 440 г CO2. Найти массу, количество молекул 6 моль SO3.
Задания для закрепления усвоенных знаний (фронтальная работа): · Найти объем, занимаемый 3 моль СО2 (5 моль Н2). · Найти массу 40 л СО2 (50 л О2).
Задания для индивидуальной работы для закрепления усвоенных знаний:
Заполнить таблицу
____________________________________________________________________ УМЕТЬ
Задание на закрепление усвоенных знаний: · Плотность газа по воздуху 2. Какова его молярная масса? · Плотность газа по гелию 0,5. Какова его молярная масса? · Соединение фосфора с водородом имеет такую же плотность, что и сероводород H2S. Найдите его формулу. · Плотность паров цинка по водороду 33. Каков состав молекулы цинка? · Плотность паров фосфора по водороду 62. Найдите его формулу. · Сколько атомов в молекулах серы при 500 Со и 1160 Со, если плотность паров серы при этих условиях соответственно равны 6,62 и 2,2. · Легче или тяжелее воздуха NH3? · Найдите массу 20 см3 гелия. · Сколько молекул находятся в 560 мл SO2? · Какой воздух тяжелее: сухой или влажный?
Вычисления по уравнениям реакций: 1. В реакцию: 2NO + O2 = 2 NO2 вступило 78,4 литра NO. Какой объем кислорода при этом вступило в реакцию? 2. В реакцию: CuO + H2SO4 = CuSO4 + H2O вступило 8 грамм CuO. Сколько грамм CuSO4 при этом образуется? 3. Относительная плотность газа равна 15. Найдите его относительную плотность по воздуху, и плотность в г/л. 4. Определите объем, который занимают 0,07 кг азота N2 при 210 С и давлении 142 кПа. 5. Из нижеследующих реакций определите экзотермические и эндотермические реакции:
N2 + 3H2 = 2 NH2 + 92 кДж Н2 + Сl2 - 185 кДж = 2 HCl
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-20; просмотров: 481; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.38 (0.009 с.) |