
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Элюотропные ряды органических растворителей
На слой адсорбента вблизи основания пластинки тонким капилляром наносят капли образцов (2−10 мкл) в виде 0,1−1,0%-ных растворов анализируемых веществ в летучих растворителях. Линию старта отмечают на пластинке тонкозаточенным карандашом, не повреждая слой адсорбента, на расстоянии 1,5−2,0 см от основания пластинки. Расстояние между точками нанесения должно быть не менее 1−2 см. Диаметр пятна не должен превышать 3 мм. Растворы наносят в виде круглых пятен или коротких узких полосок, осторожно прикасаясь капилляром к поверхности пластинки, и дают раствору впитаться в слой адсорбента. Пластинку основанием вниз помещают в наклонном положении в герметически закрывающуюся стеклянную камеру, на дне которой находится элюент высотой 5−7 мм. Линия старта с нанесенными образцами должна находиться несколько выше уровня элюента в камере. Камеру закрывают стеклянной крышкой для лучшего насыщения ее парами элюента. Элюент под действием капиллярных сил передвигается по слою адсорбента снизу вверх, увлекая за собой компоненты анализируемой смеси. В результате многократного повторения актов адсорбции и десорбции компоненты смеси в соответствии со своими коэффициентами распределения передвигаются с различной скоростью по мере подъема элюента и распределяются по дискретным зонам, образуя пятна. Как только растворитель дойдет до линии фронта, отстоящей от верхнего края пластинки на ~5 мм, пластинку вынимают из камеры, отмечают карандашом линию фронта и высушивают на воздухе до полного испарения подвижной фазы.
Затем проводят проявление хроматограмм с использованием методов, позволяющих сделать бесцветные пятна разделенных веществ видимыми. Дискретные зоны веществ обнаруживают при рассмотрении хроматограммы в УФ-свете с длиной волны 254 нм (при использовании для элюирования адсорбента с флюорогеном – неорганическим флуоресцентным индикатором), а также после обработки хроматограммы парами йода или после ее опрыскивания растворами реагентов, дающих цветное окрашивание с компонентами смеси. При полном разделении каждое пятно на пластинке соответствует индивидуальному веществу. Положение пятна разделенного вещества определяют посредством измерения величины его подвижности Rf (rate – скорость; fraction – фракция):
где Rf – подвижность вещества; А – расстояние, пройденное веществом от линии старта до середины пятна, см; В – расстояние, пройденное подвижной фазой от линии старта до линии фронта, см. Величина А не может быть больше величины В, поэтому значения Rf лежат в пределах от 0 до 1. Величина Rf для каждого индивидуального вещества в данных условиях хроматографирования (подвижная и неподвижная фазы, температура) – величина постоянная. Качественный анализ компонентов смеси проводят на основании сравнения значений подвижности Rf анализируемых веществ с табличными данными или со значениями Rf, полученными для стандартных веществ («свидетелей») при хроматографировании их вместе с исследуемыми образцами. Стандартные вещества наносят на линию старта пластинки отдельными пятнами по обе стороны от ряда пятен исследуемых веществ. Последний метод является единственным надежным методом качественного анализа соединений, позволяющим избежать влияния различных факторов на значения Rf. ТСХ - анализ липидов. Используют готовые хроматографические пластинки Silufol. Для изучения влияния полярности элюента на Rf индивидуальных липидов в качестве подвижной фазы применяют смеси изопропилового спирта и гексана в различных соотношениях. Проявление хроматограмм осуществляют, обрабатывая их парами йода.
Лабораторная работа
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-27; просмотров: 165; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.225.31.159 (0.005 с.) |
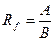 , (5.1)
, (5.1)


