
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Определение, классификация, строение спиртов и гомологический ряд
  «ОН» - функциональная группа спиртов и фенолов. В фенолах она связана с углеродом ароматического ядра, в спиртах – с любым углеродным атомом. СН3 – СН2ОН – этиловый спирт
Одноатомные спирты имеют общую формулу R – OH, или Ar – (СН2)n- OH,
Номенклатура. Изомерия 3 2 1 4 3 2 1
Способы получения Гидратация алкенов СН2 = СН2 + Н2О → + Н2О → СН3 - СН2ОН СН2= СН - СН3ОН → СН3 – СН – СН3 | OH В промышленности гидратация олефинов проводится двумя способами: при участии серной кислоты сернокислотная гидратация и прямая гидратация. СН2 = СН2 + НОSO2OH → СН3 - СН2 – ОSO2ОН СН3 - СН2– ОSO2ОН + Н2О → СН3 - СН2ОН + H2SO4 Прямую гидратацию проводят в одну стадию:
 СН3 - СН2ОН СН3 - СН2ОН
2)

| OH Восстановление кислот и сложных эфиров
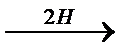 R – СН2ОН R – СН2ОН
R – СН2ОН + R1 – OH
4) Гидролизом галогеналкилов при нагревании с водой раствором щелочей (в первом случае реакция обратима) HOH С2Н5OH + HCl С2Н5Cl NaOH С2Н5OH + NaCl
Действием металлорганических соединений на альдегиды и кетоны
ОMgJ

+ СН3MgJ →СН3 – СН СН3 – СН – СН3 +MgJ(OH) | | СН3 OH
C = O+ СН3MgJ →СН3 – СН - СН3 СН3 – СН – СН3 +MgJ(OH) | | | СН3 СН3 СН3
Получение спиртов брожением (этилового и бутилового) С6Н12OH → 2 СО2 + 2С2Н5OH

Химические свойства Химическое поведение определяется в первую очередь наличием в их молекуле функциональной группы ОН.
Также для спиртов характерны реакции отщепления (элиминирования). Окисления, дегидратации. Положение гидроксильной группы ОН и молекулярная масса существенно влияет на химическое поведение спиртов. Реакции с разрывом связи О-Н.
Образование алкоголятов. Спирты – очень слабые кислоты, но взаимодействуя с металлами (K, Na,Mg, Al), образуют алкоголяты: 2СН3 → СН2ОН +2Na →СН3 - СН2ОNa + Н2↑ СН3 - СН2ОNa + HOH →СН3 - СН2ОH + NaOH Легче всего замещается атом водорода в металле. Труднее в третичных спиртах. Образование сложных эфиров. Реакция этерификации
 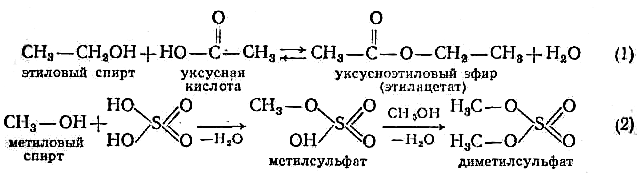 
  Первичные спирты реагируют быстрее вторичных, вторичные быстрее третичных. Первичные спирты реагируют быстрее вторичных, вторичные быстрее третичных.
Легче, чем с кислотами, спирты образуют сложные эфиры при взаимодействии с хлорангидридами и ангидридами кислот.

+ СН3OH → СН3 – С - СН3 + HCl



+ СН3OH → СН3 – С - СН3 +
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-28; просмотров: 481; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.102.225 (0.009 с.) |


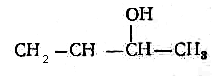
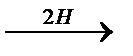 СН3 - СН2ОН
СН3 - СН2ОН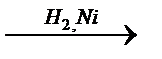
 Н2С =О + СН3MgJ →СН3 - СН2ОMgJ СН3 - СН2ОН +MgJ(OH)
Н2С =О + СН3MgJ →СН3 - СН2ОMgJ СН3 - СН2ОН +MgJ(OH) + R1 – OH
+ R1 – OH



