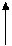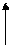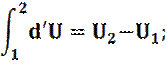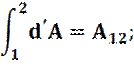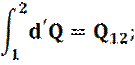Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Кинетическая и потенциальная энергия тела как целого не входит во внутреннюю энергию.
Внутренняя энергия термодинамической системы тел слагается из внутренней энергии взаимодействия между телами и внутренней энергии каждого тела. Работа термодинамической системы над внешними телами заключается в изменении состояния этих тел и определяется количеством энергии, которую термодинамическая система передает внешним телам. Теплота - это количество энергии, представляемое системой внешним телам при теплообмене. Работа и теплота не являются функциями состояния системы, а функцией перехода из одного состояния в другое. Термодинамической системой – называют такую систему, совокупность макроскопических тел, которые могут обмениваться энергией между собой и с внешней средой (с другими телами) (Например, жидкость и находящийся над ней пар). Термодинамическая система характеризуется параметрами:
Состояния системы, когда хотя бы один из параметров изменяется, называется неравновесными. Термодинамические системы, которые не обмениваются с внешними телами энергией, называются замкнутыми. Термодинамический процесс – переход системы из одного состояния (P1,V1,T1) в другое (P2,V2,T2) – нарушение равновесия в системе.
2. Первое начало термодинамики. Количество теплоты, сообщенное системе, идет на приращение внутренней энергии системы и на совершение системой работы над внешними телами. Первый закон термодинамики - это специальный случай закона сохранения энергии, учитывающий внутреннюю энергию системы: Q=U2-U1+A; U1, U2 - начальное и конечное значения внутренней энергии тела. A - работа, совершаемая системой. Q - Количество теплоты, сообщаемое системе. В дифференциальном виде: d DU - есть полный дифференциал, и он зависит от разности начального и конечного состояния системы. d d
d Первое начало термодинамики - невозможен вечный двигатель первого рода, то есть двигатель, который совершал бы работу в большем количестве, чем получаемая им извне энергия.
- не зависит от пути интегрирования.
- зависит от пути интегрирования функции процесса и нельзя записать: A2 - A1; Q2 - Q1; A, Q - не являются функциями состояния. Нельзя говорить о законе работы и теплоты. Это и есть не что иное, как закон сохранения энергии.
3. Изопроцессы. 1) Изохорический процесс: V=сonst; Процесс при нагревании газа в замкнутом объеме. d pdV=0; d
|
||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-28; просмотров: 163; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.224.184.149 (0.006 с.) |
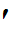 Q=dU+d
Q=dU+d