
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Опыт 22. Ионизиция кислот в водных растворах.
В 6 пробирок налейте по 3-5 капель 0,2 молярных растворов кислот в следующем порядке: муравьиная, уксусная, соляная, щавелевая, салициловая, бензойная. К каждой из них добавьте по 2 капли водного раствора метилового оранжевого. Перемешайте содержимое пробирок и сравните изменение тона окраски индикатора в растворах кислот (чем сильнее кислота, тем розовее окрашен раствор). ОПЫТ 23. ОБРАЗОВАНИЕ СОЛЕЙ. Раствор уксусной кислоты разливают в 2 пробирки. В одну бросают кусочек Zn (можно Fe, Sn), в другую –кусочек мела. К отверстиям каждой пробирки подносят горящую лучинку. Что наблюдаем? Написать уравнения реакций. ОПЫТ 24. ПОЛУЧЕНИЕ УКСУСНО- из О -АМИЛОВОГО ЭФИРА. В пробирку наливают 0,5 мл изо -амилового спирта, 0,5 уксусной кислоты и 0,5 мл концентрированной серной кислоты. Нагревают на водяной бане и выливают в стаканчик с водой. Уксусно- изо -амиловый эфир имеет приятный запах грушевой эссенции. Записать наблюдения и реакции. Вопросы и упражнения. 158. Привести примеры 3-х представителей альдегидов жирного ряда и 2-х представителей ароматического ряда. Назвать. 159. Привести примеры 3-х представителей кетонов жирного и ароматического ряда. Назвать. 160. Написать реакцию с гидроокисью меди и аммиачным раствором окиси серебра для муравьиного и капронового альдегида. 161. Написать отличительные реакции для пропаналя и ацетона. 162. Напишите структурные формулы и назовите изомерные альдегиды и кетоны состава С5Н10О. 163. Напишите структурные формулы следующих соединений: 2-метилпропаналь; 2-метилпентаналь; 2,3-диметилбутаналь; 2,2,4-триметилпентаналь; пентанон-3-аль-1. 164. Какие основные методы получения альдегидов и кетонов Вы знаете? 165. Какие исходные дигалогенпроизводные используют для получения альдегидов, а какие для кетонов? 166. Напишите уравнения реакций и назовите альдегиды (или кетоны), образующиеся при окислении хромовой смесью следующих соединений: а) диэтилкарбинола; б) 3-метилбутанола-2; в) пентанола-3; 2,2-диметилбутанола-1. 167. При окислении 10 мл метанола (d= 0,8г/см3)получено 120 г раствора с массовой долей 3% формальдегида. Каков выход альдегида в процентах. 168. Укажите, из каких дибромпроизводных могут быть получены следующие вещества: а) этилизобутилкетон; б) метилпропилкетон; в) масляный альдегид. Напишите структурные формулы этих веществ.
169. Расскажите о строении карбонильной группы. В чем сходство и различие связей С=О и С=С? 170. Почему альдегиды активнее кетонов? 171. Приведите примеры реакций присоединения в ряду альдегидов и кетонов. Какая закономерность прослеживается при протекании этих реакций? 172. Какие соединения называются полуацеталями? Напишите их структурные формулы в общем виде. 173. Как окислить альдегид? Напишите уравнение реакции "серебряного зеркала". 174. Что такое альдольная и кротоновая конденсации? Приведите пример. 175. Напишите уравнения реакций взаимодействия пропионового альдегида со следующими веществами: а) аммиачным раствором окиси серебра; б) NН3; в) NaНSО3; г) НСN; д) Н2N- ОН; е) H2N-NH2. 176. Какие массы аммиака и формальдегида необходимы для получения 105 г уротропина? 177. Какой продукт и какая масса образуется при действии избытка водорода на 100 г пропионового альдегида? 178. Укажите, какое сходство, и какие различия в химическом поведении альдегидов и кетонов. 179. Какой объем ацетилена, и воды требуется для получения уксусного альдегида массой 90 г с массовой долей 98% по реакции Кучерова. 180. Почему ацетон широко используется в производстве метилметакрилата? 181. Какой продукт и какая масса образуется при действии избытка водорода на 44 г уксусного альдегида? 182. Какими химическими реакциями можно отличить муравьиный альдегид от уксусного альдегида? 183. Напишите структурную формулу ванилина и предложите схему получения из бензола. 184. Какими химическими реакциями можно обнаружить муравьиный альдегид и ацетон? 185. Что Вы знаете о муравьином альдегиде? 186. Напишите альдольную конденсацию для уксусного альдегида. 187. Объясните, почему бензойный альдегид окисляется кислородом воздуха, в отличие от альдегидов жирного ряда? 188. Написать по 2 гомолога одно- и двухосновных кислот с 5-ю и 6-ю атомами углерода. Назвать по тривиальной и женевской номенклатуре. 189. Написать уравнение диссоциации на ионы муравьиной и пропионовой кислот. 190. Написать реакцию нейтрализации уксусной кислоты аммиаком. Написать реакции, которые следует ожидать при нагревании уксуснокислого аммония.
191. Написать реакции получения сложных эфиров из янтарной кислоты и этилового спирта. 192. Написать реакцию получения ангидридов уксусной, масляной и о -фталевой кислот. 193. Объяснить уменьшение растворимости кислот в воде с ростом углеводородной части молекулы и увеличение растворимости в воде с увеличением основности кислот. 194. Приведите примеры образования амидов и хлорангидридов карбоновых кислот на примере капроновой килоты. 195. Распределите карбоновые кислоты по увеличению их кислотности: уксусная, монохлоруксусная, аминоуксусная, трихлоруксусная и бензойная кислоты. 196. Напишите структурные формулы следующих соединений:
197. Приведите все структурные изомеры карбонильных соединений: алифатического ряда C4H8O; ароматического ряда C8H8O. 198. Получите следующие альдегиды и кетоны окислением спиртов и гидролизом дихлорзамещенных углеводородов: метилизопропилкетон; пропионовый альдегид; фенилуксусный альдегид. Напишите уравнения реакций. 199. Какие методы используются для введения альдегидной группы в ароматическое ядро? Ответ иллюстрируйте уравнениями реакций, в каждом случае оговаривая условия их проведения. 200. Какие соединения образуются при восстановлении и окислении метилэтилкетона, изомасляного альдегида, бензальдегида, бензофенона? 201. Приведите реакции уксусного альдегида, в которых участвует водород при α-углеродном атоме. Чем обусловлена активность этого атома водорода? Почему неактивен водород альдегидной группы? 202. Напишите реакцию бромирования ацетона. Каков механизм данной реакции? 203. Приведите реакции, характеризующие особые свойства муравьиного альдегида по сравнению с его гомологами. 204. Предложите химические реакции, позволяющие отличить масляный альдегид от метилэтилкетона. 205. Напишите схемы реакций, являющихся общим для ароматических и жирных альдегидов на примере бензальдегида и пропионового альдегида. 206. Осуществите следующие превращения, напишите уравнения реакции. Назовите полученные продукты:
207. Осуществите следующие превращения, напишите уравнения реакции. Назовите полученные продукты:
208. Осуществите следующие превращения, напишите уравнения реакции. Назовите полученные продукты:
209. Осуществите следующие превращения, напишите уравнения реакции. Назовите полученные продукты:
210. Осуществите следующие превращения, напишите уравнения реакции. Назовите полученные продукты:
211. Осуществите следующие превращения, напишите уравнения реакции. Назовите полученные продукты: 210.




  CH3Cl CO + HCl [H] SOCl2 NH3 CH3Cl CO + HCl [H] SOCl2 NH3
AlCl3 AlCl3 212. Как влияет на свойства спиртов увеличение количества гидроксильных групп в их молекуле? 213. Окисление альдегидов, кетонов, спиртов. Какими реакциями можно подтвердить легкость окисления альдегидов? Приведите схему одной из них.
214. Как называются продукты присоединения синильной кислоты к альдегидам? 215. Напишите структурные формулы следующих соединений:
216. Осуществите следующие превращения, напишите уравнения реакций и назовите полученные соединения:
3) Mg СO2 [HCl] [O] >t°
     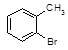 абс. эфир -MgBrCl абс. эфир -MgBrCl
217. Объясните, почему уксусная кислота кипит при более высокой температуре, чем этиловый спирт? 218. Напишите уравнения реакции пропионовой и салициловой кислот со следующими реагентами: а) NaOH; б) NH4OH; в) NaHCO3; г) Ca (OH)2 219. Приведите схемы реакций и механизмы кислотного и щелочного гидролиза этилацетата. 220. Напишите схему реакции гидролиза следующих производных кислот: а) хлорангидрида масляной кислоты; б) ангидрида уксусной кислоты; в) амида бензойной кислоты; г) этилформиата. 221. Исходя из бензола, предложите схемы синтеза всех изомерных: а) нитробензойных кислот; б) хлорбензойных кислот. 222. Из изомасляной кислоты получите: а) ангидрид; б) амид; в) изо -пропиламид. 223. Предложите пути синтеза следующих органических соединений:
O
O
O CH3
ЛАБОРАТОРНАЯ РАБОТА № 5
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 357; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.21.162.87 (0.022 с.) |
 СH3 – CH3 – H2 №1 HBr №2 OH - №3 [O] №4
СH3 – CH3 – H2 №1 HBr №2 OH - №3 [O] №4
 С2Н2 НОН №1 [H] №2 H2SO4(к) №3
С2Н2 НОН №1 [H] №2 H2SO4(к) №3


 H2SO4 (к.) №1 сплав. NaOH №2 CH3I №3
H2SO4 (к.) №1 сплав. NaOH №2 CH3I №3

 а) CH3 – C – NH2
а) CH3 – C – NH2 б) CH3 – CH2 – C – NH – CH3
б) CH3 – CH2 – C – NH – CH3
 в) CH3 – CH2 – C – N-CH3
в) CH3 – CH2 – C – N-CH3


