
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Комплексонометрия. Определение жесткости воды
Основная реакция: Na2H2V + Me2+ →Na2MeV + 2H+ V4- – анион этилендиаминтетрауксусной кислоты
РАБОТА № 8 Определение жесткости воды Реагенты Сульфат магния MgSO4; 0,01 н раствор (первичный стандартный раствор) Комплексон III; 0,05 н раствор (титрант). Аммонийная буферная смесь. Индикатор – кислотный хром темно-кислый 1. Приготовление первичного стандартного раствора MgSO4 Стандартный раствор 0,01 н MgSO4 готовят по фиксаналу. Для этого содержимое ампулы количественного через воронку смывают дистиллированной водой из промывалки в мерную колбу емкостью 1000 мл, доводят раствор до метки и тщательно перемешивают. 2. Установление концентрации раствора комплексона III Концентрацию комплексона III устанавливают по первичному стандартному раствору сульфата магния. Раствор комплексона III (титранта) наливают в бюретку и устанавливают уровень жидкости на нуле. В коническую колбу емкостью 250 мл пипеткой отмеривают 20 мл стандартного раствора MgSO4, добавляют 20 мл дистиллированной воды, 5 мл аммонийной буферной смеси и 5 капель индикатора. Раствор перемешивают и медленно титруют раствором титранта до перехода розовой окраски в синюю. Титрование повторяют 2-3 раза. Находят среднее значение, по которому рассчитывают точную концентрацию титранта по формуле:
3. Определение жесткости воды Полученный для анализа раствор жесткой воды в мерной колбе емкостью 100 мл разбавляют дистиллированной водой до метки и тщательно перемешивают. В коническую колбу емкостью 250 мл пипеткой отмеривают 20 мл жесткой воды, добавляют 20 мл дистиллированной воды, 5 мл аммонийного буферного раствора, 5 капель индикатора и титруют раствором комплексона III до перехода розовой окраски в синюю. При титровании идет следующая реакция: Na2H2V + Ca2+ = Na2CaV +2H+ По результатам титрования вычисляют жесткость воды по формуле: Жесткость = Вопросы для самопроверки 1. На чем основана классификация титриметрических методов анализа? Привести примеры. 2. Первичные и вторичные стандартные растворы. 3. Что означает титр раствора по определяемому веществу и как он связан с нормальной концентрацией титранта? 4. Что лежит в основе расчетов результатов титриметрического анализа? 5. На титрование 20,00 мл раствора содержащего сульфат железа (II) затрачено 18,54 мл 0,02 н раствора перманганата калия. Вычислить нормальность раствора сульфата железа (II) и титр перманганата калия по железу. 6. Как рассчитать эквивалентные массы окислителя и восстановителя в редоксиметрии?
|
|||||||||||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 726; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.135.190.232 (0.004 с.) |
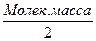 (для всех веществ)
(для всех веществ)
 синий Титрование ведут в присутствии буферных растворов
синий Титрование ведут в присутствии буферных растворов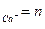 Компл. III ЭМ =
Компл. III ЭМ = 
 , мг – экв/л
, мг – экв/л


