
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Квантовые числа. Движение электрона в атоме. Атомная орбитальСтр 1 из 4Следующая ⇒
Генетическая связь
CaSO4
Металл - группа элементов, в виде простых веществ обладающих характерными металлическими свойствами, такими как высокие тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск. Неметалл - химические элементы с типично неметаллическими свойствами, которые занимают правый верхний угол Периодической системы Оксид - бинарное соединение химического элемента с кислородом в степени окисления −2, в котором сам кислород связан только с менее электроотрицательным элементом. К исключениям относятся, например, дифторид кислорода OF2. Гидроксиды - соединения металлов с водой. Известны гидроксиды почти всех химических элементов; некоторые из них встречаются в природе в виде минералов. Гидроксиды щелочных металлов называются щелочами. Гидроксиды имеют вид: Me(OH)x Кислота - химические соединения, способные отдавать катион водорода (кислоты Брёнстеда) либо соединения, способные принимать электронную пару с образованием ковалентной связи (кислоты Льюиса) Соль - это сложные вещества, которые в водных растворах диссоциируют на катионы металлов и анионы кислотных остатков. ИЮПАК определяет соли как химические соединения, состоящие из катионов и анионов. Есть ещё одно определение: солями называют вещества, которые могут быть получены при взаимодействии кислот и оснований с выделением воды
Номенклатура Названия простых веществ Простые вещества называют, как правило, так же, как и соответ-ствующие элементы. Свои собственные названия имеют только ал-лотропные модификации углерода (алмаз, графит, карбин, фуллере-ны) и вторая модификация кислорода (озон). При названиях алло-тропных модификаций остальных элементов обычно указывают ее краткую физическую характеристику (белый, красный, черный фосфор, кристаллическая и пластическая сера, серое и белое олово и т. д.). Бинарные соединения В формулах двухэлементных соединений, состоящих из металла и неметалла, символ металла записывают на первом месте, то есть слева, а символ неметалла – справа. В соединениях из двух металлов или неметаллов первым записывают символ того элемента, ко-торый стоит в периоде развернутой Периодической системы левее, а в группе – ниже. Исключение составляют благородные газы, помещаемые как бы в нулевую группу и начинающие этот условный ряд и водород, который в этом ряду неметаллов традиционно помещают между элементами V и VI групп. Кислород записывают на первом месте только в соединениях со фтором. Примеры: MnI2, FeO, CuAl2, FeNi3, XeO4, CH4, AsH3, H2S, BrF3, ClO2, OF2. Названия бинарных соединений составляют из двух слов. В русском языке первым словом обозначают более электроотрицательный элемент (реальный или условный анион), составляя его из латинского корня названия элемента с окончанием -ид, вторым сло-вом является русское название менее электроотрицательного эле-мента (реального или условного катиона) в родительном падеже:
NaCl -хлорид натрия; B2O3-оксид бора; Al2S3-сульфид алюминия; Mg3N2-нитрид магния.
В случае, если менее электроотрицательный элемент имеет несколько положительных степеней окисления, в названии следует указать либо его степень окисления, либо число атомов аниона, используя числовые приставки:
FeCl3 –х лорид железа(III); FeCl2 - дихлорид железа; SF6 - гексафторид серы; SF4 - фторид серы(IV); PbO2 - диоксид свинца; PbO- оксид свинца(II); Pb3O4 - оксид свинца (II, IV); N2O4 - тетраоксид азота. В последнем примере однозначность написания формулы по названию обусловлена отсутствием у азота степени окисления (VIII). Если соединение содержит катионы нескольких металлов или анионы нескольких неметаллов, то при написании формулы придерживаются того же порядка, как и в случае соответствующих бинарных соединений, а называют вещество справа налево, используя дефис: SnBrCl3 -трихлорид-бромид олова; KNaCl2 - хлорид натрия-калия; Cu2Cl2O - оксид-хлорид меди(II); CaTiO3 - оксид титана(IV)-кальция;
Кислородсодержащие кислоты Названия этого класса соединений строятся из группового слова «кислота» и прилагательного, которое составляется из русского корня названия элемента, окончания -ая- и суффиксов, указывающих, насколько степень окисления кислотообразующего элемента отличается от максимальной.
Для высшей или единственной степени окисления применяют суффиксы -н-, -ов-, -ев-: H3BO3 - борная кислота; H2CO3 - угольная кислота; H2SiO3 - кремниевая кислота; H2CrO4 - хромовая кислота; HNO3 - азотная кислота; HPO3 - метафосфорная кислота; HReO4 - рениевая кислота; H3PO4 - ортофосфорная кислота. Приставки орто- и мета- применяют, чтобы различать названия кислот, молекулы которых отличаются только «содержанием воды». Если возможны две степени окисления, то для низшей используют суффиксы -ист-, -овист-: H2SeO3 - селенистая кислота; H2TeO3 - теллуристая кислота; HAsO2 - метамышьяковистая кислота; H3AsO3 - ортомышьяковистая кислота. В случае трех возможных степеней окисления кислотообразующего элемента, помимо упомянутых суффиксов, для самой низкой (обычно +1) применяется составной суффикс -новатист-: H3PO2 - фосфорноватистая кислота; H2N2O2 - азотноватистая кислота. В названиях кислот с четырьмя различными степенями окисления последовательно используют суффиксы -н-, -новат-, -ист- и -новатист-: HClO4 - хлорная кислота; HClO3 - хлорноватая кислота; HClO2 - хлористая кислота; HClO3 - хлорноватистая кислота. Для того, чтобы различить кислоты, содержащие разное количе-ство атомов кислотообразующего элемента в одной степени окис-ления, применяют числовые приставки: H2Cr2O7 - дихромовая кислота; H2Cr3O10 - трихромовая кислота; H2S2O5 - дисернистая кислота; Оксокислоты, в которых атомы кислорода замещены на атомы серы (частично или полностью) или на пероксогруппы (-О-О-), по-лучают к своему названию приставку соответственно тио- или пероксо- (по необходимости, с числовой приставкой): H2S2O3 (H2SO3S) - тиосерная кислота; H2CS3 - тритиоугольная кислота; HNO4 (HNO2(O2)) - пероксоазотная кислота; H2S2O8 (H2S2O6(O2) - пероксодисерная кислота. Название солей Название солей неорганических соединений состоят из традиционных названий катионов и анионов. Если элемент в образуемых им оксоанионах проявляет одну степень окисления, то название аниона оканчивается на -ат: (NH4)2CO3 - карбонат аммония; K4SiO4 - ортосиликат калия; NaBiO3 - висмутат натрия; LiBO2 - метаборат лития. В случае двух степеней окисления ещё используют окончание -ит: BaSeO4 - селенат бария; FeAsO4 - ортоарсенат железа(III); BaSeO3 - селенит бария; Fe(AsO2)2 - метаарсенит железа(II). Если степеней окисления элемента в анионах может быть более двух, то для самой низкой (обычно +1) применяют приставку гипо- с окончанием -ит: Na2N2O2 - гипонитрит натрия; Названия анионов, образованных элементом в степени окисления +7, имеют приставку пер- и окончание -ат: H3OClO4 - перхлорат оксония; KMnO4 - перманганат калия; Ag5IO6 - ортопериодат серебра; SrIO4 - метапериодат стронция.
&3. Строение ядра. Квантовые числа.
А́том (от др.-греч. ἄτομος — неделимый) — частица вещества микроскопических размеров и массы, наименьшая часть химического элемента, являющаяся носителем его свойств Атом состоит из атомного ядра и электронов. Если число протонов в ядре совпадает с числом электронов, то атом в целом оказывается электрически нейтральным. В противном случае он обладает некоторым положительным или отрицательным зарядом и называется ионом. В некоторых случаях под атомами понимают только электронейтральные системы, в которых заряд ядра равен суммарному заряду электронов, тем самым противопоставляя их электрически заряженным ионам Ядро, несущее почти всю (более чем 99,9 %) массу атома, состоит из положительно заряженных протонов и незаряженных нейтронов, связанных между собой при помощи сильного взаимодействия. Атомы классифицируются по количеству протонов и нейтронов в ядре: число протонов Z соответствует порядковому номеру атома в периодической системе Менделеева и определяет его принадлежность к некоторому химическому элементу, а число нейтронов N — определённому изотопу этого элемента. Число Z также определяет суммарный положительный электрический заряд (Ze) атомного ядра и число электронов в нейтральном атоме, задающее его размер. Атомы различного вида в разных количествах, связанные межатомными связями, образуют молекулы.
Строение атома Первой научной гипотезой о строении атома, опирающейся на новые открытия, была модель, предложенная Томсоном. Обращение к построению атома было вызвано открытием электрона, являющегося составной частью всех атомов. Кроме того, явление радиоактивности говорило о том, что оно зависит от "изменений, происходящих в атомах радиоактивных веществ". В своей модели Томсон развивает теорию строения атома, предложенную в 1902 г. Уильямом Томсоном в статье "Эпинус атомизированный". У Томсона атом представляет собой сферу, равномерно заряженную положительным электричеством, в центре которой помещен электрон. Томсон опирается на эту модель и предлагает свою. Модель Томсона представляла собой равномерно заряженную положительным зарядом сферу, в которой вращались или покоились электроны (корпускулы, как их называл Томсон). Поскольку атом в целом нейтрален, то общий заряд электронов равен положительному заряду сферы. Объем сферы гораздо больше объема корпускулы. Электроны вращаются по круговым орбитам, расположенным на различных расстояниях от центра сферы, зависящих от скорости электронов. При некоторой скорости корпускулы достигают поверхности сферы, а дальнейшее увеличение скорости заставляет их покидать сферу. Это означает, что атом распался. Томсон заключает, что атом устойчив тогда, когда кинетическая энергия корпускул не превышает некоторой предельной величины.
Модель Томсона не была свободна от недостатков. Главным из них был вопрос о распределении положительного заряда в атоме, размерах положительно заряженной сферы. Томсон знал об этом слабом месте своей модели. К 1904 году японский физик Нагаока разработал раннюю, ошибочную «планетарную модель» атома («атом типа Сатурна»). Модель была построена на аналогии с расчётами устойчивости колец Сатурна (кольца уравновешены из-за очень большой массы планеты). Модель Нагаоки была неверна, но два следствия из нее оказались пророческими: ядро атома действительно очень массивно; электроны удерживаются на орбите благодаря электростатическим силам (подобно тому, как кольца Сатурна удерживаются гравитационными силами). Модели атома Томсона был нанесен удар исследованиями Резерфорда и его учеников по рассеянию а- частиц в 1911 году. Суть этих исследований заключалась в следующем. Поток а-частиц, испускаемых радием, пропускался через маленькое отверстие в трубку с откаченным из нее воздухом. На небольшом расстоянии от отверстия находился сернистоцинковый экран. При ударе о него а-частиц получалось изображение светлого пятна. При закрывании отверстия тонкой металлической пластинкой изображение светлого пятна на экране несколько размывалось, т.е. а-частицы рассеивались веществом металлической пластинки. Изучение рассеяния показало, что небольшое число а-частиц (примерно 1/8000) отклонялось на угол больше 90°. Модель Томсона не допускала таких больших отклонений. Математический расчет показывал, что такие большие отклонения могут происходить, если а-частицы попадают под влияние сильных электрических полей, существующих вокруг зарядов, сконцентрированных в очень малом объеме. Электрическое поле, создаваемое положительно заряженной, размытой по всему объему атома сферой, не могло оказывать такого сильного влияния на а-частицу, и ее столкновение с электроном не могло повлиять на траекторию движения, поскольку масса а-частицы почти в 8000 раз больше массы электрона. Поэтому Резерфорд приходил к выводу, что почти вся масса атома сосредоточена в положительно заряженном ядре. Вокруг него, как планеты вокруг Солнца, вращаются электроны. Модель атома Резерфорда - новый этап в развитии физики атома.
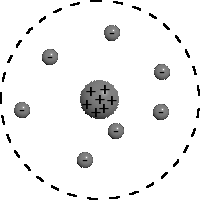
Бо́ровская моде́ль а́тома (Моде́ль Бо́ра) — полуклассическая модель атома, предложенная Нильсом Бором в 1913 г. За основу он взял планетарную модель атома, выдвинутую Резерфордом. Однако, с точки зрения классической электродинамики, электрон в модели Резерфорда, двигаясь вокруг ядра, должен был бы излучать непрерывно и очень быстро, потеряв энергию, упасть на ядро. Чтобы преодолеть эту проблему Бор ввел допущение, суть которого заключается в том, что электроны в атоме могут двигаться только по определенным (стационарным) орбитам, находясь на которых они не излучают, а излучение или поглощение происходит только в момент перехода с одной орбиты на другую. Причем стационарными являются лишь те орбиты, при движении по которым момент количества движения электрона равен целому числу постоянных Планка.
А.Зоммерфельд дополнил модель Бора предложив, что электроны вращаются вокруг ядра по эллиптической орбите (1915 г.) Постулаты Бора Постулаты Бора — основные допущения, сформулированные Нильсом Бором в 1913 году для объяснения закономерности линейчатого спектра атома водорода и водородоподобных ионов (формула Бальмера-Ридберга) и квантового характера испускания и поглощения света. Бор исходил из планетарной модели атома Резерфорда. Первый постулат: Атомы имеют ряд стационарных состояний соответствующих определенным значениям энергий: Е1, Е2...En. Находясь в стационарном состоянии, атом энергии не излучает и не поглощает, несмотря на движение электронов. Второй постулат: В стационарном состоянии атома электроны движутся по стационарным орбитам, для которых выполняется квантовое соотношение: m•V•r = n•h/2•p где m•V•r =L - момент импульса, n=1,2,3...,h-постоянная Планка. Третий постулат: Излучение или поглощение энергии атомом происходит при переходе его из одного стационарного состояния в другое. При этом излучается или поглощается порция энергии (квант), равная разности энергий стационарных состояний, между которыми происходит переход: ε= h• ν= Em-En
Достоинства теории Бора · Объяснила дискретность энергетических состояний водородоподобных атомов. · Теория Бора подошла к объяснению внутриатомных процессов с принципиально новых позиций, стала первой полуквантовой теорией атома. · Эвристическое значение теории Бора состоит в смелом предположении о существовании стационарных состояний и скачкообразных переходов между ними.. Недостатки теории Бора · Не смогла объяснить интенсивность спектральных линий. · Справедлива только для водородоподобных атомов и не работает для атомов, следующих за ним в таблице Менделеева. · Теория Бора логически противоречива: не является ни классической, ни квантовой. В системе двух уравнений, лежащих в её основе, одно — уравнение движения электрона — классическое, другое — уравнение квантования орбит — квантовое.
Общие положения. Молекулы химических веществ представляют собой сложную систему атомных ядер и электронов. Атомы в молекуле удерживаются преимущественно силами электростатического характера. В этом случае говорят, что они связаны химической связью. Химическая связь осуществляется s- и p-электронами внешнего и d-электронами предпоследнего слоя. Эта связь характеризуется следующими параметрами: 1. Длиной связи – межъядерным расстоянием между двумя химически связанными атомами. 2. Валентным углом – углом между воображаемыми линиями, проходящими через центры химически связанных атомов. 3. Энергией связи – количеством энергии, затрачиваемой на ее разрыв в газообразном состоянии. 4. Кратностью связи – числом электронных пар, посредством которых осуществляется химическая связь между атомами. Атом в молекуле – понятие условное, т. к. его энергетическое и электронное состояние в корне отличается от изолированного атома. Если мы будем сближать два протона, то между ними возникнут силы отталкивания, и о получении устойчивой системы говорить не приходится. В образовании химической связи участвуют s-, p- и d-электроны, имеющие различную геометрическую конфигурацию электронных облаков и различные знаки волновых функций в пространстве. В зависимости от симметрии электронных облаков, в результате перекрывания которых образуется химическая связь, суммарное электронное облако будет иметь различную симметрию, в соответствии с которой они распадаются на три вида: σ-, π- и δ- связи. σ-связь осуществляется при перекрывании облаков вдоль линии, соединяющей центры атомов, при этом максимальная электронная плотность достигается в межъядерном пространстве и имеет цилиндрическую симметрию относительно линии, соединяющей центры атомов. Как видно из рис. 2.4., в образовании σ-связи в силу своей шаровой симметрии всегда принимают участие s-электроны. Они образуют σ -связь в результате перекрывания со следующими электронами другого атома: s-, рХ-, d(x2-y2)-электронами. Возможность образования σ-связи s-электронами не исчерпывается, она может образоваться в случае перекрывания и других электронных облаков, таких, как двух pX или pX и d(x2-y2).
Рис.2.4. Некоторые примеры образования σ-связей.
Рис. 2.5. Примеры π- и δ -связей.
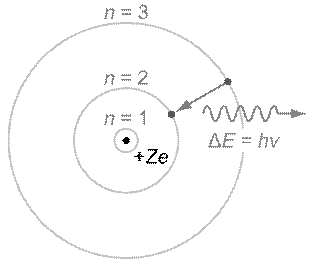
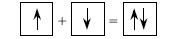
π -связи возникают при перекрывании электронных облаков над и под линией, соединяющей центры атомов. Суммарные электронные облака также симметрично расположены относительно этой оси, но они не имеют цилиндрической симметрии, как в случае σ-связи. В силу своего пространственного расположения π-связь образуют электроны на таких парах орбиталей как pY – pY, pZ – pZ, pY – dXY. δ -связь образуют только d-электроны за счет перекрывания всех четырех своих лепестков электронных облаков, расположенных в параллельных плоскостях. Такое возможно, когда в образовании связиучаствуют dXY – dXY, dXZ – dXZ, dYZ – dYZ-электроны. Выше была рассмотрена классификация химических связей, исходя из симметрии электронных облаков. Существует и другой подход к классификации химической связи, основанный на характере распределения электронной плотности между атомами в молекуле, т. е. химическая связь рассматривается с точки зрения принадлежности электронной пары тому или иному атому. Возможны три случая: 1) Электронная пара связывает в молекуле два одинаковых атома. В этом случае она в равной мере принадлежит им обоим. В молекуле нет разделения центров тяжести положительного и отрицательного зарядов. Они совпадают, и такая связь называется ковалентной неполярной. 2) Если же электронная пара связывает два различных атома, то она смещается в сторону более электроотрицательного атома. Центры тяжестиположительного и отрицательного зарядов разделяются, связь становитсяполярной и носит название ковалентной полярной связи. 3) Третий случай связан с полной передачей электронной пары во владение одного из атомов. Это происходит при взаимодействии двух атомов, резко отличающихся по электроотрицательности, т. е. способности удерживать электронную пару в своем электрическом поле. При этом атом, отдавший электроны, становится положительно заряженным ионом, а атом, принявший их, – отрицательным. В этом случае связь носит название ионной. Характер связи во многом определяет физико-химические свойства веществ. Метод валентных связей В методе валентных связей химическая связь рассматривается как двухэлектронная и двухцентровая, т. е. пара электронов, образующих связь, локализована в пространстве между двумя атомами и находится в их общем пользовании. Возможны два механизма образования общей электронной пары. Первый называется обменными заключается в спаривании двух электронов, принадлежащих разным атомам и имеющим противоположные спины. Его можно выразить следующей схемой:
Второй механизм, называемый донорно-акцепторным, приводит к образованию химической связи за счет предоставления одним атомом в общее пользование пары электронов, а другим – свободной орбитали. Атом, предоставляющий электронную пару, называется донором, а атом, имеющий свободную орбиталь, – акцептором. Схема образования связи в этом случае выглядит так:
Для элементов второго периода происходит распаривание s-электронов и переход их на p-подуровень c образованием новых уровней, на которых энергии электронов, находящихся уже на орбиталях другого типа, одинаковы. А раз это так, то по правилу Хунда, в атоме появляется максимальное число неспаренных электронов. Эта гипотеза получила название явления гибридизации, а орбитали, образующиеся в результате усреднения энергий подуровней, называются гибридными. Естественно, что при этом меняются и форма электронных облаков, и их расположение в пространстве. В зависимости от того, какие орбитали участвуют в образовании гибридных орбиталей, рассматривают различные типы гибридизации и пространственные конфигурации образовавшихся гибридных орбиталей. Число получившихся гибридных орбиталей должно быть равно общему числу орбиталей, вступивших в гибридизацию. В зависимости от того, какие орбитали взаимодействуют между собой, рассматривают несколько типов гибридизации: sp-гибридизация. В этом явлении принимают участие s- и одна p-орбитали, и в результате образуются две орбитали нового типа, которые называются sp-гибридными. Эти орбитали имеют форму, показанную на рисунке, оси их лежат на одной прямой, образуя угол 1800. В образовании связей в молекуле BeH2 принимают участие sp-гибридные орбитали атома бериллия и молекула имеет линейное строение;
Рис. Пространственное расположение электронных облаков для различных типов гибридизации.
sp2-гибридизация. Во взаимодействие вступают s- и две p-орбитали, в результате чего образуются три орбитали нового типа, которые называются sp2-гибридными. Оси этих орбиталей лежат в одной плоскости, и углы между ними равны 1200. Например, атом бора в молекуле BF3 находится в sp2 -гибридном состоянии, и эта молекула имеет форму правильного треугольника с атомом бора в центре. sp3-гибридизация. В этом случае исходными являются s- и три p- орбитали. В результате гибридизации образуются четыре новые орбитали –sр3-гибридные. Оси этих орбиталей направлены от центра к вершинам тетраэдра, углы между осями равны 109028′. CH4 – молекула метана, где реализуется этот тип гибридизации, имеет тетраэдрическое расположение атомов водорода. В молекуле аммиака (NH3) атом азота тоже находится в sp3-гибридном состоянии, три пары электронов являются общими с атомами водорода и участвуют в образовании связей, а одна электронная пара (неподеленная электронная пара) принадлежит только атому азота. Первый закон термодинамики Первое начало термодинамики было сформулировано в середине XIX века в результате работ немецкого учёного Ю. Р. Майера, английского физика Дж. П. Джоуля и немецкого физика Г. Гельмгольца. Согласно первому началу термодинамики, термодинамическая система может совершать работу только за счёт своей внутренней энергии или каких-либо внешних источников энергии. Первое начало термодинамики часто формулируют как невозможность существования вечного двигателя первого рода, который совершал бы работу, не черпая энергию из какого-либо источника. Существует несколько формулировок первого начала термодинамики В любой изолированной системе запас энергии остаётся постоянным. Количество теплоты, полученное системой, идёт на изменение её внутренней энергии и совершение работы против внешних сил Изменение внутренней энергии системы при переходе её из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе, то есть, оно зависит только от начального и конечного состояния системы и не зависит от способа, которым осуществляется этот переход. Это определение особенно важно для химической термодинамики/ Первое начало термодинамики При изобарном процессе
при изохорном процессе
при изотермическом процессе
Основные понятия Система - любая физически или мысленно выделенная часть окружающей среды.Все, что находится вне системы, называется внешней средой. По способности обмена с внешней средой системы делятся на: Изолированные - не обмениваются с внешней средой ни энергией, ни веществом. Закрытые - обмениваются с внешней средой энергией, но не веществом. Открытые - обмениваются с внешней средой и энергией, и веществом. Теплота (энтальпия) Превращения энергии при химических реакциях. Химические реакции протекают с выделением или с поглощением энергии. обычно эта энергия выделяется или поглощается в виде теплоты. Выделение теплоты при взаимодействии различных веществ заставляет признать, что эти вещества еще до реакции в скрытой форме обладали определенной энергией. Такая форма энергии, скрытая в веществах и освобождающаяся при химических, а также при некоторых физических процессах (например, при конденсации пара в жидкость жгли при кристаллизации жидкости), называется внутренней энергией вещества При некоторых реакциях наблюдается выделение или поглощение лучистой энергии. Обычно в тех случаях, когда при реакция выделяется свет, внутренняя энергия превращается в излучение не непосредственно, а через теплоту. Но известны процессы, в коде которых внутренняя энергия превращается в лучистую непосредственно. Эти процессы носят название холодного свечения или люминесценции. Большое значение имеют процессы взаимного превращения внутренней и электрической энергии. При реакциях, протекающих со взрывом, внутренняя энергия превращается в механическую – частью непосредственно, частью переходя сперва в теплоту. Но известны процессы, в коде которых внутренняя энергия превращается в лучистую непосредственно. Эти процессы носят название холодного свечения или люминесценции. Итак, при химических реакциях происходит взаимное превращение внутренней энергии веществ, с одной стороны, и тепловой, лучистой, электрической или механической энергии, с другой. Реакции, протекающие с выделением энергии, называют экзотермическими, а реакции, при которых энергия поглощается, эндотермическими. Энтропия Энтропия— в естественных науках мера беспорядка системы, состоящей из многих элементов. Понятие энтропии было впервые введено в 1865 году Рудольфом Клаузиусом Вероятность различных состояний вещества (газ, кристаллическое, жидкое) можно описать как некоторое его свойство и количественно выразить значением энтропии S [в Дж/(К*моль)] Зависимость энтальпии и энтропии от температуры
7.3. Закон Гесса (открыт в 1840) Закон Гесса — основной закон термохимии, который формулируется следующим образом: Тепловой эффект реакции зависит только от начального и конечного состояния веществ и не зависит от промежуточных стадии процесса
Практически значимое следствия закона Гесса • Тепловой эффект прямой реакции равен по величине и противоположен по знаку тепловому эффекту обратной реакции (закон Лавуазье — Лапласа). • Тепловой эффект химической реакции равен сумме теплот образования образующихся веществ за вычетом суммы теплот образования исходных веществ умноженные на их стехиометрические коэффициенты. • Если начальное и конечное состояния химической реакции (реакций) совпадают, то её (их) тепловой эффект равен нулю Энергию Гиббса Свободная энергия Гиббса (или просто энергия Гиббса, или потенциал Гиббса, или термодинамический потенциал в узком смысле) — это величина, показывающая изменение энергии в ходе химической реакции и дающая таким образом ответ на вопрос о принципиальной возможности протекания химической реакции; это термодинамический потенциал следующего вида:
Энергию Гиббса можно понимать как полную химическую энергию системы (кристалла, жидкости и т. д.) Понятие энергии Гиббса широко используется в термодинамике и химии. Самопроизвольное протекание изобарно-изотермического процесса определяется двумя факторами: энтальпийным, связанным с уменьшением энтальпии системы (ΔH), и энтропийным T ΔS, обусловленным увеличением беспорядка в системе вследствие роста её энтропии. Разность этих термодинамических факторов является функцией состояния системы, называемой изобарно-изотермическим потенциалом или свободной энергией Гиббса (G, кДж) В химических процессах одновременно действуют два противоположных фактора — энтропийный (
Характер изменения энергии Гиббса позволяет судить о принципиальной возможности осуществления процесса. При Обратите внимание, что речь идёт исключительно о принципиальной возможности протекания реакции. В реальных же условиях реакция может не начинаться и при соблюдении неравенства
История создания В 1798 году Иоганн Вильгельм Риттер указал, что ряд Вольта эквивалентен ряду окисления металлов (т. е. последовательности уменьшения их сродства с кислородом). Таким образом, Риттер высказал гипотезу о возникновении электрического тока вследствие протекания химической реакции В 1812 году Й. Берцелиус на основе электрохимической теории сродства построил классификацию элементов, разделив их на «металлоиды» (сейчас применяется термин «неметаллы») и «металлы» и поставив между ними водород. История создания Последовательность металлов по их способности вытеснять друг друга, давно известная химикам, была в 1860-е и последующие годы особенно основательно и всесторонне изучена и дополнена Н. Н. Бекетовым. Уже в 1859 году он сделал в Париже сообщение на тему «Исследование над явлениями вытеснения одних элементов другими». В эту работу Бекетов включил целый ряд обобщений о зависимости между взаимным вытеснением элементов и их атомным весом, связывая эти процессы с «первоначальными химическими свойствами элементов – тем, что называется химическим сродством»
Практическое использование ряда напряжений
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 500; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.189.177 (0.19 с.) |

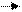 Металл: Ca CaO Ca(OH)2
Металл: Ca CaO Ca(OH)2





 Неметалл: S SO3 H2SO4
Неметалл: S SO3 H2SO4









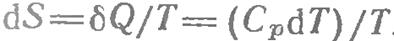



 ) и энтальпийный (
) и энтальпийный ( ). Суммарный эффект этих противоположных факторов в процессах, протекающих при постоянном давлении и температуре, определяет изменение энергии Гиббса (
). Суммарный эффект этих противоположных факторов в процессах, протекающих при постоянном давлении и температуре, определяет изменение энергии Гиббса (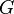 ):
):
 процесс может протекать, при
процесс может протекать, при  процесс протекать не может (иными словами, если энергия Гиббса в исходном состоянии системы больше, чем в конечном, то процесс принципиально может протекать, если наоборот — то не может). Если же
процесс протекать не может (иными словами, если энергия Гиббса в исходном состоянии системы больше, чем в конечном, то процесс принципиально может протекать, если наоборот — то не может). Если же  , то система находится в состоянии химического равновесия.
, то система находится в состоянии химического равновесия. С развитием современных представлений электрохимии (главным образом в работах Вальтера Нернста) стало ясно, что эта последовательность соответствует «ряду напряжений» – расположению металлов по значению стандартных электродных потенциалов
С развитием современных представлений электрохимии (главным образом в работах Вальтера Нернста) стало ясно, что эта последовательность соответствует «ряду напряжений» – расположению металлов по значению стандартных электродных потенциалов


