
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Общая характеристика процессов горения
Горением называется процесс взаимодействия топлива с окислителем, сопровождающийся выделением тепла, а иногда и света. Роль окислителя в подавляющем большинстве случаев выполняет кислород воздуха. Всякое горение предполагает прежде всего тесный контакт между молекулами топлива и окислителя. Поэтому, чтобы происходило горение, необходимо обеспечить этот контакт, т. е. необходимо смешать топливо с воздухом. Следовательно, процесс горения складывается из двух стадий: 1) смешение топлива с воздухом; 2) горение топлива. Во время протекания второй стадии происходят сначала воспламенение, а затем уже и горение топлива, В процессе горения образуется пламя, в котором протекают реакции горения составляющих топлива и выделяется тепло, В технике при сжигании газообразного, жидкого и твердого пылевидного топлив применяют так называемый факельный метод сжигания. Факел - это частный случай пламени, когда топливо и воздух поступают в рабочее пространство печи в виде струй, которые постепенно перемешиваются одна с другой. Поэтому форма и длина факела обычно вполне определенные. При наиболее распространенном в металлургии и машиностроении факельном сжигании топлива аэродинамическую основу процесса составляют струйные течения, исследование которых основано на применении положений теории свободной турбулентности к различным случаям. Поскольку при факельном сжигании характер движения струй может быть ламинарным и турбулентным, в процессах смешения большая роль принадлежит молекулярной и турбулентной диффузии. На практике при создании устройств для сжигания топлива (горелок, форсунок) применяют различные конструктивные приемы (направляют струи под углом друг к другу, создают закручивание струй и др.) с тем, чтобы организовать смешение так, как это необходимо для конкретного случая сжигания топлива. Различают гомогенное и гетерогенное горение. При гомогенном горении тепло-и массообмен протекают между телами, находящимися в одинаковом агрегатном состоянии. Гомогенное горение происходит в объеме и свойственно газообразному топливу. При гетерогенном горении тепло-и массообмен происходят между телами, находящимися в разных агрегатных состояниях (в состоянии обмена находятся газ и поверхность частиц топлива). Такое горение свойственно жидкому и твердому топливам. Правда, при горении жидкого и твердого топлив благодаря испарению капель и выделению летучих есть элементы и гомогенного горения. Однако при гетерогенном процессе в основном идет горение с поверхности.
Гомогенное горение может протекать в кинетической и диффузионной областях. При кинетическом горении полное перемешивание топлива с воздухом осуществляют предварительно, и в зону горения подают заранее подготовленную топливо-воздушную смесь. В этом случае основную роль играют химические процессы, связанные с протеканием реакций окисления топлива. При диффузионном гомогенном горении процессы смешения и горения не разделены и совершаются практически одновременно. В этом случае процесс горения определяется перемешиванием, так как время смешения гораздо больше времени, необходимого для протекания химической реакции. Таким образом, полное время протекания процесса горения складывается из времени смесеобразования (τсм) и времени собственно химической реакции (τх), т. е.
При кинетическом горении, когда смесь приготовлена предвари тельно:
При диффузионном горении, наоборот, время смешения неизмеримо больше времени протекания химической реакции
При гетерогенном горении твердого топлива также различают кинетическую и диффузионную области реагирования. Кинетическая область возникает в том случае, когда скорость диффузии в порах топлива значительно превосходит скорость химической реакции; диффузионная область возникает при обратном соотношении скоростей диффузии и горения. С точки зрения смесеобразования, осуществляемого при помощи газогорелочных устройств, организация процессов сжигания топлива в воздушном потоке может быть осуществлена на основе трех принципов: диффузионного, кинетического и смешанного.
Возникновение пламени
Возникновение пламени (воспламенение топлива) может произойти только после того, как будет достигнут необходимый контакт молекул топлива и окислителя. Любая реакция окисления протекает с выделением тепла. Вначале реакция окисления идет медленно с выделением малого количества тепла. Однако выделяющееся тепло способствует повышению температуры и ускорению реакции, что в свою очередь приводит к более энергичному выделению тепла, которое опять-таки оказывает благоприятное влияние на развитие реакции. Таким образом, происходит постепенное нарастание скорости реакции до момента воспламенения, после чего реакция идет с очень большой скоростью и носит лавинный характер. В реакциях окисления неразрывно связаны друг с другом механизм химической реакции и тепловые характеристики процесса окисления. Первичным фактором является химическая реакция и вторичным - выделение тепла. Оба эти явления тесно связаны между собой и влияют друг на друга.
Установлено, что воспламенение возможно как в изотермических условиях, так и при повышении температуры. В первом случае происходит так называемое цепное воспламенение, при котором скорость реакции нарастает в результате увеличения числа активных центров, возникающих только в результате химического взаимодействия. Чаще воспламенение происходит в неизотермических условиях, когда увеличение числа активных центров происходит в результате как химического взаимодействия, так и термического воздействия. В практических условиях обычно прибегают к искусственному поджиганию топлива, вводя в зону горения определенное количество тепла, что приводит к резкому ускорению момента достижения воспламенения. Температура воспламенения не является физико-химической константой, определяемой только свойствами смеси; она определяется условиями протекания процесса, т. е. характером теплообмена с окружающей средой (температурой, формой сосуда и др.). Температуры воспламенения различных топлив приведены в таблице 5. Таблица. 5 - Температуры воспламенения в воздухе при атмо- сферном давлении.
Кроме температуры, большое влияние на процесс зажигания топлива оказывает концентрация горючей составляющей в смеси, Существуют такие минимальная и максимальная концентрации горючей составляющей, ниже и выше которых вынужденное воспламенение произойти не может. Такие предельные концентрации называются нижними и верхними концентрационными пределами воспламенения; значения их для некоторых газов приведены в таблице 6. Таблица 6 - Пределы воспламенения в воздушных и кислородных смесях при атмосферном давлении и температуре 20оС
Чтобы установить пределы воспламенения промышленных газов, которые являются смесью различных горючих компонентов, пользуются правилом Ле-Шателье, по которому
где Z- искомый нижний или верхний предел воспламенения; Z 1; Z 2; Z 3 - соответствующие пределы воспламенения для горючих компонентов топлива; Р 1; Р2; Р3 - процентное содержание отдельных горючих компонентов в топливе. Если газообразное топливо содержит балласт в виде СО2 и N2, то для определения пределов воспламенения применяют формулу
где σ = СО+ N2 – содержание балласта в горючем газе, %; Zг - пределы воспламенения, рассчитанные для горючей массы газа.
|
|||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-09-18; просмотров: 1281; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.211.66 (0.013 с.) |
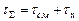 (2.1)
(2.1)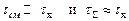
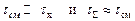
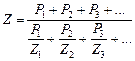 , (2.2)
, (2.2)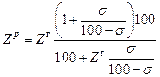 , (2.3)
, (2.3)


