
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Закон теплопроводности Фурье
В установившемся режиме плотность потока энергии, передающейся посредством теплопроводности, пропорциональна градиенту температуры:
где 23. Число степеней свободы: наименьшее число независимых координат, определяющих положение и конфигурацию молекулы в пространстве. Число степеней свободы для одноатомной молекулы - 3 (поступательное движение в направлении трех координатных осей), для двухатомной - 5 (три поступательных и две вращательных, т.к. вращение вокруг оси Х возможно только при очень высоких температурах), для трехатомной - 6 (три поступательных и три вращательных). Теорема о равнораспределении кинетической энергии по степеням свободы, закон равнораспределения, теорема о равнораспределении — связывает температуру системы с её средней энергией в классическойстатистической механике. В первоначальном виде теорема утверждала, что при тепловом равновесии энергия разделена одинаково между её различными формами, например, средняя кинетическая энергияпоступательного движения молекулы должна равняться средней кинетической энергии её вращательного движения.
24. Внутренняя энергия — это кинетическая энергия хаотического (теплового) движения частиц системы (молекул, атомов, ядер, электронов) и потенциальная энергия взаимодействия этих частиц. 25. При изобарном процессе: A=p(V2-V1) A=нюR(T2-T1) При изотермическом процессе: A = нюRT*ln(T2/T1) A=нюRT*ln(p1/p2) 26. Внутренняя энергия тела может изменяться, если действующие на него внешние силы совершают работу (положительную или отрицательную). Например, если газ подвергается сжатию в цилиндре под поршнем, то внешние силы совершают над газом некоторую положительную работу A'. В то же время силы давления, действующие со стороны газа на поршень, совершают работу A = – A'. Если объем газа изменился на малую величину Δ V, то газ совершает работу pS Δ x = p Δ V, где p – давление газа, S – площадь поршня, Δ x – его перемещение.
При расширении работа, совершаемая газом, положительна, при сжатии – отрицательна. В общем случае при переходе из некоторого начального состояния (1) в конечное состояние (2) работа газа выражается формулой:
или в пределе при Δ Vi → 0:
В изохорном процессе (V = const) газ работы не совершает, A = 0. В изобарном процессе (p = const) работа, совершаемая газом, выражается соотношением:
В изотермическом процессе температура газа не изменяется, следовательно, не изменяется и внутренняя энергия газа, Δ U = 0. Первый закон термодинамики для изотермического процесса выражается соотношением Q = A. 27. Теплоёмкость тела (обычно обозначается латинской буквой C) — физическая величина, определяющая отношение бесконечно малого количества теплоты δ Q, полученного телом, к соответствующему приращению его температуры δ T:
Единица измерения теплоёмкости в системе СИ — Дж / К. Удельной теплоёмкостью называется теплоёмкость, отнесённая к единичному количеству вещества. Количество вещества может быть измерено в килограммах, кубических метрах и молях. В зависимости от того, к какой количественной единице относится теплоёмкость, различают массовую, объёмную и молярную теплоёмкость. 28. Первое начало термодинамики — один из трёх основных законов термодинамики, представляет собой закон сохранения энергии для термодинамических систем. Существует несколько эквивалентных формулировок первого начала термодинамики В любой изолированной системе запас энергии остаётся постоянным. Это — формулировка Дж. П. Джоуля (1842 г.). Количество теплоты, полученное системой, идёт на изменение её внутренней энергии и совершение работы против внешних сил Изменение внутренней энергии системы при переходе её из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе, то есть, оно зависит только от начального и конечного состояния системы и не зависит от способа, которым осуществляется этот переход. Это определение особенно важно для химической термодинамики (ввиду сложности рассматриваемых процессов). Иными словами, внутренняя энергия является функцией состояния. В циклическом процессе внутренняя энергия не изменяется.
Изменение полной энергии системы в квазистатическом процессе равно количеству теплоты
29. Молярная теплоемкость — количество теплоты, необходимое для нагревания 1 моль вещества на 1 К: При постоянном объеме работа газа равна нулю ( При постоянном давлении тепло 30. Адиабати́ческий, или адиаба́тный проце́сс (от др.-греч. ἀδιάβατος — «непроходимый») — термодинамический процесс в макроскопической системе, при котором система не обменивается тепловой энергией с окружающим пространством. Для идеальных газов, чью теплоёмкость можно считать постоянной, в случае квазистатического процесса адиабата имеет простейший вид и определяется уравнением [6][15][16]
При адиабатическом процессе показатель адиабаты равен 31. Политропный процесс это процесс, в котором теплоемкость остается постоянной. Политропным процессом являются изохорный, изобарный, изотермический и адиабатный процессы, потому что все они имеют общую особенность - они происходят при постоянной теплоемкости. В первых двух процессах теплоемкости соответственно равны Cv и Cp, в изотермическом процессе (dT=0) теплоемкость равна бесконечности, в адиабатном политропный процесс равна нулю. 32. Обратимые и необратимые процессы, пути изменения состояния термодинамической системы. Процесс называют обратимым, если он допускает возвращение рассматриваемой системы из конечного состояния в исходное через ту же последовательность промежуточных состояний, что и в прямом процессе, но проходимую в обратном порядке. При этом в исходное состояние возвращается не только система, но и среда. Обратимый процесс возможен, если и в системе, и в окружающей среде он протекает равновесно. При этом предполагается, что равновесие существует между отдельными частями рассматриваемой системы и на границе с окружающей средой. Обратимый процесс - идеализированный случай, достижимый лишь при бесконечно медленном изменении термодинамических параметров. Скорость установления равновесия должна быть больше, чем скорость рассматриваемого процесса. Если невозможно найти способ вернуть и систему, и тела в окружающей среде в исходное состояние, процесс изменения состояния системы называют необратимым.
33. Отношение полезной работы, совершенной машиной, к количеству полученного тепла составляет КПД тепловой машины
Понятно, что КПД машины всегда меньше единицы, поскольку не все количество полученного тепла переходит в полезную работу. В реальных тепловых машинах КПД, очевидно, еще меньше, так как часть тепла теряется безвозвратно в процессе работы машины. Для получения максимального КПД следует рассмотреть рабочий цикл, образованный обратимыми процессами. Этому требованию отвечает цикл (см. рис.), впервые рассмотренный французским ученым Карно. В качестве рабочего тела в цикле Карно рассматривается идеальный газ. Цикл Карно состоит из последовательных расширения и сжатия газа, причем каждый из процессов совершается сначала изотермически, а затем адиабатически. При прямом цикле тело по-прежнему сначала получает тепло, а затем отдает его. Достоинство цикла Карно состоит в том, что все процессы обратимы, и, следовательно, КПД такой машины будет максимальным Выражение для КПД цикла Карно:
Из формулы (2.59) следует, что КПД тепловой машины определяется только разностью температур нагревателя и холодильника. КПД не зависит ни от свойств рабочего тела, используемого в машине, ни от свойств самой машины. Полученный результат показывает, что при T1 = T2 КПД машины равен нулю, т. е. машина не совершает работы. Работа максимальна (η = 1) при T2 = 0. Таким образом, машина тем выгоднее, чем ниже температура охладителя. 34. Цикл Карно́ — идеальный термодинамический цикл. Цикл Карно состоит из четырёх стадий: 1. Изотермическое расширение (на рисунке — процесс A>Б). В начале процесса рабочее тело имеет температуру TH, то есть температуру нагревателя. Затем тело приводится в контакт с нагревателем, который изотермически (при постоянной температуре) передаёт ему количество теплоты QH. При этом объём рабочего тела увеличивается. 2. Адиабатическое (изоэнтропическое) расширение (на рисунке — процесс Б>В). Рабочее тело отсоединяется от нагревателя и продолжает расширяться без теплообмена с окружающей средой. При этом его температура уменьшается до температуры холодильника. 3. Изотермическое сжатие (на рисунке — процесс В>Г). Рабочее тело, имеющее к тому времени температуру TX, приводится в контакт с холодильником и начинает изотермически сжиматься, отдавая холодильнику количество теплоты QX.
4. Адиабатическое (изоэнтропическое) сжатие (на рисунке — процесс Г>А). Рабочее тело отсоединяется от холодильника. При этом его температура увеличивается до температуры нагревателя. Цикл Карно
КПД цикла Карно:
Отсюда видно, что КПД цикла Карно с идеальным газом зависит только от температуры награвателя (Tн) и холодильника (Тх). Из уравнения следуют выводы: 1. Для повышения КПД тепловой машины нужно увеличить температуру нагревателя и уменьшить температуру холодильника; 2. КПД тепловой машины всегда меньше 1.
|
|||||||||||
|
Последнее изменение этой страницы: 2016-08-26; просмотров: 580; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.14.121.242 (0.026 с.) |

 — вектор плотности теплового потока — количество энергии, проходящей в единицу времени через единицу площади, перпендикулярной каждой оси,
— вектор плотности теплового потока — количество энергии, проходящей в единицу времени через единицу площади, перпендикулярной каждой оси,  — коэффициент теплопроводности (иногда называемый просто теплопроводностью),
— коэффициент теплопроводности (иногда называемый просто теплопроводностью),  — температура. Минус в правой части показывает, что тепловой поток направлен противоположно вектору grad T (то есть в сторону скорейшего убывания температуры). Это выражение известно как закон теплопроводности Фурье.
— температура. Минус в правой части показывает, что тепловой поток направлен противоположно вектору grad T (то есть в сторону скорейшего убывания температуры). Это выражение известно как закон теплопроводности Фурье.



 , сообщённому системе, в сумме с изменением энергии, связанной с количеством вещества
, сообщённому системе, в сумме с изменением энергии, связанной с количеством вещества 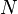 при химическом потенциале
при химическом потенциале  , и работы
, и работы  , совершённой над системой внешними силами и полями, за вычетом работы
, совершённой над системой внешними силами и полями, за вычетом работы  , совершённой самой системой против внешних сил
, совершённой самой системой против внешних сил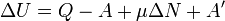 .
. .
. , где
, где — молярная масса (масса одного моля вещества).
— молярная масса (масса одного моля вещества). ) и все полученное тепло идет на увеличение внутренней энергии газа (
) и все полученное тепло идет на увеличение внутренней энергии газа ( ).
). .
. , полученное газом, идет на увеличение внутренней энергии газа
, полученное газом, идет на увеличение внутренней энергии газа  и совершение работы
и совершение работы  над внешними телами:
над внешними телами:  .
. .
. Серьёзное исследование адиабатических процессов началось в XVIII веке [1] .
Серьёзное исследование адиабатических процессов началось в XVIII веке [1] . 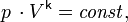
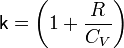 .
. .
.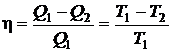 . (2.59)
. (2.59)



