Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Качественное определение кетоновых тел.
В нормальной моче кетоновые тела (ацетон, ацетоуксусная и b-гидроксимасляная кислоты) содержатся в небольших количествах (0,02-0,05 г/сут, или 20-50 мг) и обычными качественными реакциями не обнаруживаются. Повышенная экскреция их с мочой (кетонурия) наблюдается при сахарном диабете (до 10-50 г/сут), голодании, инфекционных заболеваниях (туберкулезе и др.) Проба с нитропруссидом натрия (Легаля) на ацетон При взаимодействии ацетона с нитропруссидом натрия в щелочной среде появляется оранжево-красное окрашивание. После подкисления концентрированной уксусной кислотой оранжево-красное окрашивание переходит в вишневое. В пробирку налить 1 мл мочи и добавить 2 - 3 капли свежеприготовленного раствора нитропруссида натрия и 3 - 4 капли 10% раствора едкого натра. После развития оранжево-красной окраски прилить несколько капель концентрированной уксусной кислоты и отметить изменение цвета раствора в вишневый. Проба Либена на ацетон Проба основана на образовании йодоформа СНI3 при взаимодействии ацетона с I2 в щелочной среде. К 1 мл мочи добавить 3 - 4 капли 10% раствора КОН и по каплям - раствора йода в йодистом калии (раствор Люголя) до появления мути (слабо-желтый кристаллический осадок йодоформа) при наличии ацетона, обладающего специфическим «больничным» запахом. СНз-С-СН3 + 2I2 + 4NаОН —® СНI3 + CH3COONa + 3NaI + 3Н2О êê О К 1 мл мочи добавить 4 - 5 капель 5% раствора FеСl3. Наблюдается вишнево-красное окрашивание за счет комплексного соединения железа с енольной формой ацетоуксусной кислоты, постепенно бледнеющее при стоянии вследствие самопроизвольного декарбоксилирования ацетоуксусной кислоты: СНз-С-СН2СООН —® СН3-С-СН3 + СО2 êê êê О О Качественная реакция на кровяные пигменты. Появление в моче форменных элементов крови (гематурия) или кровяных пигментов (гемоглобинурия) относится к патологии и может быть обнаружено с помощью ряда проб (гваяковой, бензидиновой и др.). Гематурия имеет место при нарушении целостности кровеносных сосудов, повреждении мочеполовых путей (мочевые камни, рак мочевого пузыря); гемоглобинурия наблюдается при отравлении гемолитическими ядами, при ожогах происходит разрушение эритроцитов. Кровяные пигменты можно открыть бензидиновой пробой, которая основана на окислении бензидина атомарным кислородом, который образуется при разложении перекиси водорода кровяным пигментом, моча окрашивается в синий или зеленый цвет.
Проба с бензидином В пробирку налить 1 мл прокипяченной мочи, добавить 4 капли 5% раствора бензидина в ледяной уксусной кислоте (свежеприготовленный) и 4 капли 3% раствора перекиси водорода. После перемешивания жидкость окрашивается в синий или зеленый цвет, что указывает на присутствие крови в моче. Проба гваяковой смолой Налить в пробирку 1 мл исследуемой мочи. В другую пробирку добавить 1 мл 2% раствора гваяковой смолы, туда же добавить 3 - 5 капель 1% раствора перекиси водорода и осторожно наслоить в пробирку раствор, содержащий мочу. При наличии кровяных пигментов отметить появление синего кольца на границе наслаивания. Качественное определение желчных пигментов. Желчные пигменты (билирубин, биливердин и др.) образуются при распаде гемоглобина эритроцитов и появляются в моче при желтухах. Моча, содержащая желчные пигменты, имеет желтовато-коричневое или зеленое окрашивание (характерный признак желтухи). Проба на билирубин с раствором йода (проба Розина) К 3 мл мочи осторожно наслоить 1% спиртовый раствор йода или раствор Люголя. При наличии билирубина на границе между обеими жидкостями образуется зеленое кольцо. С нормальной мочой проба отрицательна. Проба Гмелина на желчные кислоты К 1 мл концентрированной азотной кислоты осторожно по стенке наслоить мочу равный объем. При наличии желчных пигментов на границе наслаивания образуется зеленое кольцо. Проба Петенкофера на желчные кислоты. Реакция основана на конденсации желчных кислот с оксиметилфурфуролом, образующимся под влиянием концентрированной серной кислоты из сахарозы. Продукт конденсации имеет красно-фиолетовую окраску. В пробирку поместить 1 мл мочи добавить 5 капель 5% раствора сахарозы и осторожно по стенке пробирки наслоить 1 мл концентрированной серной кислоты. При наличии желчных кислот на границе наслаивания образуется кольцо красно-фиолетового цвета. Проба Яффе на уробилин.
К 2 мл мочи прибавить небольшую порцию раствора хлористого цинка. При встряхивании появляется хлопьевидный осадок, который растворить в концентрированном растворе аммиака (около 1мл). В норме появляется слабо-зеленая флюоресценция, ярко выраженная при патологии. Качественное определение индикана в моче. Индикан - калиевая или натриевая соль индоксилсерной кислоты - содержится в нормальной моче в виде следов. Много индикана содержится в моче травоядных животных, а также в моче человека при усиленном гниении белков в кишечнике, при запорах и непроходимости кишечника. В пробирку налить 4 мл исследуемой мочи и прибавить при помешивании равный объем серной кислоты. Затем добавить около 1 мл хлороформа, 1 - 2 капли раствора перманганата калия, закрыть пробкой и несколько раз перевернуть, не встряхивая. Пробирку поставить в штатив и наблюдать интенсивность окрашивания хлороформного слоя в синий цвет
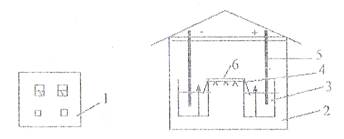
Разделение и количественное определение белковых Фракций сыворотки крови методом электрофореза на бумаге. Принцип метода. Электрофорез – это движение заряженных частиц в поле постоянного электрического тока. Скорость перемещения молекул белков в электрическом поле зависит от величин заряда, молекулярной массы, pH, ионной силы раствора. Белки сыворотки крови помещают на полоску бумаги, смоченную буферным раствором, через которую пропускают постоянный электрический ток. При pH 8,6 белки сыворотки крови заряжаются отрицательно и под воздействием электрического поля перемещаются к аноду. Сыворотка крови человека содержит различные белки. С помощью электрофореза на бумаге выделяются 5 фракций - альбумины, α1-, α2-, β-, γ-глобулины. Клинико-диагностическое значение. Многие патологические состояния сопровождаются количественными изменениями соотношения белковых фракций крови – диспротеинемиями. Уменьшение содержания фракции альбуминов характерно для заболеваний печени за счет снижения белок-синтезирующей функции гепатоцитов. Гипоальбуминемия также сопровождает заболевания почек вследствие потери белка с мочой. Увеличение содержания фракций α1- и α2-глобулинов наблюдается при стрессе, наличии воспалительных процессов за счет белков «острой фазы», при коллагенозах и метастазировании злокачественных новообразований. Фракция β-глобулинов растет при гиперлипопротеинемиях. Фракция γ-глобулинов повышается при иммунных реакциях, вызванных вирусными и бактериальными инфекциями. Снижение γ-глобулиновой фракции может иметь место при первичном и вторичном иммунодефиците. Порядок выполнения работы 1. Устройство прибора для электрофореза. Прибор состоит из выпрямителя, подающего постоянный ток необходимого напряжения, и камеры для электрофореза. Сама камера состоит из 2-х ванн; в одной из них имеется неподвижная перегородка, куда помещается платиновый электрод (+ анод), а в другой находится электрод из нержавеющей стали (- катод). Между ваннами, заполненными соответствующим буфером, имеется соединительный мост, на который помещают полоски специальной фильтровальной бумаги.
2. Проведение электрофореза. Заполнить обе ванны камеры раствором вероналового буфера с pH 8,6. Буферного раствора в ваннах должно быть столько, чтобы он покрывал неподвижную перегородку, но был ниже подвижных перегородок. Вставить в ванны электроды. Вырезать из фильтровальной бумаги полосы необходимого размера в зависимости от величины камеры (обычно шириной 4-6 см) и простым карандашом отметить место, на которое впоследствии будет наноситься сыворотка (старт). Смочить эти полоски в вероналовом буфере. Вставить в ванны-камеры соединительный мост. Поместить полоски бумаги на сухие пластинки щипцами, погрузив концы полосок в ванны с буфером, и на заранее отмеченные участки бумаги нанести сыворотку по 0,025-0,005 мл на расстоянии 5-6 см от края моста. Нанесение сыворотки производится со стороны катода.
Рисунок 1. Схема камеры для электрофореза белков на бумаге: 1-стабилизатор; 2-камера для электрофореза; 3-буферный раствор; 4-поддерживающий соединительный мост-электрод; 5-фильтровальная бумага для электрофореза. После нанесения на бумажные полоски сыворотки камера герметично закрывается крышкой. На крышке камеры расположен прижим блокировки, служащий для включения камеры. Присоединенный выпрямитель подает к камере постоянный ток от 2 до 4 мА при постоянном напряжении 110-160В. Электрофорез проводят при градиенте потенциала от 3 до 8 В на 1 см полосы при комнатной температуре. Хорошее разделение происходит за 18-20 часов. 3. Выключение прибора и выявление белковых фракций. Выключают прибор. Снимают камеры и извлекают бумажные полоски из прибора. Затем каждую полоску помещают в сушильный шкаф на 20 минут при температуре 1050С. При этом происходит фиксация белковых фракций на бумаге. Окраску белков проводят раствором бромфенолового-синего в течение 30 минут, затем промывают электрофореграммы 2% раствором уксусной кислоты. Полученные электрофореграммы сушат на воздухе. Белковые фракции окрашиваются в сине-зеленый цвет. 4. Количественное определение белковых фракций. Окрашенные белковые пятна вырезают, краситель элюируют 0,01 н раствором щелочи. Интенсивность окраски каждой фракции определяют колориметрически на ФЭКе. Количественное определение белковых фракций на электрофореграмме можно установить двумя способами: путем элюирования краски и фотоколориметрирования и денситометрическим методом.
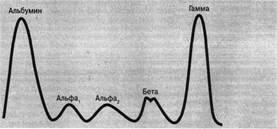
Содержание белковых фракций сыворотки крови, полученное с помощью электрофореза на бумаге, в среднем составляет у взрослого человека: альбумины 55,4-65,9 % α1-глобулины 3,4-4,7 % α2-глобулины 5,5-9,5 % β-гдобулины 8,9-12,6 % γ-глобулины 13-22,2 % Денситометрический метод. В специальном аппарате (денситометре) через электрофореграмму пропускают пучок света, поглощение которого зависит от оптической плотности окрашенных белковых пятен. Свет, прошедший через электрофореграмму, улавливается фотоэлементом и превращается в электрический ток, колебания которого фиксируют на бумажном листе в виде кривой, каждый пик кривой соответствует определенной белковой фракции.
Рисунок 2. Электрофореграмма сыворотки человека.
|
||||||||
|
Последнее изменение этой страницы: 2016-08-26; просмотров: 403; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.138.175.180 (0.022 с.) |