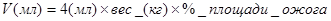Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Сопровождающихся нарушениями кровообращения
Гиповолемический шок Гиповолемический шок вызывается острой потерей крови, плазмы или жидкостей организма. Гиповолемия (снижение объема крови — ОЦК) приводит к уменьшению венозного возврата и снижению давления наполнения сердца (ДНС). Это в свою очередь ведет к снижению ударного объема сердца (УОС) и падению артериального давления (АД). Вследствие стимуляции симпатоадреналовой системы возрастает частота сердечных сокращений (ЧСС) и возникает вазоконстрикция (рост периферического сопротивления — ОПСС), что позволяет поддерживать центральную гемодинамику и вызывает централизацию кровообращения. При этом существенное значение в централизации кровотока (наилучшее снабжение кровью сердца, мозга и легких) имеет преобладание α-адренорецепторов в сосудах, иннервируемых n. splanchnicus, а также в сосудах почек, мышц и кожи. Такая реакция организма вполне оправданна, но если гиповолемия не корригируется, вследствие недостаточной тканевой перфузии развивается картина шока. Для гиповолемического шока, таким образом, характерно снижение ОЦК, снижение давления наполнения сердца и сердечного выброса, снижение артериального давления и возрастание периферического сопротивления. Кардиогенный шок Наиболее частой причиной кардиогенного шока является острый инфаркт миокарда, реже миокардит и токсическое поражение миокарда. При нарушении насосной функции сердца, аритмии и других острых причинах падения эффективности сердечных сокращений происходит снижение УОС. Вследствие этого возникает снижение АД, в то же время возрастает ДНС из-за неэффективности его работы. В результате опять таки стимулируется симпатоадреналовая система, возрастает частота сердечных сокращений и периферическое сопротивление. Изменения в принципе сходны с таковыми при гиповолемическом шоке и вместе с ними относятся к гиподинамическим формам шока. Патогенетическое различие заключается лишь в значении ДНС: при гиповолемическом шоке оно снижено, а при кардиогенном — повышено. Анафилактический шок Анафилактическая реакция является выражением особой повышенной чувствительности организма к инородным субстанциям. В основе развития анафилактического шока лежит резкое снижение сосудистого тонуса под воздействием гистамина и других медиаторных субстанций.
Вследствие расширения емкостной части сосудистого русла (вены) развивается относительное снижение ОЦК: возникает несоответствие между объемом сосудистого русла и ОЦК. Гиповолемия приводит к уменьшению обратного кровотока к сердцу и снижению ДНС. Это ведет к уменьшению УОС и АД. Снижению производительности сердца способствует и прямое нарушение сократительной способности миокарда. Характерным для анафилактического шока является отсутствие выраженной реакции симпатоадреналовой системы, этим во многом объясняется прогрессивное клиническое развитие анафилактического шока. Септический шок При септическом шоке первичные расстройства касаются периферии кровообращения. Под влиянием бактериальных токсинов открываются короткие артериовенозные шунты, через которые кровь устремляется, обходя капиллярную сеть, из артериального русла в венозное. При этом возникает ситуация, когда при уменьшении поступления крови в капиллярное русло кровоток на периферии высок и ОПСС снижено. Соответственно снижается АД, компенсаторно увеличивается УОС и ЧСС. Это так называемая гипердинамическая реакция циркуляции при септическом шоке. Снижение АД и ОПСС происходит при нормальном или увеличенном УОС. При дальнейшем развитии гипердинамическая форма переходит в гиподинамическую, что ухудшает прогноз. Сравнительная характеристика нарушений гемодинамики
Несмотря на различие в патогенезе представленных форм шока, финалом их развития является снижение капиллярного кровотока. Вследствие этого доставка кислорода и энергетических субстратов, а также выведение конечных продуктов обмена становятся недостаточными. Развивается гипоксия, характер метаболизма изменяется от аэробного в сторону анаэробного. Меньше пирувата включается в цикл Кребса и переходит в лактат, что наряду с гипоксией приводит к развитию тканевого метаболического ацидоза.
Под влиянием ацидоза возникают два феномена, приводящие к дальнейшему ухудшению микроциркуляции при шоке: 1. шоковая специфическая вазомоция: прекапилляры расширяются, тогда как посткапилляры еще сужены. Кровь устремляется в капилляры, а отток нарушен. Повышается внутрикапиллярное давление, плазма переходит в интерстиций, что приводит как к дальнейшему снижению ОЦК, так и к нарушению реологических свойств крови 2. нарушение реологических свойств крови: происходит агрегация клеток в капиллярах. Эритроциты склеиваются в монетные столбики, образуются глыбки тромбоцитов. В результате повышения вязкости крови создается почти непреодолимое сопротивление току крови, образуются капиллярные микротромбы, развивается диссеминирующее внутрисосудистое свертывание крови. Так центр тяжести изменений при прогрессирующем шоке все больше перемещается от макроциркуляции к микроциркуляции. Нарушение функции клеток, их гибель вследствие нарушения микроциркуляции при шоке могут касаться всех клеток организма, но определенные органы особенно чувствительны к циркуляторному шоку. Такие органы называются шоковыми. К шоковым органам человека относят в первую очередь легкие и почки, во вторую очередь — печень. При этом следует различать изменения этих органов при шоке (легкое при шоке, почки при шоке, печень при шоке), которые прекращаются при выводе больного из шока, и органные нарушения, связанные с разрушением тканевых структур, когда после выхода из шока остается недостаточность или полное выпадение функции органа (шоковое легкое, шоковые почки, шоковая печень). Легкое при шоке характеризуется нарушением поглощения кислорода и распознается по артериальной гипоксии. Если развивается шоковое легкое (респираторный дистресс-синдром), то после устранения шока быстро прогрессирует тяжелая дыхательная недостаточность, снижается парциальное давление кислорода в артериальной крови, уменьшается эластичность легкого, и оно становится все более неподатливым. Начинает повышаться парциальное давление углекислоты на столько, что становится необходимым все больший объем дыхания. В этой прогрессирующей фазе шока синдром шокового легкого, по-видимому, уже не подвергается обратному развитию: больной погибает от артериальной гипоксии. Почки при шоке характеризуются резким ограничением циркуляции крови и уменьшением количества гломерулярного фильтрата, нарушением концентрационной способности и уменьшением количества выделяемой мочи. Если эти нарушения после устранения шока не подверглись немедленному обратному развитию, то еще больше снижается диурез и увеличивается количество шлаковых субстанций — развивается шоковая почка, основным проявлением которой является клиническая картина острой почечной недостаточности. Печень является центральным органом обмена веществ и играет важную роль в течение шока. Развитие шоковой печени можно заподозрить, когда уровень печеночных ферментов возрастает и после купирования шока.
ГИПОВОЛЕМИЧЕСКИЕ ШОКИ Особенностьюгиповолемии при геморрагическом шоке является снижение кислородной емкости крови по мере увеличения кровопотери. В запуске патогенеза травматического шока значительную роль играет болевой фактор, интоксикация продуктами распада тканей. Тяжесть травматического шока не всегда коррелирует с объемом кровопотери.
Клиника и диагностика Диагностика основана на оценке клинических и лабораторных признаков. В условиях острой кровопотери чрезвычайно важно определить ее величину. Для этого необходимо воспользоваться одним из существующих методов, которые подразделяют на 3 группы: клинические, эмпирические и лабораторные. Клинические методы позволяют оценить объем кровопотери на основании клинических симптомов и гемодинамических показателей. Тяжесть кровопотери определяется ее видом, быстротой развития, объемом потерянной крови, степенью гиповолемии и возможностью развития шока, которые наиболее полно отражены в классификации П. Г. Брюсова. Общие принципы лечения 1. Остановка кровотечения, борьба с болью. 2. Обеспечение адекватного газообмена. 3. Восполнение дефицита ОЦК. 4. Лечение органной дисфункции и профилактику полиорганной несостоятельности: · лечение сердечной недостаточности; · профилактика почечной недостаточности; · коррекция метаболического шока; · стабилизация обменных процессов в клетке; · лечение и профилактика ДВС-синдрома. 5. Ранняя профилактика инфекции До постоянной остановки кровотечения при наружном кровотечении ― прижатие сосуда, давящая повязка, жгут, лигатура или зажим на кровоточащий сосуд. При внутреннем кровотечении ― срочное оперативное вмешательство, проводимое параллельно комплексу лечебных мероприятий по выведению больного из шока. Борьба с болевым синдромом и защита от психического стресса осуществляются путем внутривенного введения наркотических и ненаркотических анальгетиков, транквилизаторов. Первоначальная доза наркотических анальгетиков у особо тяжелых больных должна быть сни-жена на 50% из-за возможного угнетения дыхания, тошноты и рвоты, возникающих при внут-ривенном введении этих препаратов. При травме ― иммобилизация конечности, проведение новокаиновых блокад. Обеспечение адекватного газообмена направлено на усвоение О2 и удаление СО2. Мероприятия имеют как профилактическое, так и лечебное значение. Всем больным показано обеспечение проходимости верхних дыхательных путей, профилактика аспирации содержимого желудка, профилактическое введение через носовой катетер не менее 4 л/мин О2. При необходимости показана интубация трахеи и перевод на ИВЛ с положительным давлением в конце выдоха ПДКВ= 5 см вод.ст. (для предотвращение спадения альвеол в конце выдоха), при необходимости этот показатель увеличивают, однако следует помнить что, ПДКВ более 10-15 см вод.ст. приводит к снижению сердечного выброса.
Восполнение дефицита ОЦК является первоочередной задачей лечения гиповолемических шоков. Для восполнения дефицита ОЦК необходимо: 1. Улучшенное положение Тренделенбурга для увеличения венозного возврата. 2. Инфузия в 2-3 периферические или 1-2 центральные вены. Темп восполнения определяется величиной АД и причиной кровопотери. Как правило, начальный темп восполнения – струйный или быстрой каплей. После стабилизации АД на безопасном уровне инфузия проводится капельно. Клиника ожогового шока Практический опыт показал, что клинически выраженные проявления общей реакции организма на термическое поражение с возможностью неблагоприятного исхода развиваются при ожогах свыше 15-20% поверхности тела. Поэтому во всем мире принято незамедлительное проведение таким больным инфузионной или пероральной жидкостной терапии, которая уменьшает тяжесть наступающих расстройств и их последствий, называемых ожоговым шоком. При легкой степени шока (площадь ожога менее 20%) больные испытывают сильную боль и жжение в местах ожогов. В первые минуты и часы может быть возбуждение. Тахикардия до 90. АД нормальное или незначительно повышено. Одышки нет. Диурез не снижен. Ели лечение запаздывает на 6-8 ч или не проводится, могут наблюдаться олигурия и умеренная гемоконцентрация. При тяжелом шоке (20-50% п. т.) быстро нарастают заторможенность, адинамия при сохраненном сознании. Тахикардия более выражена (до 110), АД стабильно только при инфузионной терапии и введении кардиотоников. Больные испытывают жажду, отмечаются диспептические явления (тошнота, рвота, икота, вздутие живота). Часто наблюдается парез ЖКТ, острое расширение желудка. Уменьшается мочеотделение. Диурез обеспечивается только применением медикаментозных средств. Выражена гемоконцентрация - гематокрит достигает 65. С первых часов после травмы определяется умеренный метаболический ацидоз с респираторной компенсацией. Больные мерзнут, температура тела ниже нормы. Шок может продолжаться 36-48 ч и более. При 3-й (крайне тяжелой) степени шока (ожоге более 50% п. т.) состояние крайне тяжелое. Через 1-3 ч после травмы сознание становится спутанным, наступают заторможенность и сопор. Пульс нитевидный, АД снижается до 80 мм рт. ст. и ниже (на фоне инфузионной терапии, введения кардиотонических, гормональных и других средств). Одышка, дыхание поверхностное. Часто наблюдается рвота, которая может быть многократной, цвета "кофейной гущи". Выраженный парез ЖКТ. Моча в первых порциях с признаками микро- и макрагематурии, затем темно-коричневого цвета с осадком. Быстро наступает анурия. Гемоконцентрация выявляется через 2-3 ч, гематокрит повышается до 70 и более. Нарастает гиперкалиемия и декомпенсированный смешанный ацидоз. Температура тела падает ниже 36°С. Шок может продолжаться до 3 сут. и более, особенно при ОДП.
Лечение обожженных в состоянии шока базируется на патогенетических предпосылках и про водится по правилам интенсивной или реанимационной терапии. 1. Устранение воздействия повреждающего фактора. 2. Обезболивание. 3. Обеспечение адекватного газообмена. 4. Начало инфузионной терапии. 5. Коррекция агрегатного состояния крови. 6. Лечение органной дисфункции и профилактика органной недостаточности. 7. Профилактика и лечение раневой инфекции. 8. Коррекция расстройств энергетического обмена. 9. Ранняя детоксикация. 10. Профилактика и лечение желудочно-кишечных кровотечений Особенности инфузионной терапии. Инфузионная заключается во внутривенном струйном введении сбалансированных соле-вых растворов через катетеры диаметром 1,2-1,4 мм, установленные в одну или две перифери-ческие вены. Проводят пункцию центральной вены. Объем и темп инфузии определяются тяжестью состояния больного и зависят от суточного объема жидкости, необходимого для возмещения дефицита ОЦК. При проведении инфузионной терапии руководствуются следующими правилами: 1.Темп инфузии и компонентность растворов определяются временем от момента пора-жения. 2.Первые 24 часа ожогового шока: a. суточный объем инфузии рассчитывают по формуле Паркланда:
b. скорость инфузии: • 50% расчетного объема вводят в первые 8 часов; • 25% - во вторые 8 часов; • 25% - в третьи 8 часов. Формулу следует рассматривать в качестве ориентировочной установки. В дальнейшем объем и темп введения лечебных средств корректируется на основании показателей диуреза, гематокрита, гемоглобина, пульса и артериального давления в динамике. Поскольку при ожогах из сосудистого русла вместе с плазмой уходит большое количество ионов натрия (0,5-0,6 мэкв/% ожога /кг веса больного), инфузионная терапия в первую очередь преследует цель наполнения сосудистого русла и восстановления в нем содержания натрия. Для этого используются физиологический раствор или лактатный раствор Рингера. Последний более предпочтителен, поскольку по своему составу он ближе к внеклеточной жидкости. В зависимости от тяжести шока при расчетах следует учитывать разное соотношение коллоидов и кристаллоидов. При тяжелом шоке рассчитанный объем должен включать 2/3 кристаллоидов и 1/3 коллоидов, а при крайне тяжелом шоке и ожогах свыше 50% поверхности тела кристаллоиды и коллоиды используют в соотношении 1:1. Если инфузия начинается в условиях артериальной гипотонии спустя несколько часов после травмы, наряду с введением кристаллоидов возможно переливание плазмозаменителей (полиглюкин, гидроксиэтилкрахмал). Введение белковых коллоидных растворов целесообразно начинать спустя 12-24 ч после начала инфузионной терапии, когда наступает некоторое уравновешивание внутри- и внесосудистого секторов. Наибольший эффект обеспечивает СЗП, которая имеет все белковые фракции и влияет на осмотические и онкотические свойства крови. Растворы альбумина следует использовать, когда уменьшатся нарушения проницаемости сосудистой стенки и прекратится нарастание отека в зоне ожога. Темп инфузии белковых препаратов ―1-2 мл/кг/час. Растворы глюкозы в первые сутки получения тяжелой ожоговой травмы у взрослых не используют, т.к. вследствие нарушения функции капиллярной мембраны они проникают в межклеточное пространство и способствуют образованию отеков, нарушению питания тканей и усугублению уже имеющихся повреждений На вторые сутки объем инфузии составляет 50-70% от первонального объема (при достиже-нии диуреза не < 50 мл/ч). Ожоговый шок может длиться до 3-х суток. Инфузионная терапия должна проводиться все время без перерыва. С целью улучшения реологических свойств крови назначаются безбелковые средне- и низкомолекулярные коллоидные растворы в объеме 400-800 мл со скоростью 2 мл/кг/час. В настоящее время при ожоговом шоке гемотрансфузию не проводят, однако последняя показана при большой кровопотере во время некротомии или при массивном гемолизе сразу после выведения больного из шока. При тяжелом и крайне тяжелом шоке, при поздно начатой терапии бывает невозможно поддерживать артериальное давление выше 90 мм рт. ст. введением кристаллоидов и коллоидов в расчетных количествах. В таких случаях целесообразно не увеличивать объем вводимых жидкостей, так как это может привести к увеличению интерстициальной и внутриклеточной жидкости, а применить препараты инотропного действия (допамин в дозе 5-10 мкг/кг/мин). В этой дозировке допамин улучшает сократимость миокарда и увеличивает сердечный выброс. В дозировке 1-3 мг/кг/мин он способствует улучшению перфузии почек. Hаибольшие трудности в лечении обожженных возникают при сочетании ожогов кожи с термоингаляционным поражением дыхательных путей. У таких больных течение шока резко отягощается токсическим воздействием на дыхательные пути и организм в целом ядовитых продуктов горения. Особенностью инфузионной терапии у этих больных является необходимость "балансирования" в объеме инфузии, так как постоянно имеется угроза развития отека легких, а снижение темпа и количества вводимых внутривенно жидкостей вызывает снижение перфузии почек, способствует сохранению и усугублению гиповолемии. В таких случаях можно прибегать к инфузионной терапии гипертоническим раствором натрия (240 мэкв/л). При этом необходимо следить за тем, чтобы уровень натрия в плазме не превышал 160 мэкв/л. Введение гипертонического раствора целесообразно ограничить первыми 8-10 часами после получения ожога, то есть временем, наиболее выраженных нарушений проницаемости сосудистой стенки. В тех случаях, когда развивается явление дыхательной недостаточности, больным необходимо проводить искусственную вентиляцию легких с положительным давлением на выдохе. Hормализация реологических свойств крови осуществляется путем описанной выше инфузионной терапии, т.е. за счет коррекции гиповолемии, а также за счет применения низких доз гепарина (до 20000 ед/сутки и более). Hормализация диуреза, стабилизация артериального давления, снижение гемоконцентрации, повышение температуры тела, прекращение диспептических растройств и усвоение выпитой жидкости являются показателями адекватности лечения и выхода больного из состояния ожогового шока.
КАРДИОГЕННЫЙ ШОК Классификация кардиогенного шока (Е.И. Чазов) Рефлекторный КШ: снижение сердечного выброса обусловлено, в основном, рефлекторными влияниями из зоны поражения на насосную функцию сердца и тонус периферических сосудов. Поэтому для предотвращения перехода рефлекторной формы КШ в "истинный" кардиогенный шок необходимо немедленное и полное купирование ангинозного приступа. Аритмическая форма КШ обусловлена острыми гемодинамически значимыми аритмиями и требует безотлагательного восстановления синусового ритма или нормализации частоты сердечных сокращений, особенно при пароксизмальной тахикардии. "Истинный" КШ характеризуется глубокой артериальной гипотонией, выраженной левожелудочковой недостаточностью и нарушением периферического кровообращения. Ведущим фактором в патогенезе "истинного" КШ является резкое снижение насосной функции сердца и тканевой перфузии. "Ареактивный" КШ отличается от "истинного" максимальной выраженностью гемодинамических и клинических проявлений, отсутствием реакции на введение инотропных препаратов и практически 100%-й летальностью. "Гиповолемический" КШ может быть своевременно распознан с внедрением в клиническую практику экспресс-методов определения основных параметров центральной гемодинамики. Критерии диагностики кардиогенного шока: 1) систолическое АД составляет менее 90 мм рт.ст. на протяжении 1 часа и более; пульсовое давление снижается до 15-20 мм рт.ст. 2) признаки гипоперфузии ― цианоз, холодные влажные кожные покровы, выраженная олигурия (мочеотделение менее 20 мл в час), застойная сердечная недостаточность, ментальные расстройства; 3) частота сердечных сокращений выше 60 уд. в мин; 4) гемодинамические признаки ― сердечный индекс менее 2,2 л/мин/кв.м., и давления наполнения левого желудочка, которое при гиповолемии не превышает 10-12 мм рт.ст., а при "истинном" КШ обычно выше 25-30 мм рт.ст. Диагностические исследования: 1. Аналогично исследованиям при неосложненном ИМ. 2. Почасовой контроль диуреза с помощью мочевого катетера. 3. Эхокардиография (при возможности). 4. Определение насыщения артериальной крови кислородом (при возможности). 5. Прикроватная рентгенография грудной клетки. Лечение кардиогенного шока Лечение кардиогенного шока, требует интенсивных неотложных мероприятий. Обязательным является наличие постоянного венозного доступа путем установки катетера (желательно двух катетеров) в периферическую вену, а также мочевого катетера. При невозможности инвазивного мониторинга внутрисердечной и центральной гемодинамики, в/в инфузия препаратов проводится под тщательным контролем АД, пульса., ЧД, аускультации легких. Достаточным является повышение систолического давления до уровня 90-100 мм рт. ст. (при отсутствии тяжелой артериальной гипертонии до инфаркта миокарда; в последнем случае указанный уровень АДс может быть недостаточным). Выбор метода лечения КШ зависит от особенностей патогенеза левожелудочковой недостаточности и исходной клинико-гемодинамической ситуации в каждом конкретном случае Рефлекторный КШ (как следствие выраженного ангинозного приступа) ― адекватное обезболивание ― 1-2 мл 0,005% р-ра фентанила или 1 мл 1% р-ра морфина или 1 мл 2% р-ра промедола в/венно, струйно, медленно. Аритмический КШ (как следствие тахиаритмий (а) и брадиаритмий (б)) ― коррекция нарушений ритма а) 5-10 мл 10% р-ра новокаинамида в сочетании с 0,2-0,3 мл 0,1% р-ра мезатона в/венно в течение 5 минут; или амиодарон 5 мг/кг в/венно струйно медленно, затем 150-300 мг капельно на 5% р-ре глюкозы (при наджелудочковых и желудочковых аритмиях), 6-10 мл 2% р-ра лидокаина (тримекаина) в/венно в течение 5 минут (при желудочковых аритмиях) Электроимпульсная терапия применяется после предварительного наркоза (тиопенталом натрия, оксибутиратом натрия) при отсутствии эффекта от антиаритмических средств. б) временная электрокардиостимуляция, при ее отсутствии ― 1-2 мл 0,1% р-ра атропина в/венно, медленно или (а также при отсутствии эффекта) 1 мл 0,05% р-ра алупента в 200 мл 5% р-ра глюкозы (или физр-ра) в/венно, капельно, под контролем АД и ЧСС. “Истинный” КШ (как следствие резкого снижения насосной функции левого желудочка) при наличии показаний вводят низкомолекулярный декстран внутривенно, со скоростью не менее 20 мл в минуту (250мл/10мин.), до исчезновения признаков шока или до повышения ЦВД до120-140 мм водн.ст. Если систолическое давление остается ниже 90мм рт.ст применяют кардиотинические средства. Применение положительных инотропных препаратов является основным методом стандартной терапии кардиогенного шока. В тяжелых случаях их комбинируют с вазопрессорами. ü дофамин: 5-20 мкг/кг/мин., увеличение дозы на 1-4 мкг/кг/мин., каждые 10-30 мин. ― до оптимального ответа ü добутамин: 5-20 мкг/кг/мин. в виде постоянной инфузии Возможно сочетание низких доз дофамина (для стимуляции дофаминовых рецепторов) и добутамина ü норадреналин: 1-2 мкг/мин. при АД менее 70 мм рт. ст. на фоне введения дофамина Возможно применение ингибиторов фосфодиэстеразы: ü милринон (бипиридин), нагрузочная доза 50 мкг/кг за 10 минут, поддерживающая - 0,375-0,75 мкг/кг/мин. в виде постоянной инфузии Ингибиторы фосфодиэстеразы III оказывают инотропное и вазодилятирующее действие, вызывают увеличение МОК, УОС и снижение сопротивления легочныхи периферических сосудов. Лечение причины (инфаркта миокарда), возможно более ранняя реваскуляризация Адекватная тромболитическая терапия является важнейшим способом предупреждения и лечения кардиогенного шока. Особенности ее проведения: 1. Низкое АД не является препятствием для назначения тромболитиков, поскольку противошоковые мероприятия проводятся одновременно. 2. Тромболитики могуг быть назначены в сроки, превышающие формально установленные, т.е. позднее 12 ч от дебюта ОИМ (в пределах 24 ч). 3. При назначении стрептокиназы для профилактики возможной аллергической реакции показано предварительное в/в болюсное введение преднизолона в дозе до 240 мг (предвари-тельное введение преднизолона не предупреждает характерной гипотензивной реакции на быструю инфузию стрептокиназы, поскольку последняя не связана с аллергической реакцией). В крупных клинических испытаниях проведение тромболитической терапии привело к снижению госпитальной летальности от кардиогенного шока. Летальность данного контингента больных составила менее 50%. Комплексная медикаментозная терапия КШ, помимо нормализации основных гемодинамических оказателей, предполагает коррекцию таких нарушений, как гипоксемия и метаболический ацидоз. Кислород назначается через носовые катетеры или маску со скоростью 4-6 л/мин с ее по-вышением при необходимости до 8-10 л/мин. Проводится контроль насыщения крови кислоро-дом. Если несмотря на ингаляцию 100% кислорода со скоростью 8-10 л/мин не удается добить-ся достаточного повышения насыщения крови кислородом (РаО2 < 60 мм рт. ст.), показана ис-кусственная вентиляция легких. Декомпенсированный метаболический ацидоз ухудшает функциональное состояние миокарда и существенно снижает эффективность инотропных препаратов. Коррекция метаболического ацидоза при затяжном кардиогенном шоке осуществляется введением 4% раствора гидрокарбоната натрия под контролем показателей КОС из расчета 0,5-1 ммоль (1-2мл) на кг. Необходимо помнить, что избыточное введение гидрокарбоната натрия может привести к метаболическому алкалозу с последующим ухудшением транспорта кислорода и нарушением ритма вплоть до асистолии. Отсутствие убедительного клинического эффекта в течение 1-2 часов интенсивной медикаментозной терапии является основанием для использования внутриаортальной баллонной контрпульсации. АНАФИЛАКТИЧЕСКИЙ ШОК Принципы лечения
1. Патогенетическая терапия септического шока сводится к санации очагов инфекции, назначению антибиотиков широкого спектра действия. Санация инфекционного очага является краеугольным камнем терапии септического шока. Даже самые мощные антибиотики и другие методы дезинтоксикационной терапии оказываются неэффективными при отсутствии или недостаточной санации очага. Целенаправленная антибиотикотерапия возможна после выделения возбудителя и определения его чувствительности к антибиотикам, то есть в лучшем случае не ранее 48 часов. Вместе с тем ранняя антибиотикотерапия (в течение 30 мин. от поступления) достоверно снижает летальность у данной категории больных. Поэтому, представляется целесообразным использование так называемого деэскалационного принципа антибиотикотерапии с начальным назначением антибиотиков максимально широкого спектра действия (карбопенемы, фторхинолоны, цефалоспорины 4-го поколения) с последующей заменой, по возможности, антибиотиком определенного (в результате бактериологического исследования) спектра. 2.1 Гемодинамическая поддержка. Инфузионная терапия принадлежит к первоначальным мероприятиям поддержания гемодинамики и прежде всего сердечного выброса. По данным Американского колледжа и Американской ассоциации критической медицины, приблизительно у 50% септических больных основные гемодинамические параметры можно нормализовать с помощью адекватной инфузионной терапии. Основными задачами инфузионной терапии у больных с сепсисом являются: восстановление адекватной тканевой перфузии, нормализация клеточного метаболизма, коррекции расстройств гомеостаза, снижение концентрации медиаторов септического каскада и токсических метаболитов Начинают инфузионную терапию с введения кристаллоидов ― болюс 20 мл/кг в течение 20-30 минут затем после оценки состояния гемодинамики повторно, со скоростью порядка 20-30 мл/кг/час под контролем ЦВД и показателей гемодинамики до общей дозы 4 литров (60 мл/кг) Для инфузионной терапии в рамках целенаправленной ИТ сепсиса и СШ практически с одинаковым результатом применяют кристаллоидные и коллоидные инфузионные растворы. Все инфузионные среды имеют как свои достоинства, так и недостатки. Принимая во внимание имеющиеся результаты экспериментальных и клинических исследований, на сегодняшний день нет оснований отдавать предпочтение какой-то из инфузионных сред. Однако следует иметь в виду, что для адекватной коррекции венозного возврата и уровня преднагрузки требуется значительно большие объемы (в 2–4 раза) инфузии кристаллоидов, чем коллоидов, что связано с особенностями распределения растворов между различными секторами. Кроме того, инфузия кристаллоидов более сопряжена с риском отека тканей, а их гемодинамический эффект менее продолжителен, чем коллоидов. В то же время кристаллоиды более дешевы, не влияют на коагуляционный потенциал и не провоцируют анафилактоидных реакций. В этой связи качественный состав инфузионной программы должен определяться особенностями пациента: степенью гиповолемии, фазой синдрома ДВС, наличием периферических отеков и уровнем альбумина крови, тяжестью острого легочного повреждения. Плазмозаменители (декстраны, желатиноль, гидроксиэтилкрахмалы) показаны при выраженном дефиците ОЦК. Гидроксиэтилкрахмалы (ГЭК) с молекулярной массой 200/0,5 и 130/0,4 имеют потенциальное преимущество перед декстранами в силу меньшего риска утечки через мембрану и отсутствия клинически значимого воздействия на гемостаз. Применение альбумина при критических состояниях может способствовать повышению летальности. Увеличение КОД при инфузии альбумина носит транзиторный характер, а затем в условиях синдрома "капиллярной протечки" происходит дальнейшая экстравазация альбумина (rebound syndrome). Переливание альбумина, возможно, будет полезным только при снижении уровня альбумина менее 20 г/л и отсутствии признаков его "утечки" в интерстиций. Применение криоплазмы показано при коагулопатии потребления и снижении коагуляционного потенциала крови. По мнению большинства экспертов, минимальная концентрация гемоглобина для больных с тяжелым сепсисом должна быть в пределах 90–100 г/л. При сепсисе и СШ необходимо стремиться к быстрому достижению (первые 6 ч после поступления) целевых значений следующих параметров: ЦВД 8–12 мм рт. ст., САД>65 мм рт. ст., диурез 0,5 мл/кг/ч, гематокрит более 30%, сатурация крови в верхней полой вене или правом предсердии не менее 70%. Низкое перфузионное давление требует немедленного включения препаратов, повышающих сосудистый тонус, и/или инотропную функцию сердца. Допамин и/или норадреналин являются препаратами первоочередного выбора коррекции гипотензии у больных с СШ. Норадреналин (с начальной скоростью 1 мкг/мин. (у взрослых), подбирая дозу для достижения систолического давления 90 мм рт. ст.) повышает САД и увеличивает гломерулярную фильтрацию. Оптимизация системной гемодинамики под действием норадреналина ведет к улучшению функции почек без применения низких доз допамина. Работы последних лет показали, что применение норадреналина в сравнении с комбинацией допамина в высоких дозировках ± норадреналин ведет к статистически значимому снижению летальности. Адреналин – адренергический препарат с наиболее выраженными побочными гемодинамическими эффектами. Адреналин обладает дозозависимым действием на ЧСС, АДср, сердечный выброс, работу левого желудочка, доставку и потребление кислорода. Однако это действие адреналина сопровождается тахиаритмиями, ухудшением спланхнического кровотока, гиперлактатемией. Поэтому применение адреналина должно быть ограничено случаями полной рефрактерности к другим катехоламинам. Добутамин должен рассматривается как препарат выбора для увеличения сердечного выброса и доставки и потребления кислорода при нормальном или повышенном уровне преднагрузки. Благодаря преимущественному действию на ß1-рецепторы добутамин в большей степени, чем допамин, способствует повышению данных показателей. Катехоламины помимо поддержки кровообращения могут вмешиваться в течение системного воспаления, влияя на синтез ключевых медиаторов, обладающих дистантным эффектом. Под действием адреналина, допамина, норадреналина и добутамина снижались синтез и секреция TNF, активированными макрофагами. Отменять препараты кардиоциркуляторной поддержки следует через 24-36 часов после стабилизации центральной гемодинамики. Рефрактерный септический шок ― сохраняющаяся артериальная гипотония, несмотря на адекватную инфузию, применение инотропной и вазопрессорной поддержки. В случае развития рефрактерного септического шока показано введение глюкокортикостероидов ― гидрокортизон 240-300мг в первые сутки. После стабилизации давления доза может быть снижена до 50 мг каждые 8 часов последующие 48 часов. Длительность терапии – 5-7 суток. 2.2.Респираторная поддержка. Легкие очень рано становятся одними из первых органов-мишеней, вовлекаемых в патологический процесс при сепсисе. Острая дыхательная недостаточность (ОДН) – один из ведущих компонентов полиорганной дисфункции. Клинико-лабораторные проявления ОДН при сепсисе соответствуют синдрому острого легочного повреждения, а при прогрессировании патологического процесса ― острому респираторному дистресс-синдрому (ОРДС). Проводят ингаляцию кислорода, а по показаниям интубация трахеи и ИВЛ.
|
||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-16; просмотров: 299; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.202.167 (0.082 с.) |