Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Завдання першого рівня складностіСтр 1 из 2Следующая ⇒
Завдання першого рівня складності 1А1 Кількісною характе-ристикою молекули є: а)відносна молекулярна маса; 1А2 Хімічний елемент: б) вид атомів з однаковим зарядом ядра; 1А3 Проста речовина – це в)речовина, молекули якої складаються з атомів одного елемента;
1А4 Складна речовина г) речовина, молекули якої складаються з атомів різних елементів;
1А5 Алотропія: а) явище існування хімічного елемента у вигляді двох або кількох простих речовин, відмінних за властивостями;
1А6 Відносна атомна маса магнію Аr (Mg) дорівнює: б) 24,3 1А7 Відносна молекулярна маса цинк оксиду Мr (ZnO) дорівнює: в) 81,4;. 1А8 Внаслідок різних реакцій отримано воду: 1) NaOH + HCl ® NaCl + H2O; 2) CuSO4×H2O 3) C2H5OH Чи можна стверджувати, що після дистиляції вода має склад: а) однаковий у всіх випадках;
1А9 Маса речовин, які вступили в хімічну реакцію:
в) дорівнює масі вихідних речовин;
1А10 Якщо два елементи утворюють між собою декілька сполук, то вагові кількості одного елемента, що сполучається з однією й тією ж ваговою кількістю іншого, співвідносяться між собою: б) як невеликі цілі числа;
1А11 За однакових умов об’єми газів, які вступають у реакцію відносяться між собою і до об’єму утворених газів: б) як невеликі цілі числа;
1А12 В однакових об’ємах газів за одних і тих самих умов (р, Т) міститься: в)однакова кількість молекул;
1А13 За 1 а.о.м. прийнято: в) 1/12 маси атома ізотопу 12С;
1А14 За нормальних умов 22,4 л це: в) молярний об’єм будь-якого газу; 1А15 1 моль молекулярного кисню О2 містить: а) 6,02∙1023 молекул; . 1А16 1 моль води Н2О містить: в)6,02∙1023 молекул; 1А17 1 моль натрій хлориду NaCl містить: г) 6,02∙1023 йонних асоціатів NaCl;
1А18 1 моль йонів Cu2+ містить: д) 6,02∙1023 йонів купруму.
1А19 1 моль електронів містить: в) 6,02∙1023 електронів;
1А20 Газ легший за повітря: б) аміак;
1А21 Відносна молекулярна маса нітратної кислоти складає: а) 63;
1А22 Молярна маса нітратної кислоти складає: д) 63 г/моль.
1А23 Молекулярна маса нітратної кислоти складає: б) 63 а.о.м.;
1А24 Молярна маса еквівалентів Н2SO4 і Na2SO4 згідно реакції Н2SO4 + 2NaOН ® Na2SO4 + 2H2O становить: в) Ем(Н2SO4) = 49 г/моль; Ем(Na2SO4) = 71 г/моль;
1А25 Молярна маса еквівалентів Al(OH)3 і H3PO4 згідно реакції Al(OH)3 + H3PO4 ® AlPO4 + 3H2O становить:
г) Ем(Al(OH)3) = 26 г/моль; Ем(H3PO4) = 32,7 г/моль;
Завдання другого рівня складності 1В1 Найбільший об’єм за нормальних умов (н.у.) займає: в) 3,01∙1023 молекул кисню;
1В2 Найменший об’єм за нормальних умов (н.у.) займає: г) 0,3 г кисню; 1В3 Найбільшу масу має: г) 0,7 моль газу азоту; 1В4 Відносна густина газу за киснем дорівнює 2. Яка його формула: г) SO2;
1В5 Відносна густина газу за воднем дорівнює 15. Яка його формула: б) C2Н6;
1В6 Відносна густина пропану (С3Н8) за воднем дорівнює: б) 22;
1В7 Яка кількість речовини карбон (ІV) оксиду міститься в 1 м3 газу (н.у.)? г) 44,64моль;
1В8 Яка кількість речовини водню міститься в 1 дм3 газу (н.у.): а) 0,0446 моль;
1В9 Визначити молекулярну формулу речовини, якщо її порція містить 2 моль Феруму, 6 моль Нітрогену, 18 моль Оксигену: в) Fe(NO3)2;
1В10 Який об’єм займає суміш газів (н.у.), що складається з 0,6 моль водню та 0,8 моль хлору: г) 31,36 л;
1В11 Повітря містить 0,93 % аргону за об’ємом. Скільки молекул аргону міститься в 1 л повітря (н.у.): в) 2,5∙1022;
1В12 Обчисліть масу молекули фтору в міліграмах: г) 6,308∙10-21 мг;
1В13 Обчисліть масу молекули озону в кілограмах: д) 7,968∙10-26 кг. 1В14 Визначити, у якій кількості речовини кисню міститься 3,01∙1022 молекул: б) 0,05 моль; 1В15 Який об’єм (н.у.) займає 20 г водню? в) 224 л;
1В16 Який об’єм (н.у.) займає займає суміш, що складається з 0,5 моль озону і 0,75 моль азоту? г) 28 л;
1В17 За однакових умов об’єм кожного їз двох газів О3 і Аr складає 639 мл. У скільки разів число атомів одного газу більше від числа атомів іншого? а) у 3 рази;
1В18 Визначити молярну масу невідомого газу, якщо густина цього газу за киснем дорівнює 5. г) 160 г/моль;
1В19 За деякої температури густина парів сірки за азотом 9,14. Зі скількох атомів складається молекула сірки за цієї температури? б) 8;
1В20 Густина парів фосфору за повітрям дорівнює 4,28. Зі скількох атомів складається молекула газоподібного фосфору? а) 4; Завдання третього рівня складності 1С1 Газ масою 1,73 за температури 39° С і тиску 741 мм. рт. ст. займає об’єм 640 мл. Визначити молярну масу газу.
б) 71 г/моль;. 1С2 Обчисліть масу хрому в 515 г суміші, яка містить 80 % Cr(OH)3. в) 208 г
1С3 Є газова суміш, масові частки газів у якій рівні: водню – 35 %, азоту – 65 %. Визначте об’ємні частки газів у суміші: а) ω(H2) = 88,3 %; ω(N2) = 11,7 %;
1С4 При спалюванні 1 г природного вугілля одержано 1250 мл СО2 (н.у.). Визначте масову частку вуглецю в цьому зразку природного матеріалу (%): г) 67 %;
1С5 Спалили окремо 2 л метану СН4 і 1 л пропану С3Н8, Який об’єм вуглекислого газу утворився в кожному випадку? а) 2 л; 3 л; Тестові завдання з теми: «Періодичний закон і періодична система хімічних елементів. Будова ядер і електронних оболонок атомів хімічних елементів.». Тестові завдання по темі: «Класи неорганічних сполук» Тестові завдання по темі: «Хімічний зв’язок і будова молекул. Ступінь окиснення. Комплексні (координаційні) сполуки» Тестові завдання по темі: «Окисно-відновні реакції» Завдання першого рівня складності 1А1 Кількісною характе-ристикою молекули є: а)відносна молекулярна маса; 1А2 Хімічний елемент: б) вид атомів з однаковим зарядом ядра; 1А3 Проста речовина – це в)речовина, молекули якої складаються з атомів одного елемента;
1А4 Складна речовина г) речовина, молекули якої складаються з атомів різних елементів;
1А5 Алотропія: а) явище існування хімічного елемента у вигляді двох або кількох простих речовин, відмінних за властивостями;
1А6 Відносна атомна маса магнію Аr (Mg) дорівнює: б) 24,3 1А7 Відносна молекулярна маса цинк оксиду Мr (ZnO) дорівнює: в) 81,4;. 1А8 Внаслідок різних реакцій отримано воду: 1) NaOH + HCl ® NaCl + H2O; 2) CuSO4×H2O 3) C2H5OH Чи можна стверджувати, що після дистиляції вода має склад: а) однаковий у всіх випадках;
1А9 Маса речовин, які вступили в хімічну реакцію:
в) дорівнює масі вихідних речовин;
1А10 Якщо два елементи утворюють між собою декілька сполук, то вагові кількості одного елемента, що сполучається з однією й тією ж ваговою кількістю іншого, співвідносяться між собою: б) як невеликі цілі числа;
1А11 За однакових умов об’єми газів, які вступають у реакцію відносяться між собою і до об’єму утворених газів: б) як невеликі цілі числа;
1А12 В однакових об’ємах газів за одних і тих самих умов (р, Т) міститься: в)однакова кількість молекул;
1А13 За 1 а.о.м. прийнято: в) 1/12 маси атома ізотопу 12С;
1А14 За нормальних умов 22,4 л це: в) молярний об’єм будь-якого газу; 1А15 1 моль молекулярного кисню О2 містить: а) 6,02∙1023 молекул; . 1А16 1 моль води Н2О містить: в)6,02∙1023 молекул; 1А17 1 моль натрій хлориду NaCl містить: г) 6,02∙1023 йонних асоціатів NaCl;
1А18 1 моль йонів Cu2+ містить: д) 6,02∙1023 йонів купруму.
1А19 1 моль електронів містить: в) 6,02∙1023 електронів;
1А20 Газ легший за повітря: б) аміак;
1А21 Відносна молекулярна маса нітратної кислоти складає: а) 63;
1А22 Молярна маса нітратної кислоти складає: д) 63 г/моль.
1А23 Молекулярна маса нітратної кислоти складає: б) 63 а.о.м.;
1А24 Молярна маса еквівалентів Н2SO4 і Na2SO4 згідно реакції Н2SO4 + 2NaOН ® Na2SO4 + 2H2O становить: в) Ем(Н2SO4) = 49 г/моль; Ем(Na2SO4) = 71 г/моль;
1А25 Молярна маса еквівалентів Al(OH)3 і H3PO4 згідно реакції Al(OH)3 + H3PO4 ® AlPO4 + 3H2O становить: г) Ем(Al(OH)3) = 26 г/моль; Ем(H3PO4) = 32,7 г/моль;
|
||||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 253; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.138.143.108 (0.041 с.) |
 CuSO4 + H2O;
CuSO4 + H2O;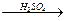 C2H4 + H2O;
C2H4 + H2O;