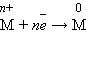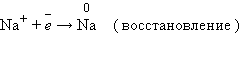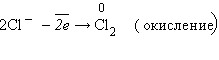Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Общие способы получения металловСодержание книги
Поиск на нашем сайте
Минералы и горные породы, содержащие металлы и их соединения, из которых выделение чистых металлов технически возможно и экономически целесообразно, называют рудами. Получение металлов из руд – задача металлургии. Металлургия – это и наука о промышленных способах получения металлов из руд, и отрасль промышленности. Любой металлургический процесс – это процесс восстановления ионов металла с помощью различных восстановителей. Суть его можно выразить так:
Существуют следующие способы получения металлов: пирометаллургический, гидрометаллургический, электрометаллургический. Пирометаллургия – восстановление металлов из руд при высоких температурах с помощью углерода, оксида углерода (II), водорода, металлов – алюминия, магния. Например, олово восстанавливают из касситерита SnO2, а медь – из куприта Cu2O прокаливанием с углем (коксом):
Сульфидные руды предварительно подвергают обжигу при доступе воздуха, а затем полученный оксид восстанавливают углем:
ZnO + C = Zn + CO Из карбонатных руд металлы выделяют также путем накаливания с углем, так как карбонаты при нагревании разлагаются, превращаясь в оксиды, а последние восстанавливаются углем:
FeO + C = Fe + CO ↑ Восстановлением углем можно получить Fe, Cu, Zn, Cd, Ge, Sn, Pb и другие металлы, не образующие прочных карбидов (соединений с углеродом). В качестве восстановителя можно применять водород (а) или активные металлы (б): а) МоО3 + 3Н2 = Мо + 3Н2О (водородотермия) К достоинствам этого способа относится получение очень чистого металла. б) TiO2 + 2Mg = Ti + 2MgO (магнийтермия) 3MnO2 + 4Al = 3Mn + 2Аl2O3 (алюминотермия) Чаще всего в металлотермии используют алюминий, теплота образования оксида которого очень велика (2Аl + 1,5O2 = Al2O3 + 1676 кДж/моль). Гидрометаллургия – это восстановление металлов из их солей в растворе. Процесс проходит в 2 этапа: 1) природное соединение растворяют в подходящем реагенте для получения раствора соли этого металла; 2) из полученного раствора данный металл вытесняют более активным или восстанавливают электролизом. Например, чтобы получить медь из руды, содержащей оксид меди СuО, ее обрабатывают разбавленной серной кислотой: CuO + H2SO4 = CuSO4 + Н2O Затем медь извлекают из раствора соли либо электролизом, либо вытесняют из сульфата железом: CuSO4 + Fe = Сu + FeSO4 Таким способом получают серебро, цинк, молибден, золото, уран. Электрометаллургия – восстановление металлов в процессе электролиза растворов или расплавов их соединений. Электролиз Если в раствор или расплав электролита опустить электроды и пропустить постоянный электрический ток, то ионы будут двигаться направленно: катионы – к катоду (отрицательно заряженному электроду), анионы – к аноду (положительно заряженному электроду). На катоде катионы принимают электроны и восстанавливаются, на аноде анионы отдают электроны и окисляются. Этот процесс называют электролизом. Электролиз – это окислительно-восстановительный процесс, протекающий на электродах при прохождении электрического тока через расплав или раствор электролита. Простейший пример таких процессов – электролиз расплавленных солей.
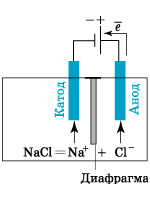
Рисунок Схема электролиза расплава хлорида натрия Рассмотрим процесс электролиза расплава хлорида натрия (рис.) В расплаве идет процесс термической диссоциации: NaCl → Na+ + Cl– Под действием электрического тока катионы Na+ движутся к катоду и принимают от него электроны:
Анионы Сl– движутся к аноду и отдают электроны:
Суммарное уравнение процессов:
Или
На катоде образуется металлический натрий, на аноде – газообразный хлор. Главное, что вы должны помнить: в процессе электролиза за счет электрической энергии осуществляется химическая реакция, которая самопроизвольно идти не может. Электролиз расплавов и растворов веществ широко используют в промышленности: 1. Для получения металлов (алюминий, магний, натрий, кадмий получают только электролизом). 2. Для получения водорода, галогенов, щелочей. 3. Для очистки металлов – рафинирования (очистку меди, никеля, свинца проводят электрохимическим методом). 4. Для защиты металлов от коррозии – нанесения защитных покрытий в виде тонкого слоя другого металла, устойчивого к коррозии (хрома, никеля, меди, серебра, золота) – гальваностегия Получение металлических копий, пластинок – гальванопластика. Неметаллы
|
||||||||||||||||||||||
|
Последнее изменение этой страницы: 2022-01-22; просмотров: 119; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.151 (0.01 с.) |