Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Загальна характеристика треть ої аналітичної групи катіонів
До третьої аналітичної групи відносять такі катіони: Al3+, Cr3+, Fe3+, Fe2+, Mn2+, Zn2+, Ni2+ и Со2+. Ці йони відносно стійкі й широко розповсюджені при звичайних умовах. Їхні сульфіди, на противагу сульфідам катіонів 1-ої і 2-ої груп, практично не розчинні у воді (A12S3 і Cr2S3, гідролізуючи, переходять у нерозчинні гідроксиди), однак, вони розчиняються в розведених кислотах. Груповим реагентом катіонів ІІІ-ої аналітичної групи є сульфід амонію (NH4)2S, який осаджує Fe3+, Fe2+, Mn2+, Zn2+, Ni2+ и Со2+ у вигляді сульфідів, а А13+ и Сг3+ - у виді гідроксидів. Сірководень не придатний для цієї мети: він утворює у розчині настільки мало іонів S2-, що добутки розчинності сульфідів 3-ї групи (за винятком сульфіду цинку Zn) не досягаються. Використовувати як груповий реагент сульфід натрію Na2S або сульфід калію K2S також не можна, бо при цьому у розчин додатково вводяться йони Na+ або К+. Катіони 3-ої аналітичної групи поділяють на дві підгрупи. Критерієм для такого поділу є відношення їх до дії NH4OH у присутності хлориду амонію. Хлорид амонію пригнічує дисоціацію основи і зменшує концентрацію гідроксид-йонів у розчині. При таких умовах тільки добутки розчинності досягаються лише для гідроксидів алюмінію, хрому й заліза А1(ОН)3, Сг(ОН)3 і Fe(OH)3, які й випадають в осад. Інші катіони 3-ої групи залишаються в розчині. Це і є критерієм поділу 3-ої групи на дві підгрупи: 1-а підгрупа - А13+, Cr3+, Fe3+, що осаджуються NH4OH у присутності солей амонію; 2-а підгрупа - Fe2+, Mn2+, Zn2+, Co2+, Ni2+, які не осаджуються таким способом. Солі катіонів 3-ї групи, утворені сильними кислотами, мають у розчинах кислу реакцію. Солі А13+ і Сг3+, утворені слабкими кислотами, гідролізують практично повністю. Сульфіди, фосфати й карбонати катіонів 3-ої аналітичної групи – нерозчинні у воді. Всі катіони 3-ї групи мають агробіологічне значення. Кислі підзолисті ґрунти із рН нижче 5 - 5,5 містять значні кількості А13+ у рухливому стані. Багато культур погано розвиваються на таких ґрунтах через підвищену кислотність і частково через отруйність алюмінію. При гідролізі солей, утворених А13+ і сильними кислотами, підвищується концентрація іонів Н+ у ґрунтовому розчині і підвищується його кислотність. Солі алюмінію застосовують для очищення природних вод. Якщо додати до води сульфат алюмінію A12(SO4)3 і небагато гашеного вапна Са(ОН)2, то утворюється гідроксид алюмінію А1(ОН)3, який, коагулюючи, захоплює із собою на дно відстійника завислі частинки домішок.
Органічні сполуки заліза містяться в тканинах всіх рослин і тварин. Входячи до складу гемоглобіну крові, залізо зв'язує молекулярний кисень і доставляє його клітинам. Нестача заліза в ґрунті викликає в рослин так званий хлороз –рослина втрачає зелене забарвлення через знижений зміст хлорофілу. Надлишок заліза в ґрунті також шкідливий для рослин. Марганець, цинк, нікель, кобальт і хром - мікроелементи, необхідні рослинам (і тваринам) у мізерно малих кількостях. При нестачі марганцю в ґрунті в злаків й інших культур виникають різні захворювання, знижується врожайність і рослина навіть може загинути. Всі ці небажані явища усувають внесенням у ґрунт марганцевих мікродобрив. При недостачі цинку в організмі рослин погіршується утворення хлорофілу, вітамінів, речовин, які відповідають за ріст (ауксинів). Ці хвороби усуваються при внесенні у ґрунт солей цинку. У ветеринарії, як і у медицині цинковмісні мазі застосовують для лікування шкірних хвороб. Недостача кобальту в ґрунтах негативно позначається на рості зернових культур, цукрового буряка,.конюшини, льону. Знижений вміст його в кормах погіршує життєдіяльність великої рогатої худоби й овець. Додавання солей кобальту в раціон збільшує кількість гемоглобіну в крові й вітамінів у тканинах тварин. Значення нікелю й хрому для рослин і тварин вивчено менше. Таким чином, виявлення й кількісне визначення катіонів 3-ої групи пов'язано, в основному, з аналізом ґрунтів, мікродобрив, рослинного й тваринного матеріалу.
ЕКСПЕРИМЕНТАЛЬНА ЧАСТИНА ЯКІСНІ РЕАКЦІЇ НА КАТІОНИ 2.1. Якісні реакції катіонів I аналітичної групи (Na +, K +, NH 4 +, Mg 2+) Реакції виявлення йона N a + Дослід 1. Реакція з калій гексагідроксостибіатом (V) К [ Sb (ОН)6 ]. Калій гексагідроксостибіат (V) у нейтральному середовищі утворює з іонами Натрію білий кристалічний осад натрій гексагідроксостибіату(V) за рівнянням NaCl + К[Sb(ОН)6] = Na[Sb(OH)6]↓ + KC1 Na+ + [Sb(OH)6]- = Na[Sb(OH)6]↓ Для безпомилкового виявлення іона Na+ необхідно дотримуватися таких умов: реакцію треба виконувати лише в нейтральному середовищі(pH=7), бо у кислому середовищі реагент K[Sb(OH)6] утворює ортосурмяну кислоту за реакцією:
K[Sb(OH)6] + HCl = H3SbO4 + KCl + 2H2O, яка розкладається і утворюється аморфний осад метасурмяної кислоти: H3SbO4 → HSbO3↓ + H2O. Такий осад не свідчить про наявність у розчині катіона Na+. У сильнолужному середовищі осад Na[Sb(OH)6] розчиняється з утворенням середньої солі Na3SbO4: Na[Sb(OH)6] + 2NaOH = Na3SbO4 + 4H2O. Отже, якщо досліджуваний розчин кислий, його нейтралізують KOH (або K2CO3), якщо ж лужний – слабкою кислотою (ацетатною). Виконання досліду. До 2-3 крапель розчину солі Na+ додають рівний об’єм реактива K[Sb(OH)6] і потирають скляною паличкою внутрішню поверхню стінок пробірки, щоб попередити утворення пересиченого розчину Na[Sb(OH)6] і прискорити випадання осаду. Оскільки розчинність осаду Na[Sb(OH)6] при нагріванні сильно зростає, то реакцію виконують на холоді (15-20 оC). Іноді охолоджують пробірку з розчином проточною водою з крана. Дослід 2. Реакція з цинк-ураніл ацетатом Zn (U 02)3(CH 3 COO)8. Цинк-ураніл ацетат у розчині ацетатної кислоти утворює з іонами натрію жовтий кристалічний осад за рівнянням Na+ + Zn (UО2)3 (CH3COO)8 + СН3СОО-+ 9Н2О = = NaZn(UО2)3(CH3COO)9 ∙ 9H2O↓ Реакція є специфічною і досить чутливою (0,01 мкг), аналогічну реакцію дають іони Li+. Запишіть повне іонне рівняння реакції. Виконання досліду. Беруть 2 - 3 краплі розчину солі натрію, підкислених оцтовою кислотою, добавляють 4 - 5 крапель розчину реактиву і потирають об стінки пробірки скляною паличкою при охолодженні розчину в струмені води. Випадання кристалічного зеленувато-жовтого осаду свідчить про наявність йонів Натрію. Дослід 3. Проба на забарвлення полум'я. Солі натрію забарвлюють полум'я газового пальника у жовтий колір. Проба на забарвлення полум'я характеризується високою чутливістю. Виконання досліду. Дослід виконують, вносячи крупинки сухої солі Натрію на платиновій дротинці в полум'я пальника, і спостерігають появу інтенсивного яскраво-жовтого забарвлення, яке має зберігатися впродовж декількох секунд. Реакції виявлення йона К+ Дослід 4. Реакція з натрій гексанітрокобальтатом (ІІІ). Комплексна сполука Na3[Co(NО2)6], яку називають натрій гексанітрокобальтатом (Ш), або кобальтинітритом, у нейтральному середовищі утворює з іонами Калію жовтий кристалічний осад калій-натрій кобальтинітриту: 2 KCI + Na3[Co (NO2)6] = K2Na[Co(NО2)6]↓ + 2NaCl 2 К+ + Na+ + [Co(NО2)6]3- = K2Na[Co(NО2)6] ↓ Реактив Na3[Co(NO2)6] повинен бути свіжоприготовленим, оскільки при зберіганні він розкладається з виділенням іонів Co2+ рожевого забарвлення і такий розчин непридатний для використання. Виконання досліду. До 2-3 крапель розчину солі K+ додайте 3 краплі реактива Na3[Co(NO2)6] і потріть скляною паличкою внутрішню стінку пробірки. Випадає жовтий кристалічний осад K2Na[CO(NO2)6]. Досліджуваний розчин повинен мати pH не більше 7, бо в лужному середовищі реактив Na3[Co(NO2)6] легко розкладається з утворенням темно-бурого аморфного осаду Co(OH)3: Na3[Co(NO2)6] + 3NaOH = Co(OH)3↓ + 6NaNO2, а в сильнокислому утворюєтсья нестійка кислота H3[Co(NO2)6]: 2Na3[Co(NO2)6] + 6HCl = 2H3[Co(NO2)6] + 6NaCl, яка в момент утворення розкладається з виділенням оксидів нітрогену: 2H3[Co(NO2)6] + 4HCl = 2CoCl2 + 5NO↑ + 7NО2↑ + 5H2O. В ацетатній кислоті ані реактив, ані утворений осад не розчиняються.
Потирання скляною паличкою стінок пробірки попереджує утворення пересиченого розчину і прискорює випадання осаду. Дослід 5. Реакція з натрій гідрогентартратом NaHC 4 H 4 О6. Натрій гідрогентартрат NaHC4H4О6 утворює з іонами Калію білий кристалічний осад калій гідрогентартрату: КСl + NaHC4H4O6 = КНС4Н4О6↓ + NaCl K++HC4H4O6- = KHC4H4O6↓ Виконання досліду. У пробірку вносять 4-5 крапель розчину солі Калію і стільки ж розчину реактиву. Розчин охолоджують і потирають об внутрішні стінки пробірки скляною паличкою для прискорення утворення осаду. Середовище має бути нейтральним або слабкокислотним. Чутливість реакції — 50 мкг, граничне розбавляння 1:1000. Катіони NH4+ перешкоджають визначенню, тому їх усувають прожарюванням проби. Дослід 6. Проба на забарвлення полум'я. Солі Калію при внесенні в полум 'я газового пальника забарвлюють його у фіолетовий колір. Виконання досліду. На кінчику платинової дротинки вносять краплю солі Калію в полум'я газового пальника і спостерігають за забарвленням полум'я. Навіть сліди сполук Натрію маскують фіолетове забарвлення йонів Калію. Тому його забарвлення потрібно спостерігати крізь синє кобальтове скло, яке затримує жовті промені Натрію.
Реакції катіонів амонію NH 4 +
Дослід 7. Реакція з гідроксидами лужних металів. Сильні основи NаОН, КОН при нагріванні виділяють із розчинів солей амонію газуватий амоніак, який можна виявити за характерним запахом або за допомогою кислотно-основних індикаторів: NH4+ + ОН- = NH3↑ + Н2O Реакція з лугами дуже чутлива ( 0,01мкг) і дає змогу виявити іони амонію за наявності всіх інших катіонів. Виконання досліду. У пробірку вносять кілька крапель розчину солі амонію і добавляють 3 - 4 краплі 2Мрозчину лугу. До отвору пробірки підносять змочений водою червоний лакмусовий папірець і нагрівають пробірку. Спостерігають посиніння лакмусового папірця, оскільки амоніак, що виділяється, сполучаючись з водою, утворює амоній гідроксид, який забарвлює лакмусовий папірець у синій колір Дослід 8. Реакція з реактивом Несслера. Реактив Несслера — це суміш комплексної солі K2[HgI4] з КОН. Він утворює з солями амонію червоно-бурий осад йодиду дийододимеркуріату [Hg2I2NH2]І: NH4C1+ 2 К2 [HgI4] + 2 КОН = [Hg2I2NH2]І(т) + + 5КІ + КС1 + 2Н2O. NH4+ + 2 [HgI4]2- + 2ОН- = [Hg2I2NH2]І↓ + 5I- + 2Н2O. З надлишком лугу утворюється йодид оксодимеркурамонiю, структуру якого можна зобразити так: NH3 + 2K2[HgI4] + KOH = [NH2HgI2]I↓+ 5KI + H2O
Реакція характеризується високою чутливістю (0,25 мкг), тому її використовують для перевірки повноти виділення амоніаку з реакційної суміші, в біохімічному аналізі — для визначення залишкового Нітрогену в крові, а в екологічних дослідженнях — для аналізу стічних вод, харчових продуктів тощо. Виконання досліду. До 1 - 2 крапель розчину амонійної солі добавляють 4 краплі реактиву Несслера і спостерігають утворення бурого осаду. За незначного вмісту солей амонію в пробі (сліди) з'являється жовте забарвлення. Дослід 9. Термічний розклад солей амонію. Якщо солі амонію в розчині видалити, їх потрібно відокремити, оскільки катіон NH4+ заважає виявленню йонів К+, утворюючи осади з Na3[Co(NО2)6], NaHC4H4О6 і Na2Pb[Cu(NО2)6]. Крім цього, солі амонію, гідролізуючи, утворюють мінеральні кислоти, що розкладають K[Sb(OH)6] з виділенням осаду метасурмяної кислоти HSbО3. Йони NH4+ заважають також виявленню йонів Na+ дією з гексагідроксостибіатом калію. Для видалення катіона NH4+ використовують властивість солей амонію при високих температурах легко розкладатися та випаровуватися, утворюючи газоподібні продукти, наприклад: NH4C1 (NH4)2CO3 (NH4)3PО4 NH4NО3 Виконання досліду. Досліджуваний розчин переливають у фарфорову чашку, обережно випарюють до сухого вигляду і прожарюють на піщаній бані до повного видалення солей амонію. Для перевірки повноти видалення цих солей беруть кілька кристалів сухого залишку, переносять у пробірку, добавляють кілька крапель води і 1 - 2 краплі реактиву Несслера. Утворення бурого осаду свідчить про неповне видалення катіона NH4+, тому продовжують прожарювати. Реакції виявлення йона Mg 2+ Для вивчення реакцій Mg2+ беруть розчин хлориду MgCl2 або сульфату магнію MgSO4. Реакції Mg2+ сильно відрізняються від реакцій інших катіонів 1- ї групи. Винятком є реакція з гексагідроксостибіатом калію, при якій йон Mg2+ утворює осад Mg[Sb(OH)6]2, що зовні не відрізняється від Na[Sb(OH)6] отже, Mg2+ заважає виявленню Na+.
Дослід 10. Реакція з л угами NaOH або КОН. Луги NaOH і КОН виділяють із розчинів солей Mg2+ білий аморфний осад гідроксиду: MgCl2 + 2КОН = Mg(ОН)2↓ + 2КС1 Mg2+ +2ОН- = Mg(ОН)2↓ У ході аналізу цю реакцію використовують для відділення Mg2+ від інших катіонів І-ої групи, гідрооксиди яких добре розчинні у воді. Водний аміак осаджує іони Mg2+ не повністю. У присутності ж солей NH4+ дисоціація NH4OH настільки пригнічується, що осад гідрооксиду магнію Mg(OH)2 не випадає (через недостачу іонів ОН- у розчині). Виконання досліду. До 2-3 крапель розчину солі Mg2+ додають стільки ж розчину їдкого калію КОН; зверніть увагу на аморфний характер осаду Mg(OH)2. В іншій пробірці до 2 крапель розчину солі Mg2+ долийте спочатку 2 краплі насиченого розчину хлориду амонію NH4C1, a потім 2 краплі розчину аміаку. Переконайтеся, що осад не випадає. Очевидно, що гідроксид магнію розчиняється не тільки в кислотах, але також і в солях амонію. Підтвердіть це рівняннями відповідних реакцій. Дослід 11. Реакція з гідрофосфатом натрію Na2HPО4. Гідрофосфат натрію Na2HPО4 у присутності гідроксиду й хлориду амонію утворює із солями Mg2+ білий кристалічний осад фосфату магнію-амонію:
MgCl2 + Na2HPО4 + NH4OH = MgNH4PО4 ↓ +2NaCl + H2О Хлорид амонію додають, щоб запобігти утворенню осаду Mg(OH)2, внаслідок взаємодії MgCl2 з NH4OH. Фосфат амонію розчинний у мінеральних кислотах і навіть в оцтовій кислоті, тому реакцію виконують у нейтральному або слаболужному розчині. Виконання досліду. До 2 - 3 крапель розчину солі Mg2+ додають 2 краплі розчину, хлориду амонію й 4 краплі реактиву Na2HPО4. Потім додають 2 н. NH4OH до лужної реакції (проба з лакмусовим папірцем), або до появи запаху аміаку). Розчин перемішують скляною паличкою після додавання кожної краплі реактиву. З розведених розчинів осад випадає не відразу: появу його можна прискорити збовтуванням або потиранням паличкою об стінки пробірки. Іноді дають розчину постояти 15 - 20 хв. Реакція з гідрофосфатом натрію досить чутлива й найчастіше використовується для виявлення Mg2+ у ході систематичного аналізу. Катіони інших аналітичних груп (крім 1-й групи) заважають виявленню Mg2+, оскільки теж утворюють із гідрофосфатом натрію нерозчинні фосфати, тому їх необхідно видалити. Дослід 12. Реакція з розчинними карбонатами (Na 2 C О3 або К2СО3). Розчинні карбонати Na2CО3 і К2СО3 виділяють із розчинів солей Mg2+ білий аморфний осад основного карбонату: 2MgCl2 + 2Na2CO3 + Н2О = (MgOH)2СО3↓ + 4NaCl + СО2 ↑ 2Mg2+ + 2СО32- + Н2О = (MgOH)2 CО3 ↓ + CО2 ↑ Виконання досліду. До 2-3 крапель розчину солі Mg2+ додають однаковий об’єм розчину карбонату натрію Na2CО3. Переконайтеся, що осад (MgOH)2CО3 розчиняється в кислотах. Карбонат амонію також частково осаджує іони Mg2+ у вигляді основної солі: 2MgCl2 + 2(NH4)2CO3 + H2O →← (MgOH)2CO3 ↓ + 4NH4Cl + CO2↑ Однак ця реакція оборотна, і рівновага її сильно зміщена вліво. Якщо ж до розчину попередньо додати небагато хлориду амонію, то осад гiдроксокарбонату магнію (MgOH)2CО3 не утвориться. Переконайтес, що осад основного карбонату магнію розчинний у солях амонію. Розчинність (MgOH)2CО3 у надлишку солей амонію використовують для відділення Mg2+ від катіонів 2-й групи, що осаджуються карбонатом амонію. Іон Mg2+, що залишається при цьому в розчині, відносять до 1-й аналітичної групи. Дослід 13. Реакція з хромогеном чорним (еріохромом чорним Т). Органічний барвник хромоген чорний спеціальний ЕТ-00, що має склад C20H13O7N3S, утворює з іонами Mg2+ комплекс винно-червоного кольору. Виконання досліду. До 4-5 крапель розчину солі Mg2+ додають 1-2 краплі розчину аміаку (або амонійної буферної суміші) і 2-3 краплі розчину хромогену чорного. Розчин стає винно-червоним, але осад не випадає, тому що утворена сполука добре розчинна у воді. Замість розчину хромогену чорного можна додати кілька крупинок сухої суміші барвника із хлоридом натрію у співвідношенні 1: 100. 2.2. Якісні реакції катіонів I І аналітичної групи (Ca 2+, Sr 2+, Ba 2+) Дослід 14. Дія групового реагента ─ амоній карбонату (NH 4)2СО3. Катіони ІІ-ої групи (Ca2+, Sr2+, Ba2+) осаджують дією амоній карбонату (NH4)2СО3 в присутності амоній гідроксиду NH4ОН (для пригнічення гідролізу (NH4)2СО3) та хлориду NH4Сl при нагріванні розчину до 50 – 70 оС (для пригнічення розкладу (NH4)2СО3 та зміщення рівноваги в сторону вихідного реагента) з утворенням аморфних осадів, що легко кристалізуються під час нагрівання: Са2+ + СО32- = СаСО3↓ Ва2+ + СО32- = ВаСО3↓ Sr2+ + СО32- = SrСО3↓. Груповий реагент (NH4)2СО3 гідролізує з утворенням кислої солі NH4НСО3 і у розчині появляються кислі аніони НСО3-: (NH4)2СО3 + Н2О ↔ NH4НСО3 + NH4ОН. Гідроліз групового реагенту заважає повному осадженню катіонів другої групи, бо кислі солі Ca(HCO3)2, Sr(HCO3)2, Ba(HCO3)2 розчинні у воді. Додавання NH4ОН призводить до зміщення рівноваги вліво, при цьому гідрокарбонат-іони НСО3- переходять в карбонат-іони СО32-, що сприяє процесові осадження. Для осадження катіонів другої аналітичної групи можна було б використати Na2CO3 чи K2CO3. Однак використовувати ці реагенти для відокремлення катіонів другої аналітичної групи недопустимо, бо у розчин додатково вносяться йони Na+ чи K+, яких, наприклад, у вихідному розчині не було. Застосування ж карбонату амонію не приведе до такої помилки, бо катіон NH4+ легко виявити у вихідному розчині дробним способом. Крім того, карбонат амонію частково розкладається з утворенням карбамінату амонію, що теж сприяє певному осадженню катіонів другої групи: (NH4)2CO3 ↔ NH2COONH4 + H2O. Однак при нагріванні розчину до 50 – 70 оС ця рівновага зміщується вліво. Нагрівання сприяє також утворенню кристалічних осадів карбонатів (замість аморфних), які краще відфільтровуються. Виконання досліду. У три пробірки вносять 2 - 3 краплі розчинів солей хлоридів кальцію, барію та стронцію, почергово додають до кожної по одній краплі буферної суміші (розчин NH4ОН з NH4Сl), далі додають розчин групового реагенту (NH4)2СО3. Спостерігають утворення осадів, перевіряють їх розчинність в розчинах мінеральних кислот. Записують рівняння відповідних реакцій. Таким чином, катіони другої групи осаджують карбонатом амонію (NH4)2CO3 в присутності NH4OH і NH4Cl при нагріванні розчину до 50 – 70оС.
Реакції виявлення катіонів Кальцію Са2+
Дослід 15. Реакція з амоній оксалатом. Амоній оксалат (NH4)C2О4 утворює з іонами Кальцію білий дрібнокристалічний осад кальцій оксалату: Са2+ + С2О42-= СаС2О4↓, розчинний у мінеральних (крім оцтової) кислотах. Нагрівання сприяє швидшому осадженню осаду. Цією реакцією виявляють катіон Кальцію лише після видалення з розчину катіонів Ва2+ і Sr2+, які також утворюють осади з (NH4)C2О4, і заважають відкриттю йона Са2+. Виконання досліду. До 4 - 5 крапель розчину солі кальцію (хлориду або нітрату) додають таку саму кількість реактиву. Спостерігають утворення осаду. Досліджують його розчинність у мінеральних кислотах (НС1, HNО3), а також в ацетатній кислоті. Дослід 16. Реакція з калій гексаціанофератом (ІІ). Калій гексаціаноферат (II) К4[Fe(CN)6] (жовта кров'яна сіль) у середовищі гідроксиду та хлориду амонію (буферної суміші з рН ≈ 9) утворює з іонами Кальцію білий кристалічний осад подвійної солі кальцій-амоній гексаціаноферату (II), нерозчинного в ацетатній кислоті: СаС12+ 2NH4C1 + К4[Fe (CN)6] = Са(NH4)2[Fe (CN)6]↓ + 4KCl Ca2+ + 2NH4+ + [Fe(CN)6]4- = Ca(NH4)2[Fe(CN)6]↓. Виконання досліду. До 3 - 5 крапель розчину солі кальцію додають такий самий об'єм амонійного буферного розчину (суміш NH4ОН і NH4Cl) для підтримання постійного рН розчину (рН ≈ 9) і нагрівають на водяній бані. До гарячого розчину додають 5 - 6 крапель насиченого розчину жовтої кров'яної солі й суміш знову нагрівають. Спостерігають утворення осаду. Іони Ва2+ також утворюють осад з К4[Fe(CN)6], отже заважають виявленню Са2+. Чутливість реакції становить 25 мкг, але визначення іонів Са2+ не можливо провести за наявності катіонів d-елементів (Феруму, Купруму, Цинку), які також реагують з цим реактивом. Дослід 17. Реакція з розчинними сульфатами. Розчинні сульфати осаджують йони Са2+ з концентрованих розчинів з утворенням білого кристалічного осаду CaSО4: Ca2+ + SО42- = CaSО4↓ При додаванні до досліджуваного розчину етанолу осад випадає швидше. Осад розчиняється в сульфаті амонію (NH4)2SО4 з утворенням комплексної солі (NH4)2[Ca(SО4)2]. Розчини солей Са2+, на відміну від Ва2+ и Sr2+, не дають помутніння із гіпсовою водою. Виконання досліду. У пробірку вносять 2 - 3 краплі розчину солі кальцію, додають 1 - 2 краплі розчину сульфату й спостерігають утворення білого кристалічного осаду CaSО4, Дослід 18. Проба на з абарвлення полум'я. Солі кальцію забарвлюють полум'я газового пальника в цегляно-червоний колір. Виконання досліду. На кінчику платинової дротинки вносять краплю солі Кальцію в полум'я газового пальника і спостерігають його забарвлення. Реакції виявлення катіонів Ва2+ Дослід 19. Реакція з дихроматом або хроматом калію. Розчинні солі дихроматної або хроматної кислот виділяють з розчинів, що містять солі Барію, жовтий кристалічний осад барій хромату ВаСгО4: 2Ba2+ + Cr2О72- + H2О = 2BaCrО4↓ + 2Н+ (а) або Ва2+ + СгО42- = ВаСгО4↓ (б). В розчинах іони Cr2O72- знаходяться в рівновазі з CrO42-: Cr2O72- + H2O ↔ 2CrO42- + 2Н+, але оскільки ДР солі BaCrO4 досягається швидше, ніж ДР (BaCr2O7) то в осад випадає менш розчинна сіль BaCrO4. Сумарне рівняння має такий вигляд: K2Cr2O7 + 2BaCl2 + H2O ↔ 2BaCrO4↓ + 2KCl + 2HCl Внаслідок реакції утворюється сильна хлоридна кислота, в якій осад BaCrO4 розчиняється, тому осадження йона Ba2+ може бути неповним. Для повного осадження Ba2+ до розчину разом з дихроматом калію додають ацетат натрію. Останній, взаємодіючи з HCl утворює слабу ацетатну кислоту CH3COOH, в якій осад BaCrO4 не розчиняється. Оскільки осад ВаСгО4 розчиняється в мінеральних кислотах, а в процесі взаємодії йонів Барію з дихроматом (реакція (а)) утворюється кислота, то для досягнення повноти осадження йонів Ва2+ розчином К2Сг2О7 до нього добавляють натрій ацетату CH3COONa. Тоді сильна кислота (НС1) замінюється еквівалентною кількістю слабкої ацетатної кислоти, в якій барій хромат не розчиняється: НС1 + NaCH3COO = НСН3СОО + NaCl Виконання досліду. У пробірку вносять 2 - 3 краплі розчину солі барію, добавляють 1 - 2 краплі розчину ацетату натрію та 2 – 3 краплі реактиву К2Сг2О7 (або калій хромату) і спостерігають утворення осаду. Випробуйте розчинення осаду в хлоридній та ацетатній кислотах. Реакція з дихроматом є специфічною і використовується для виявлення йонів Ва2+ за наявності катіонів Са2+ і Sr 2+ та для відокремлення йонів Барію від цих катіонів. Дослід 20. Реакція з амоній оксалатом. Амоній оксалат (NH4)C2О4 утворює з іонами барію білий осад барій оксалату: Ва2+ + С2О42- = ВаС2О4↓ Виконання досліду. Одержаний осад оксалату барію ВаС2О4 розділяють на три частини й перевіряють його розчинність в хлоридній, нітратній, а при нагріванні й у ацетатній кислотах. Дослід 21. Реакція з сульфатною кислотою (або розчинними сульфатами). Сульфатна кислота або її розчинні солі утворюють з катіоном Ba2+ білий дрібнокристалічний осад BaSО4, який не розчиняється у воді й мінеральних кислотах: Ba2+ + SO42- = BaSО4↓. Чутливість цієї реакції висока (10 мкг), оскільки барій сульфат характеризується малою розчинністю у воді. Виявленню йонів Ва2+ перешкоджають йони Са2+- і Sr2+. Виконання досліду. У пробірку вносять 2 - 3 краплі розчину солі барію, добавляють стільки ж розбавленого розчину сульфатної кислоти (або розчину сульфату натрію Na2SO4) і спостерігають випадання осаду. Перевіряють розчинність сульфату барію у воді та в кислотах. Для переведення BaSО4 в розчин, його нагрівають з насиченим розчином карбонату натрію (мокрий спосіб): BaSО4 + Na2CO3 →← ВаСО3 + Na2SО4 або сухим способом – сплавлянням його в тиглі з надлишком карбонатів (К2СО3 і Na2CО3). Дослід 22. Реакція з гідрофосфатом натрію Na 2 HP О4. Гідрофосфат натрію утворює з іоном Ва2+ білий осад, розчинний в хлоридній, нітратній та оцтовій кислотах: Вa2+ +НРО42- = BaHPO4↓, Гідрофосфат барію розчиняється в оцтовій кислоті внаслідок одержання малодисоційованих йонів Н2РО4- згідно рівняння ВаНРО4 + Н+ = Ba2++ H2PO4- З іонами Sr2+ і Са2+ гідрофосат натрію також утворює білі осади гідрогенфосфату стронцію SrHPО4 і гідрогенфосфату кальцію СаНРО4, котрі розчиняються в цих же кислотах. Виконання досліду. До 3 - 4 крапель слабокислого розчину солі барію додають таку ж кількість натрій гідрогенфосфату. Утворення білого аморфного осаду вказує на присутність іона барію. Досліджують розчинність цього осаду в кислотах. Записують рівняння відповідних реакцій. Дослід 23. Проба на з абарвлення полум'я. Леткі солі барію забарвлюють полум'я газового пальника у жовто-зелений колір. Виконання досліду. Краплю солі барію на кінчику платинової дротинки вносять у полум'я газового пальника й спостерігають за забарвленням полум'я. Реакції виявлення катіонів Стронцію Sr2+ Дослід 24. Реакція з сульфатною кислотою (або розчинними сульфатами). Сульфатна кислота або її розчинні солі утворюють з розчинами солей стронцію білий осад SrSО4, який не розчиняється у воді та кислотах: Sr2++ SО42- = SrSО4↓. Виконання досліду. У пробірку вносять 2 - 3 краплі розчину солі Стронцію, добавляють стільки ж розбавленого розчину сульфатної кислоти і спостерігають випадання осаду, який практично не розчинний у кислотах і переводиться в розчин при нагріванні з карбонатом натрію. Дослід 25. Реакція з гіпсовою водою. Гіпсова вода CaSО4´2Н2О утворює з катіонами Sr2+ білий осад стронцій сульфату. Оскільки розчинність SrSО4 (ДР = 3,2·10-7) менша, ніж розчинність CaSО4 (ДР = 2,5·10-5), то в осад випадає SrSО4. Гіпсова вода є характерним реактивом для виявлення йонів Стронцію, однак цю реакцію не можна проводити за наявності у розчині йонів Ва2+, оскільки Барій також утворює з гіпсовою водою білий осад барій сульфату (ДР = 1,1·10-10). При цьому Барій утворює осад BaSО4 за звичайних умов, а Стронцій — тільки після нагрівання розчину. Виконання досліду. До 6 - 7 крапель розчину солі стронцію добавляють 10 крапель гіпсової води, суміш кип'ятять упродовж 1-2 хв. і залишають на 5 - 6 хв. для охолодження. Спостерігають за появою білого дрібнокристалічного осаду SrSО4. Дослід 26. Реакція з амоній оксалатом. Амоній оксалат (NH4)2С2О4 утворює з йонами стронцію білий осад стронцій оксалату: Sr2+ + C2О42- = SrC2О4↓. Осад добре розчиняється як у мінеральних, так і в ацетатній кислоті при нагріванні. Виконання досліду. До 4 - 5 крапель розчину солі стронцію добавляють стільки ж реактиву. Спостерігають утворення осаду. Випробовують його розчинність у кислотах. Дослід 27. Проба на з абарвлення полум'я. Леткі солі Стронцію забарвлюють полум'я газового пальника в карміново-червоний колір. Виконання досліду. Краплю солі стронцію на кінчику платинової дротинки вносять у полум'я газового пальника і спостерігають за забарвленням полум'я. 2.3. Якісні реакції катіонів I ІІ аналітичної групи (А13+, Сг3+, Fe 3+, Fe 2+, Mn 2+, Zn 2+, Со2+, Ni 2+) Дія групового реагента ─ (NH 4)2 S
Як зазначалося вище, груповий реагент сульфід амонію ((NH4)2S) осаджує Fe3+, Fe2+, Mn2+, Zn2+, Со2+ і Ni2+ в вигляді сульфідів, А13+ і Сг3+- у вигляді гідроксидів катіонів 3-ої групи. Сульфіди й гідроксиди катіонів ІІІ-ої групи розчинні в сильних кислотах. Тому вільні кислоти у досліджуваному розчині повинні бути нейтралізовані аміаком. Груповий реагент дуже легко гідролізує, ступінь його складає 99,9 %: (NH4)2S+H2O →← NH4HS + NH4OH. Щоб запобігти гідролізу групового реагента і забезпечити повне осадження катіонів 3-ої аналітичної групи до розчину додають водний розчин аміаку, який зміщує рівновагу гідролізу вліво. Крім того, сульфіди деяких катіонів 3-ої аналітичної групи легко переходять у колоїдний стан. Щоб попередити це небажане явище, осадження ведуть у присутності електроліта-коагулятора NH4C1 з гарячого розчину. Хлорид амонію додають ще й для того, щоби після введення NH4OH не випав осад гідроксиду магнію Мg(OH)2 (катіон Мg2+, як відомо, належить до І-ої аналітичної групи). Таким чином, катіони ІІІ-ої групи осаджуються сульфідом амонію (NH4)2S у присутності амонійної буферної суміші (розчин NH4ОН з NH4Сl) при рН ≈ 9. Катіони І-ої і ІІ-ої груп залишаються при цьому в розчині. Для осадження придатні тільки свіжоприготовлені реактиви, тому що при зберіганні (NH4)2S і NH4OH, поглинають вуглекислий газ з повітря і частково перетворюються в карбонат амонію (NH4)2CО3 (груповий реагент ІІ-ої групи катіонів). Присутність його в реактивах, як і присутність сульфату амонію, недопустима. Адже при цьому разом з 3-ою групою будуть осаджуватися й катіони 2-ї групи. Щоб вивчити забарвлення, характерні для осадів солей катіонів ІІІ-ої аналітичної групи з груповим реагентом, а також їх розчинність, слід проробити наступні реакції. Виконання досліду. До 2 крапель розчинів солей Fe3+, Fe2+, Mn2+, Ni2+ і Со2+ в окремих пробірках додайте по 2 краплі розчину сульфіду амонію, спостерігайте випадання осадів. Наприклад: 2Fe3+ + 3S2- = Fe2S3↓, Мn2+ + S2- = MnS↓, Zn2+ + S2- = ZnS↓ Зверніть увагу на те, що осади Fe2S3, FeS, CoS и NiS - чорного, MnS - тілесного, a ZnS - білого кольору. Отримані сульфіди (крім Co і Nі) розчиняються в розведених сильних кислотах з виділенням сірководню. При розчиненні сульфіду заліза (ІІІ) Fe2S3 іон Fe3+ частково відновлюється до Fe2+ і випадає вільна сірка Fe2S3 + 4HCl = 2FeCl2 + S↓ + 2H2S↑
Подійте сульфідом амонію на розчини солей А13+ і Сг3+. Запам'ятайте, що осад А1(ОН)3 - білого, а Сг(ОН)3 - сіро-фіолетового кольору. Хоча в розчині (NH4)2S одночасно присутні іони S2- і іони ОН-, добутки розчинності гідроксидів досягаються раніше, ніж відповідних сульфідів, і в осад випадають гідроксиди А1(ОН)3 або Сг(ОН)3. Утворення гідроокису алюмінію можна зобразити схемою: 3 (NH4)2S + 6HaO →← 6NH4OH + 3H2S ↑ Al2(SO4)3 + 6NH4OH → ← 2Al (OH)3 ↓ + 3(NH4)2SO4 Переконайтеся, що осади гідроксидів алюмінію й хрому, так само як сульфіди катіонів 3-ої групи, розчиняються в розведених сильних кислотах. Реакції виявлення іона А l 3+ Дослід 1. Реакція з лугами NaOH або КОН. Їдкі луги КОН і NaOH осаджують з розчинів солей алюмінію білий аморфний осад алюміній гідроксиду А1(ОН)3. Виконання досліду. До 3-4 крапель розчину солі алюмінію повільно добавляють 2н. розчин NaOH до утворення осаду: А13+ + 3ОH- = А1(ОН)3↓. Осад має А1(ОН)3 амфотерні властивості, а тому розчиняється як в кислотах, так і в лугах. Розділіть осад порівну у дві пробірки. До однієї пробірки долийте розчин хлоридної кислоти, до другої – розчин гідроксиду натрію або калію. Переконайтеся, що осад розчиняється і в кислоті, і в лугові згідно реакцій:
|
|||||||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 102; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.146.105.137 (0.162 с.) |

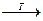 NH3 + HCl
NH3 + HCl