Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Анализ атмосферного воздуха.
Основным видом воздействия промышленных объектов на состояние воздушного бассейна является загрязнение атмосферного воздуха выбросами загрязняющих веществ, которое происходит в результате поступления в него продуктов сгорания топлива, выбросов газообразных и взвешенных веществ от различных производств, выхлопных газов автомобильного транспорта, испарений из емкостей для хранения химических веществ и топлива, пыли из узлов погрузки, разгрузки и сортировки сыпучих строительных материалов, топлива, зерна и т.п. В соответствии с требованиями федерального закона «Об охране атмосферного воздуха» юридические лица, имеющие источники выбросов вредных (загрязняющих) веществ в атмосферный воздух, должны разрабатывать и осуществлять мероприятия по охране атмосферного воздуха. Производство и использование на территории Российской Федерации технических, технологических установок, транспортных средств допускаются только при наличии сертификатов, устанавливающих соответствие содержания вредных (загрязняющих) веществ в их выбросах техническим нормативам выбросов. Запрещается выброс в атмосферный воздух веществ, степень опасности которых для жизни и здоровья человека и для окружающей природной среды не установлена. Виды и количество загрязняющих веществ, выбрасываемых в атмосферу промышленным предприятием зависят от технологических процессов производств. В целях охраны атмосферного воздуха составляют перечень производств и объектов, являющихся источниками загрязнения атмосферы, с указанием видов загрязняющих веществ в выбросах, их класса опасности и параметров выбросов. Анализ воздуха на химические и бактериологические показатели производится в городских и сельских поселениях, на территориях промышленных организаций, в рабочих зонах производственных помещений, жилых и других помещениях, согласно государственным санитарно-эпидемиологическим правилам, где установлены единые санитарно-эпидемиологические требования к атмосферному воздуху в местах постоянного или временного пребывания человека. Юридические лица, имеющие источники выбросов загрязняющих веществ в атмосферный воздух, обязаны: · разрабатывать и осуществлять планы организационно - технических или иных мероприятий, направленные на обеспечение качества атмосферного воздуха санитарным правилам;
· обеспечить разработку ПДК или ОБУВ для веществ, не имеющих нормативов; · обеспечить проведение лабораторных исследований загрязнения атмосферного воздуха (анализ проб воздуха) мест проживания населения в зоне влияния выбросов объекта; · получать санитарно - эпидемиологическое заключение органов и учреждений государственной санитарно - эпидемиологической службы на все изменения технологического процесса или оборудования (увеличение производственной мощности, изменение состава сырья, номенклатуры выпускаемой продукции и другие отклонения от утвержденного проекта); · обеспечить работы по проектированию, организации и благоустройству санитарно - защитных зон на объектах, не имеющих организованные зоны в соответствии с действующими санитарными правилами; · информировать органы и учреждения государственной санитарно – эпидемиологической службы о всех случаях нерегламентированных и аварийных выбросов вредных примесей в атмосферный воздух, разрабатывать мероприятия по их ликвидации и предотвращению аналогичных ситуаций; · выполнять в установленные сроки предписания органов и учреждений государственной санитарно - эпидемиологической службы по устранению нарушений санитарных правил. Санитарно-эпидемиологические правила и нормативы СанПиН 2.1.6.1032-01 регламентируют предельно допустимые нормы содержания примесей в атмосферном воздухе и воздухе закрытых помещений. Анализ воздуха в квартире и других жилых строениях необходимо проводить после ремонта и периодически (1 раз в год) во время проживания, т.к. нередко конструкции и наполнение дома выделяют фенол, формальдегид, стирол. Опасные выделения могут исходить от потолка, стен, отделки, предметов мебели и интерьера. Химические средства, используемые при уборке квартиры, также небезопасны. Нафталиновые шарики, отбеливатели, краски, различные чистящие средства, дезодоранты - лишь немногие из широкого спектра химикатов, воздействию которых подвергается практически ежедневно каждый человек, и которые выделяют канцерогенные вещества. Например, пластики, синтетические волокна и очистители испаряют бензол, а пенопластиковые теплоизоляторы, фанера, древесно-стружечные плиты являются источниками формальдегида. Подобные эмиссии могут вызывать головную боль, головокружение и тошноту. Вдыхание асбестовых волокон вызывает заболевание асбестоз. Эта проблема особенно актуальна для владельцев домов, построенных в советский период.
IV. Химия и гидросфера (6 часов) Вода – уникальное вещество Вода, у тебя нет вкуса, нет цвета, нет запаха, тебя невозможно описать; люди тобою наслаждаются, при этом не ведая, что ты есть такое… Нельзя сказать, что ты необходима для жизни: ты есть сама жизнь Антуан де Сент-Экзюпери В 1780 г. Кавендиш и Лавуазье установили, что вода – простейшее и устойчивое в обычных условиях химическое соединение двух атомов водорода и одного атома кислорода. Чистая вода представляет собой бесцветную прозрачную жидкость без вкуса и без запаха. Половина всей крови человека - чистейшая дистиллированная вода. Мышцы человека на 75% состоят из воды. Вода является важнейшим пищевым продуктом. Дегидратация, или потеря организмом воды, нарушает деятельность сердечно - сосудистой системы, клеточный метаболизм и терморегуляцию. Потеря всего 3% воды организмом лишает человека возможности бегать. Потеря 5% воды лишает возможности тренироваться. А потеря организмом 10% воды представляет опасность для жизни. Плотность воды при переходе ее из твердого состояния в жидкое не уменьшается, как почти у всех других веществ, а возрастает. При нагревании воды от 0 до 4 градусов по Цельсию плотность ее увеличивается. При 4 градусах вода имеет максимальную плотность. При дальнейшем нагревании ее плотность снова уменьшается. Замерзание воды сопровождается не сжатием (как у других жидкостей), а наоборот расширением. Затвердевая, вода становится менее плотной – поэтому лед плавает, а не тонет. Лед тем самым защищает нижележащие слои воды от дальнейшего охлаждения и замерзания. Таким образом, жизнь в воде продолжается. Высокая, по сравнению с соединениями водорода с похожим молекулярным весом, температура и удельная теплота плавления (0 °C и 333,55 кДж/кг), температура кипения (100 °C) и удельная теплота парообразования (2250 КДж/кг). В ночное время, а также при переходе от лета к зиме вода остывает медленно, а днем или при переходе от зимы к лету так же медленно нагревается, являясь, таким образом, самым главным регулятором температуры на земном шаре.
Из-за большой разности электроотрицательностей атомов водорода и кислорода электронные облака сильно смещены в сторону кислорода, тогда как 2 атома водорода в сумме формируют достаточно большую "площадь» распределения положительного заряда в «углах» молекулы. Несколько таких диполей будут образовывать структуры типа: Н2О...Н2О с водородной связью, когда между двумя атомами водорода будет втянут атом кислорода соседней молекулы. При этом общее распределение потенциала будет стремиться к минимизации взаимодействия с внешней средой, следовательно, молекулы воды будут располагаться в пространстве с чёткой ориентацией, в виде пространственных структур разной сложности: от спиралевидных (как у молекул ДНК) до пирамидальных, кубических, сферических разной сложности. Каждая молекула воды может участвовать максимум в четырёх водородных связях: 2 атома водорода – каждый в одной, а атом кислорода – в двух. Простая, не объединившаяся с другой молекула воды H2O, называется гидроль, (H2O)2 – дигидроль, (H2O)3 – тригидроль. В парообразном состоянии вода в основном состоит из молекул гидроля, в жидком состоянии вода – смесь гидроля, дигидроля и тригидроля, во льду преобладают молекулы тригидроля. При таянии льда часть связей рвётся, при нагревании воды связи продолжают рваться, и плотность её растёт, но при температуре выше 4 °С этот эффект становится слабее, чем тепловое расширение. При испарении рвутся все оставшиеся связи. Разрыв связей требует много энергии, отсюда высокая температура и удельная теплота плавления и кипения и высокая теплоёмкость. Вязкость воды обусловлена тем, что водородные связи мешают молекулам воды двигаться с разными скоростями. По сходным причинам вода является хорошим растворителем полярных веществ. Каждая молекула растворяемого вещества окружается молекулами воды, положительно заряженные участки молекулы растворяемого вещества притягивают атомы кислорода, а отрицательно заряженные – атомы водорода. Поскольку молекула воды мала по размерам, каждую молекулу растворяемого вещества могут окружить много молекул воды. Это свойство воды используется живыми существами. В живой клетке и в межклеточном пространстве вступают во взаимодействие растворы различных веществ в воде. Вода необходима для жизни всех без исключения одноклеточных и многоклеточных живых существ на Земле.
Чистая (не содержащая примесей) вода – хороший изолятор. Но поскольку вода – хороший растворитель, в ней практически всегда растворены те или иные соли, то есть в воде присутствуют положительные и отрицательные ионы. Благодаря этому вода проводит электричество. По электропроводности воды можно определить её чистоту. Она сильно поглощает инфракрасное излучение, и поэтому водяной пар является основным естественным парниковым газом, отвечающим более чем за 60 % парникового эффекта. Благодаря большому дипольному моменту молекул, вода также поглощает микроволновое излучение, на чём основан принцип действия микроволновой печи. Предмет гидрологии Гидрология – наука о воде (от греческого «hydro» – вода и «logos» учение, знание, наука). Гидрология – наука, занимающаяся изучением природных вод, явлений и процессов в них протекающих, закономерностей, по которым эти явления и процессы развиваются, закономерностей, определяющих распространение вод по земной поверхности и в толще почво-грунтов, а также их количественные изменения во времени. Гидрология относится к комплексу наук, изучающих физические свойства Земли, в частности такой их элемент как гидросфера, то есть гидрология – часть физической географии – науки, занимающейся изучением явлений, происходящих на поверхности земного шара, формированием и динамикой их развития, взаимосвязями и закономерностями (physis – от греческого природа). Важным рубежом в истории развития гидрологии можно считать конец XVII в., когда французские ученые Пьер Перро, Эдм Мариотт и англичанин Эдмунд Галлей на основании измерений и расчетов осадков, стока и испарения впервые установили количественные соотношения главных фаз круговорота воды. В России более или менее систематические исследования водных объектов были начаты при Петре I. Можно выделить объекты изучения гидрологии и в зависимости от объекта (в связи со специфическими особенностями процессов в них происходящих) подразделы гидрологии: · океаны и моря – гидрология моря – океанология; · реки – гидрология рек – потамология; · озера и водохранилища – лимнология; · ледники – гидрология ледников – гляциология – изучается в рамках физической географии; · гидрогеология – входит в состав гидрологии поверхностных вод суши как вспомогательная дисциплина, в объеме, необходимом для установления взаимодействия поверхностных и подземных вод и влияния подземных вод на режим поверхностных вод. Схема научных дисциплин гидрологии Помимо деления по видам изучаемых объектов в гидрологии выделяют самостоятельные разделы (научные дисциплины): 1. Гидрометрия – рассматривает методы наблюдений за режимом водных объектов и измерений гидрологических величин; применяемые для этого приборы и способы обработки результатов.
2. Гидрография – изучает и выявляет закономерности распространения поверхностных вод; дает описание водных объектов или территорий с общей характеристикой режима и хозяйственного значения, географических условий территории. 3. Общая гидрология – изучает и описывает водные объекты и их характерные свойства, устанавливает общие закономерности управляющие процессом формирования и деятельности вод суши. Изучает связь гидрологических явлений с метеорологическими факторами и условиями подстилающей поверхности. Освещает особенности проявления гидрологических закономерностей в различных водных объектах. 4-5. Инженерная гидрология – занимается разработкой методов расчета (гидрорасчеты 4) и прогноза (гидропрогнозы 5) гидрологических характеристик, необходимых в хозяйственной деятельности, строительстве гидротехнических сооружений, планировании изменений естественного режима водных объектов. 6-7. Водохозяйственные расчеты и регулирование речного стока – совокупность методов оценки соответствия водных ресурсов объектов или территории требованиям их хозяйственного использования, способов определения режима регулирования стока, параметров гидротехнических сооружений и правил их работы. 8. Гидрофизика – изучает физические и механические свойства вод (испарение, образование и таяние льда и снега, влагосодержание почв). 9-10. Динамика вод суши и русловые процессы – изучает закономерности перемещения водных масс и наносов, течения, волнение, сгонно-нагонные явления; закономерности формирования берегов и русел рек, явления размыва, перемещения и отложения (аккумуляции) частиц грунтов, слагающих русло и берега. 11. Гидрохимия – изучает химические свойства и состав вод суши. В настоящее время ее важной задачей является разработка некоторых сторон проблемы качества воды. 12. Охрана водных ресурсов – в последнее время развивается направление, занимающееся разработкой научных основ рационального использования и охраны водных ресурсов с целью предотвращения их истощения, загрязнения и неблагоприятного изменения водного режима. В рамках этого направления развивается гидроэкология, изучающая не просто изменения водных ресурсов, гидрологического режима и качества вод, а влияние этих изменений на экологическое состояние водных объектов и окружающей природной среды. Гидрология опирается на обшеобразовательные дисциплины и специальные дисциплины из смежных отраслей знаний: метеорология, климатология, гидравлика, гидродинамика, гидрогеология, геоморфология, почвоведение. Методы гидрологических исследований 2. Экспедиционный – в течение короткого времени исследуется по определенной программе некоторая территория. 3. Экспериментальный – детальное исследование какого-либо гидрологического процесса в лабораторных или природных условиях (физическое меделирование процессов). 4. Теоретический – использование общих физических законов и математических методов для решения гидрологических задач. Результаты проверяются на фактическом материале.
|
|||||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 69; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.17.181.21 (0.022 с.) |
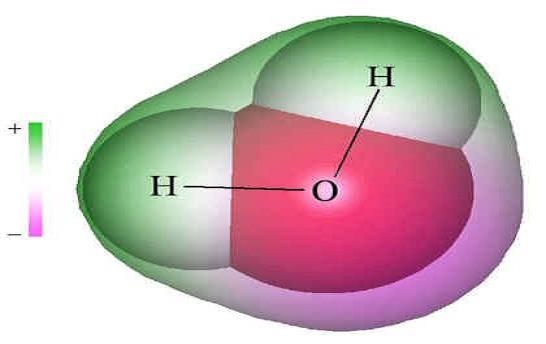
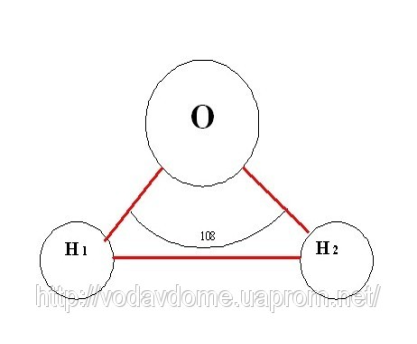 Высокая вязкость. Высокое поверхностное натяжение. Вода практически несжимаема. Отрицательный электрический потенциал поверхности воды. Особенности физических свойств воды обусловлены водородными связями. Молекула воды несимметрична: три ядра образуют равнобедренный треугольник с ядрами водорода в основании и ядром кислорода в вершине (радиус молекул воды значительно меньше внутримолекулярного расстояния, т.е. молекулы воды “упакованы” не слишком плотно).
Высокая вязкость. Высокое поверхностное натяжение. Вода практически несжимаема. Отрицательный электрический потенциал поверхности воды. Особенности физических свойств воды обусловлены водородными связями. Молекула воды несимметрична: три ядра образуют равнобедренный треугольник с ядрами водорода в основании и ядром кислорода в вершине (радиус молекул воды значительно меньше внутримолекулярного расстояния, т.е. молекулы воды “упакованы” не слишком плотно).