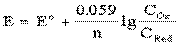Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Строение водородного электродаСодержание книги
Поиск на нашем сайте
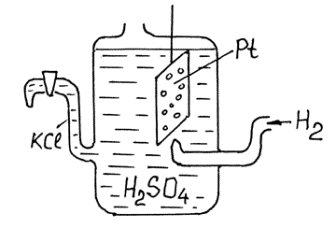
Водородный электрод состоит из платиновой пластины, покрытой платиновой чернью. Пластина помещена в водный раствор серной кислоты с концентрацией [H+] = 1 моль/л, (рН=0). Пластина омывается струей водорода с давлением 1 атм. Процесс, происходящий на пластине H+aq + e ® ½(H2) EoH= 0. Все остальные стандартные окислительно-восстановительные потенциалы, отнесенные к концентрации 1 моль/л при р=1 атм и t= 25oC, измерены относительно водородного электрода.
Ряд напряжений металлов Если пластинку металла, погруженную в раствор его соли, при концентрации 1 моль/л и t = 25◦ С соединить с водородным электродом, получится гальванический элемент, ЭДС которого легко измерить. ЭДС такого металлического элемента это стандартный электродный потенциал. Все металлы, по значениям Е0 располагаются в рад напряжения металлов. Этот ряд характеризует химические свойства металлов. Его используют: 1) для определения последовательности разряда ионов при электролизе; 2) для описания общих свойств металлов. Как пользоваться этим рядом? Правила: 1. Чем больше отрицательное значение Е0, тем лучшими восстановительными свойствами обладает металл. Li – лучший восстановитель, Au – самый слабый восстановитель. 2. Каждый вышестоящий в ряду напряжения металл вытесняет нижестоящие металлы из растворов их солей. 3. Металлы, стоящие в ряду напряжения до водорода вытесняют водород из разбавленных кислот (кроме НNO3) 4. Чем больше разность потенциалов у двух металлов, тем больше ЭДС у гальванического элемента, который построен из них. Окислительно-восстановительные потенциалы В качестве электродов могут быть использованы окислительно-восстановительные системы или пары, составленные из окисленной и восстановленной форм. Записывают: окисленная форма / восстановленная форма. Например: Fe3+ / Fe2+; MnO4- + 8H+ / Mn2+ + 4H2O Потенциал Е окислительно – восстановительной пары вычисляется по уравнению Нернста: Cox и CRed - концентрации окисленной и восстановленной форм соответственно. Для стандартных условий (298 К) его можно записать следующим образом: Е – окислительно-восстановительный потенциал данный пары в Вольтах Е0 – стандартный окислительно-восстановительный потенциал (приведен в справочниках) n – число электронов, участвующих в ОВР Cox – концентрация окисленной формы в системе (моль/л). CRed – концентрация восстановленной формы (моль/л). Если Cox = CRed; и Cox / CRed = 1, тогда Е = Е0 Стандартным электродным окислительно-восстановительным потенциалом (редокс потенциалом) называется потенциал окислительно- восстановительной системы, измеренный по отношению к стандартному водородному электроду, принятому за 0, когда отношение концентраций окисленной и восстановленной форм равно 1. Пример: Е0 MnO4- + 8H+ / Mn2+ + 4H2O = +1,51 В Плюс (+) означает, что электроны движутся от водородного электрода. Е0Zn2+ | Zn = - 0,76 В Минус (-) означает, что электроны движутся к водородному электроду. Значение редокс потенциалов (Е0) находятся в таблице. При расчетах знак потенциала не менять.
В этой таблице сильные окислители находятся в левом нижнем углу, сильные восстановители - в правом верхнем. Анализ ряда: 1) Чем > электроположительное значение Е0 пары, тем > окислительными свойствами обладает окисленная форма пары. 2) Чем > электроотрицательное значение Е0 пары,тем > восстановительными свойствами обладает восстановленная форма пары.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-11; просмотров: 377; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.20 (0.008 с.) |