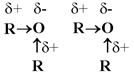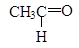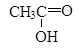Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Что происходит со спиртом, если к нему добавить кислоту? ⇐ ПредыдущаяСтр 4 из 4
То же самое:
Образуется ион алкоксония. Что надо помнить об этих реакциях? 1. Наряду с информацией о кислотных свойствах воды и спиртов (см. предыдущий урок), эти реакции говорят об амфотерности[1] воды и спиртов. 2. Эти реакции обратимы. Нуклеофильное замещение Отрицательно заряженный анион кислоты может «вытеснить» молекулу воды из иона алкоксония, заняв ее место:
В результате реакции происходит нуклеофильноезамещение гидроксильной группы спирта на анион кислоты:
Нуклеофильные реакции – реакции, заключающиеся в атаке реагента, имеющего избыточную электронную плотность, на атом углерода с частичным положительным зарядом. Нуклеофильное замещение (SN) отличается от других реакций замещения тем, что атом углерода, по которому происходит атака реагента, несет частичный положительный заряд. Реагент является нуклеофилом (Nu) – частицей с избытком электронной плотности. Пример нуклеофильного замещения – реакция этерификации Реакция этерификации — реакция образования сложного эфира[2] при взаимодействии спирта и кислоты:
этилсульфат В избытке спирта:
диэтилсульфат При нагревании эти эфиры разлагаются с выделением серной кислоты:
этилен
диэтиловый эфир Т.е. взаимодействие спирта с серной кислотой при нагревании сводится к дегидратации спирта, а серная кислота играет роль катализатора (отбирает воду):
Простые эфиры Простые эфиры – вещества, в которых два углеводородных радикала соединены между собой через атом кислорода: R1–O–R2 1. Простые эфиры называют, перечисляя углеводородные радикалы в алфавитном порядке и добавляя слово «эфир». Если радикалы одинаковы, это обозначают частицей «ди»: СН3-О-С2Н5 метилэтиловый эфир С4Н9-О-СН3 бутилметиловый эфир С4Н9-О-С4Н9 дибутиловый эфир 2. Простые эфиры изомерны спиртам: Например, веществу состава С2Н6О будут соответствовать изомеры: С2Н5ОН этиловый спирт и СН3-О-СН3 диметиловый эфир. 3. Простые эфиры не могут образовывать водородные связи, т.к. в них нет связи Н-О. Поэтому они плохо растворимы в воде, и температуры кипения эфиров намного ниже температур кипения соответствующих спиртов.
Табл. 1
Различие в физических свойствах спиртов и эфиров (см. Табл. 1) из-за того, что в эфирах нет водородной связи. Это также объясняет высокую летучесть этих веществ. Горение Все органические вещества горят. Спирты – не исключение. Рис. 1. С2Н5ОН + 3О2 = 2СО2 + 3Н2О. При горении образуются углекислый газ и вода.
Рис. 1. Спиртовка Ферментативное окисление Этанол окисляется в печени под действием фермента, превращаясь в этаналь – вещество, относящееся к классу альдегидов[1]: Рис. 4.
Обычно организм быстро окисляет этаналь дальше, переводя его с помощью другого фермента в уксусную кислоту:
Если человек злоупотребил алкоголем, то организм не справляется с переработкой этаналя, и наступает отравление, называемое похмельем (Рис. 2).
Рис. 2. Похмелье
|
||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-11; просмотров: 585; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.20.235.88 (0.007 с.) |

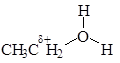 + Cl- → CH3CH2 Cl + H2O
+ Cl- → CH3CH2 Cl + H2O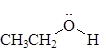 + HCl → CH3CH2 Cl + H2O
+ HCl → CH3CH2 Cl + H2O
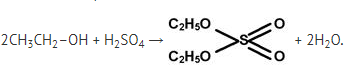



 Но:
Но: