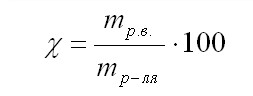Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Способы выражения концентрации растворов.
1. Массовая доля (или процентная концентрация вещества) – это отношение массы растворенного вещества m к общей массе раствора. Для бинарного раствора, состоящего из растворённого вещества и растворителя:
где: ω – массовая доля растворенного вещества; mв-ва – масса растворённого вещества; mр-ра – масса растворителя. Массовую долю выражают в долях от единицы или в процентах. 2. Молярная концентрация или молярность – это количество молей растворённого вещества в одном литре раствора V:
где: C – молярная концентрация растворённого вещества, моль/л (возможно также обозначение М, например, 0,2 М HCl); n – количество растворенного вещества, моль; V – объём раствора, л. Раствор называют молярным или одномолярным, если в 1 литре раствора растворено 1 моль вещества, децимолярным – растворено 0,1 моля вещества, сантимолярным – растворено 0,01 моля вещества, миллимолярным – растворено 0,001 моля вещества. 3. Моляльная концентрация (моляльность) раствора С(x) показывает количество молей n растворенного вещества в 1 кг растворителя m:
где: С (x) – моляльность, моль/кг; n – количество растворенного вещества, моль; mр-ля – масса растворителя, кг. 4. Титр – содержание вещества в граммах в 1 мл раствора:
где: T – титр растворённого вещества, г/мл; mв-ва – масса растворенного вещества, г; Vр-ра – объём раствора, мл. 5. Мольная доля растворённого вещества – безразмерная величина, равная отношению количества растворенного вещества n к общему количеству веществ в растворе:
где: N – мольная доля растворённого вещества; n – количество растворённого вещества, моль; nр-ля – количество вещества растворителя, моль. Сумма мольных долей должна равняться 1: N(X) + N(S) = 1. где N(X) - мольная доля растворенного вещества Х; N(S) - мольная доля растворенного вещества S. Иногда при решении задач необходимо переходить от одних единиц выражения к другим:
ω(X) - массовая доля растворенного вещества, в %; М(Х) – молярная масса растворенного вещества; ρ= m/(1000V) – плотность раствора. 6. Нормальная концентрация растворов (нормальность или молярная концентрация эквивалента)– число грамм-эквивалентов данного вещества в одном литре раствора. Грамм-эквивалент вещества – количество граммов вещества, численно равное его эквиваленту.
Эквивалент – это условная единица, равноценная одному иону водорода в кислотоно-основных реакциях или одному электрону в окислительно – восстановительных реакциях. Для записи концентрации таких растворов используют сокращения н или N. Например, раствор, содержащий 0,1 моль-экв/л, называют децинормальным и записывают как 0,1 н.
где: СН – нормальная концентрация, моль-экв/л; z – число эквивалентности; Vр-ра – объём раствора, л. Растворимость вещества S - максимальная масса вещества, которая может раствориться в 100 г растворителя:
Коэффициент растворимости – отношение массы вещества, образующего насыщенный раствор при конкретной температуре, к массе растворителя: Растворимость. Растворимость (Р, χ или k s ) – это характеристика насыщенного раствора, которая показывает, какая масса растворенного вещества может максимально раствориться в 100 г растворителя. Размерность растворимости — г/ 100 г воды. Поскольку мы определяем массу соли, которая приходится на 100 г воды, в формулу растворимости добавляем множитель 100:
здесь m р.в. – масса растворенного вещества, г m р-ля – масса растворителя, г Иногда используют обозначение коэффициент растворимости k S. Задачи на растворимость, как правило, вызывают сложности, так как эта физическая величина для школьников не очень привычна. Растворимость веществ в различных растворителях меняется в широких пределах. В таблице приведена растворимость некоторых веществ в воде при 20oС:
От чего же зависит растворимость веществ? От ряда факторов: от природы растворенного вещества и растворителя, от температуры и давления. В справочных таблицах предлагается вещества делят на хорошо растворимые, малорастворимые и нерастворимые. Такое деление очень условное, поскольку абсолютно нерастворимых веществ нет. Даже серебро и золото растворимы в воде, однако их растворимость настолько мала, что можно пренебречь ей.
Зависимость растворимости от природы растворенного вещества и растворителя* Растворимость твёрдых веществ в жидкостях зависит от структуры твёрдого вещества (от типа кристаллической решётки твёрдого вещества). Например, вещества с металлическими кристаллическими решётками (железо, медь и др.) очень мало растворимы в воде. Вещества с ионной кристаллической решёткой, как правило, хорошо растворимы в воде. Есть замечательное правило: “ подобное хорошо растворяется в подобном ”. Вещества с ионным или полярным типом связи хорошо растворяются в полярных растворителях. Например, соли хорошо растворимы в воде. В то же время неполярные вещества, как правило, хорошо растворяются в неполярных растворителях. Большинство солей щелочных металлов и аммония хорошо растворимы в воде. Хорошо растворимы почти все нитраты, нитриты и многие галогениды (кроме галогенидов серебра, ртути, свинца и таллия) и сульфаты (кроме сульфатов щёлочноземельных металлов, серебра и свинца). Для переходных металлов характерна небольшая растворимость их сульфидов, фосфатов, карбонатов и некоторых других солей. Растворимость газов в жидкостях также зависит от их природы. Например, в 100 объёмах воды при 20oС растворяется 2 объёма водорода, 3 объёма кислорода. В тех же условиях в 1 объёме Н2О растворяется 700 объёмов аммиака. Влияние температуры на растворимость газов, твёрдых веществ и жидкостей* Растворение газов в воде вследствие гидратации молекул растворяемого газа сопровождается выделением теплоты. Поэтому при повышении температуры растворимость газов понижается. Температура различным образом влияет на растворимость твёрдых веществ в воде. В большинстве случаев растворимость твёрдых веществ возрастает с повышением температуры. Например, растворимость нитрата натрия NaNO3 и нитрата калия КNO3 при нагревании увеличивается (процесс растворения протекает с поглощением теплоты). Растворимость NaCl при увеличении температуры возрастает незначительно, что связано с почти нулевым тепловым эффектом растворения поваренной соли. Влияние давления на растворимость газов, твёрдых веществ и жидкостей* На растворимость твёрдых и жидких веществ в жидкостях давление практически не оказывает влияния, так как изменение объёма при растворении невелико. При растворении газообразных веществ в жидкости происходит уменьшение объёма системы, поэтому повышение давления приводит к увеличению растворимости газов. В общем виде зависимость растворимости газов от давления подчиняется закону У. Генри (Англия, 1803 г.): растворимость газа при постоянной температуре прямо пропорциональна его давлению над жидкостью. Закон Генри справедлив лишь при небольших давлениях для газов, растворимость которых сравнительно невелика и при условии отсутствия химического взаимодействия между молекулами растворяемого газа и растворителем. Влияние посторонних веществ на растворимость* В присутствии в воде других веществ (солей, кислот и щелочей) растворимость газов уменьшается. Растворимость газообразного хлора в насыщенном водном растворе поваренной соли в 10 раз меньше. Чем в чистой воде. Эффект понижения растворимости в присутствии солей называется высаливанием. Понижение растворимости обусловлено гидратацией солей, что вызывает уменьшение числа свободных молекул воды. Молекулы воды, связанные с ионами электролита, уже не являются растворителем для других веществ.
|
|||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-02-07; просмотров: 1007; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.185.169 (0.018 с.) |
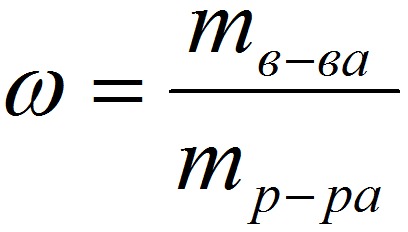 ,
,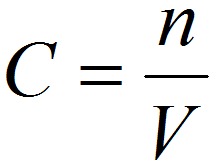 ,
, ,
,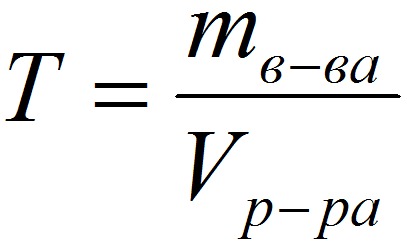 ,
, ,
,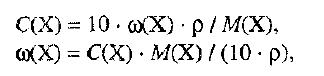
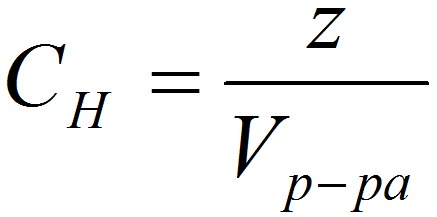 ,
,